Биология в лицее
Site biology teachers lyceum № 2 Voronezh city, Russian Federation
Биосинтез белка создает полимерную молекулу из готовых мономеров – аминокислот, уже имеющихся в клетке. Этот процесс осуществляется за счет внутренней энергии клетки (АТФ).
Биосинтез углеводов идет принципиально иначе. В клетках растений мономеры – моносахариды – образуются из неорганических веществ (углекислого газа и воды). Осуществляется этот процесс с помощью энергии света, поступающей в клетку из внешней среды. Этот процесс называют фотосинтезом (от греч. photos – «свет» и synthesis – «соединение»).
Созданные в клетке моносахариды (глюкоза, фруктоза) как первичные продукты фотосинтеза используются затем для биосинтеза различных полисахаридов, сложных белковых соединений, жирных кислот, нуклеиновых кислот и многих других органических соединений.
Фотосинтез – процесс, чрезвычайно важный для всего живого населения планеты. Он происходит в клетках зеленых растений с помощью пигментов ( хлорофилла и других), находящихся в пластидах.
Хлоропласты – это внутриклеточные органоиды (пластиды), которые благодаря пигменту хлорофиллу окрашены в зеленый цвет. В растительной клетке обычно содержится от 15 до 50 хлоропластов.
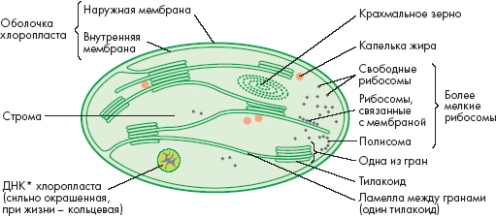
Фотосинтез – сложный многоступенчатый процесс. Начало ему задает свет. Многолетние исследования фотосинтеза показали, что он включает в себя две стадии: световую и темновую.
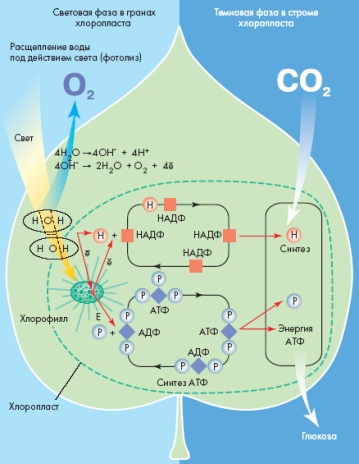
Образовавшийся при расщеплении воды водород с помощью электронов присоединяется к веществу, способному транспортировать водород в пределах хлоропласта. Таким веществом является сложное органическое соединение из группы ферментов – окисленный никотинамидаденин-динуклеотидфосфат, или НАДФ. Присоединив водород, НАДФ восстанавливается до НАДФ • Н. В такой химической связи запасается энергия, и заканчивается первая стадия фотосинтеза.
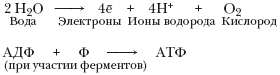
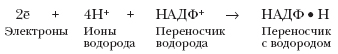
Участие энергии света здесь является обязательным условием. Поэтому данную стадию называют еще стадией световых реакций.
Кислород, образующийся на первой стадии фотосинтеза как побочный продукт при расщеплении воды, выводится наружу или используется клеткой для дыхания.
Вторая стадия фотосинтеза – темновая. Здесь используются образовавшиеся в процессе световых реакций продукты. С их помощью происходит преобразование углекислого газа в простые углеводы – моносахариды. Их создание идет путем большого количества реакций восстановления СО2 за счет энергии АТФ и восстановительной возможности НАДФ • Н. В результате этих реакций образуются молекулы глюкозы (С6Н12О6), из которых путем полимеризации создаются полисахариды – целлюлоза, крахмал, гликоген и другие сложные органические соединения. Поскольку все реакции на этой стадии идут без участия света, ее называют стадией темновых реакций.
Все световые реакции (первая стадия фотосинтеза) происходят на мембранах хлоропласта – в тилакоидах, а темновые (вторая стадия фотосинтеза) – между мембранами внутри хлоропласта – в строме.
Сложный поэтапный процесс фотосинтеза идет непрерывно, пока зеленые клетки получают световую энергию.
На скорость фотосинтеза влияют внешние условия среды: интенсивность освещения, концентрация углекислого газа и температура. Если эти параметры достигают оптимальных величин, происходит усиление фотосинтеза. Благодаря фотосинтезу примерно 1–1,5% энергии Солнца, получаемой зелеными растениями, запасается в органических молекулах. Фотосинтезирующие организмы дают пищу гетеротрофам, а также кислород, необходимый для дыхания всем живым существам на планете. Установлено, что 21% кислорода в современной атмосфере Земли создан главным образом путем фотосинтеза.
Фотосинтез – уникальный процесс создания зелеными клетками органических веществ из неорганических, притом идущий в огромных масштабах на суше и в воде. Ежегодно растения связывают 1,7 млрд т углерода, образуя при этом более 150 млрд т органического вещества и выделяя около 200 млрд т кислорода.
Фотосинтез – единственный на нашей планете процесс превращения энергии солнечного света в энергию химических связей органических веществ. Таким способом энергия Солнца, поступившая из космоса, преобразуется и запасается клетками зеленых растений в углеводах, белках и липидах, обеспечивая жизнедеятельность всего гетеротрофного населения живого мира – от бактерий до человека.
Вот почему выдающийся русский ученый–естествоиспытатель К. А. Тимирязев эту роль зеленых растений для жизни на Земле назвал космической.
Биосинтез углеводов
В тканях и органах человека происходит синтез сложных углеводов. Строительным блоком (мономерным звеном) для синтеза служит глюкоза. Большая часть глюкозы поступает в организм человека с пищей, однако при длительном голодании может включаться механизм синтеза глюкозы из неуглеводных источников.
Глюконеогенез— процесс новообразования глюкозы из неуглеводных источников. В качестве субстратов глюконеогенеза могут служить аминокислоты, превращающиеся в пировиноградную и в щавелевоуксусную кислоты; такие аминокислоты называютсягликогенными. К гликогенным относятся все протеиногенные аминокислоты, кроме лейцина. Также к неуглеводным источникам глюконеогенеза относятся глицерин, кислоты цикла Кребса, молочная кислота. Преобразование всех указанных веществ (кроме глицерина) в глюкозу проходит через стадию пировиноградной и щавелевоуксусной кислот.
Большая часть реакций на пути от пирувата до глюкозы катализируется ферментами гликолиза путем обращения соответствующих реакций. Однако нормальный путь гликолиза («сверх вниз») включает 4 необратимых этапа, которые не могут быть использованы в глюконеогенезе, идущем «снизу вверх». Это реакции, катализируемые гексокиназой, фосфофруктокиназой, фосфоглицераткиназой и пируваткиназой; в глюконеогенезе эти этапы осуществляются обходными путями.
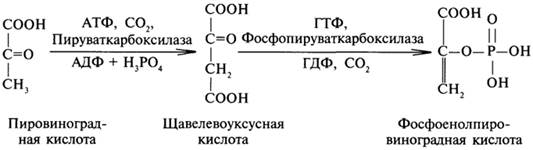
Превращение ПВК в фосфоенолпировиноградную кислоту происходит через стадию образования щавелевоуксусной кислоты:
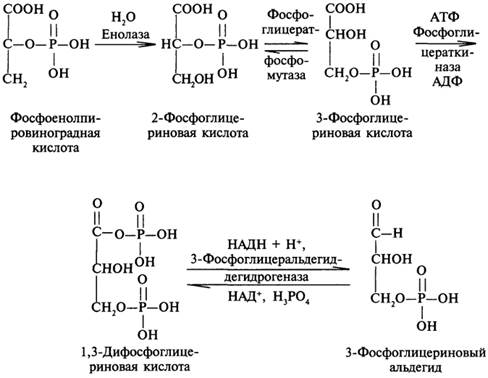
Далее фосфоенолпировиноградная кислота превращается в фосфотриозы, которые дают фруктозо-1,6-дифосфат:
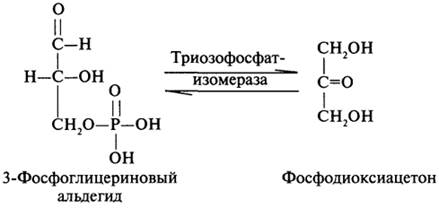
Для образования фруктозе-1,6-дифосфата требуется две молекулы 3-фосфоглицеринового альдегида, одна из которых превратится в фосфодиоксиацетон при участии фермента триозофосфатизомеразы:
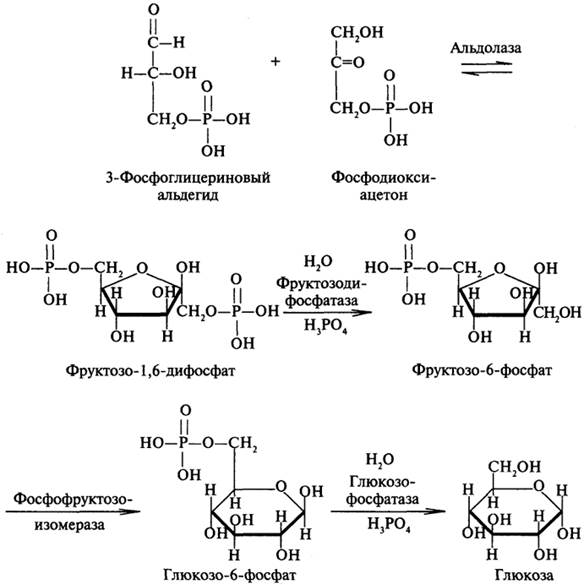
Далее из этих двух фосфотриоз образуется фруктозо-1,6-дифосфат. На последних стадиях глюконеогенеза «работают» ферменты фосфатазы, которые не представлены в гликолизе. Это еще один факт, подтверждающий самостоятельность глюконеогенеза:
Столь подробное рассмотрение процесса глюконеогенеза связано с тем, что этот метаболический путь использует молочную кислоту, накапливающуюся в мышцах во время интенсивной мышечной работы. Следовательно, глюконеогенез, протекающий в печени, можно рассматривать как приспособление для разгрузки организма от молочной кислоты, образующейся в мышцах в анаэробных условиях.
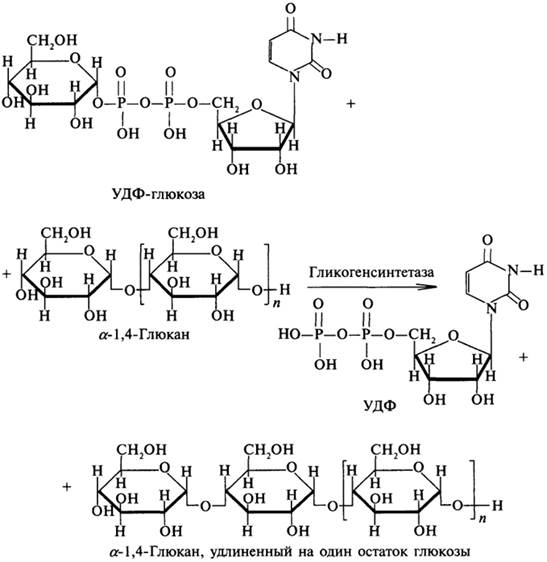
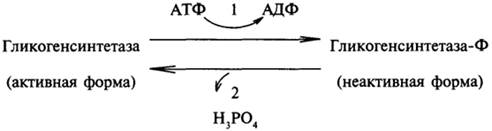
Синтез гликогена осуществляет фермент гликогенсинтетаза. Фермент снимает остаток глюкозы с УДФ-глюкозы и переносит его на нередуцирующий конец растущей цепи гликогена:
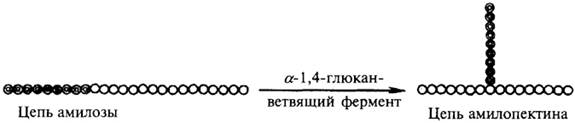
Гликогенсинтетаза ведет синтез цепи амилозного типа. Разветвленная структура образуется путем переноса полиглюкозидной цепи у α-1,4-глюкана из положения 4 в положение 6. Этот механизм реализуется с помощью фермента, который называется α-1,4-глюканветвящий фермент. Трансгликозилирование, катализируемое этим ферментом, можно схематично представить следующим образом.
Интеграция разных путей обмена углеводов в организме.Интенсивность катаболических и анаболических путей обмена углеводов в разных тканях организма неодинакова и определяется прежде всего особенностями обмена каждой ткани и органа. Если рассматривать организм в целом, то можно выявить некоторую специализацию путей превращения углеводов в отдельных тканях. Такая специализация, несомненно, оправдана, так как отвечает функциональной направленности ткани или органа. Поскольку функционирование отдельных органов обеспечивает жизнедеятельность всего организма, существенным моментом в обмене веществ в целом и в обмене углеводов в частности является интеграция катаболических и анаболических процессов.
Приведем пример. При активной мышечной работе затрачиваются большие количества энергии, которая первоначально извлекается в ходе распада гликогена до молочной кислоты.
Схема действия α-1,4-глюканветвящего фермента.
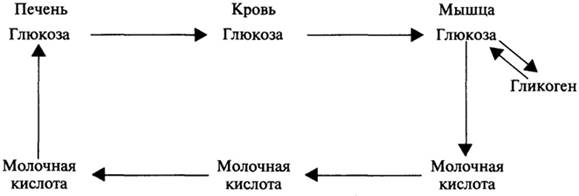
Молочная кислота, как говорилось выше, вымывается в кровь, которая доставляет ее в печень, где происходит синтез глюкозы в ходе глюконеогенеза. Глюкоза из печени переносится кровью в скелетные мышцы, где либо расходуется на образование энергии, либо запасается в виде гликогена. Этот межорганный цикл в обмене углеводов получил название цикла Кори:
Дата добавления: 2015-03-14 ; просмотров: 6427 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Биосинтез углеводов: кратко и понятно 9 класс
Биосинтез углеводов: кратко и понятно
Затем глю-6-ф превращается в глю-1-ф. В процессе активации глю-1-ф участвуют уридиннуклеотиды. В ходе этого процесса два концевых фосфорных остатка УДФ освобождаются в виде неорганического пирофосфата͵ остаток УМФ соединяется с глю-1-ф, образуя УДФ-глюкозу.
Глюкоза как моносахарид свободно диффундирует через мембрану печеночных клеток, она не может служить резервом углеводородов в печени. Так как фосфатные эфиры глюкозы и фруктозы не столь легко проникают через мембраны, фосфорилирование этих сахаров создает как бы ловушку для них, эффективно изолируя реакции гликолиза и фосфоглюконатного пути в пределах внутриклеточного отсека. Тем не менее фосфаты сахаров не могут накапливаться в больших количествах в печени, так как благодаря осмосу увеличение их запасов будет сопровождаться накоплением больших количеств воды.
Обмен гликогена
Реакции пентозофосфатного пути протекают в цитозоле.
Образование АТФ.
По другому вторичному пути катаболизма глюкозы в животных тканях образуются два специализированных продукта: D-глюконат, важная роль которого связана с обезвреживанием и выведением из организма чужеродных органических веществ, и L-аскорбиновая кислота (витамин С).
Взаимосвязь пентозного пути и гликолиза.
В печени происходит превращение избытка углеводов в нерастворимый полимер – гликоген. Эта резервная форма глюкозы может составлять одну десятую всей массы печени. При голодании запас гликогена почти полностью истощается.
Обмен гликогена включает в себя 2 процесса: гликогенез или синтез гликогена и гликогенолиз или распад гликогена.
Гликогенез – синтез гликогена — ϶ᴛᴏ анаболический процесс, требующий затраты энергии в форме как АТФ, так и уридинтрифосфата (УТФ). Исходным источником для синтеза гликогена является глю, d под действием глюкокиназы превращается в глю-6-фосфат.
Глю-6-ф занимает ключевое положение как общий промежуточный продукт ряда процессов углеводного обмена: он способен к обратимому превращению в пируват путем гликолиза или глюконеогенеза, а также к необратимому – в пентозы в ходе фосфоглюконатного пути. Глю-6-ф может обратимо превращаться в гликоген.
Источником глю при синтезе гликогена является УДФ-глю, d образуется из глюкозо-1-ф и УТФ:
Глю-1-ф + УТФ 
На следующей стадии происходит перенос остатка глю с УДФ-глю на затравку гликогена с помощью гликогенсинтетазы:
УДФ-глю + (глю)n
Гликогенсинтетаза катализирует образование только 

Гликогенолиз – распад гликогена идет путем фосфоролиза.
Гликолиз, пентозофосфатный путь, гликогенолиз — ϶ᴛᴏ катаболические пути, которые сходятся в цикле лимонной кислоты, чтобы передать свои богатые энергией электроны в дыхательную цепь. Перемещаясь по дыхательной цепи к кислороду, эти электроны поставляют энергию для синтеза АТФ. Теперь нам предстоит рассмотреть анаболические пути. На этих путях химическая энергия в форме АТФ и НАДФН используется для синтеза клеточных компонентов из простых предшественников.
Анаболизм прокариот
Основные компоненты прокариотной клетки состоят из органических веществ-полисахаридов, белков, нуклеиновых кислот, липидов, большинство из которых (исключая липиды) являются полимерами. Образованию полимеров предшествует биосинтез мономеров, их составляющих. На процессы биосинтеза мономеров и реакции их полимеризации расходуется большая часть энергии, получаемой клеткой в процессах катаболизма.
Биосинтез углеводов.Прокариоты способны синтезировать моно-, олиго-, и полисахариды, а также и другие соединения, в состав которых входят углеводы.
Для прокариот-автотрофов исходным продуктом для синтеза углеводов является СО2.
Фотосинтезирующие автотрофные микроорганизмы фиксируют СО2 и осуществляют биосинтез углеводов также, как растения при фотосинтезе, через восстановительный пентозофосфатный цикл, или цикл Кальвина. Из клеток автотрофных прокариот выделены два специфических фермента этого цикла:
1. Фосфорибулокиназа, фосфорилирующая рибулозо-5-фосфат при участии АТФ в рибулозо-1,5-дифосфат, выступающий далее акцептором СО2.
Рибулозодифосфаткарбоксилаза, катализирующая реакцию фиксации СО2 рибулозо-1,5-дифосфатом с образованием двух молекул
3-фосфоглицериновой кислоты. 3-ФГК подвергается различным превращениям до получения глюкозы.
Подобным образом фиксируют СО2 и ведут синтез углеводов хемосинтезирующие автотрофные микроорганизмы.
Но они используют энергию АТФ, получаемую клеткой в результате реакций окисления неорганических веществ субстрата.
Моносахариды, образовавшиеся в результате фиксации СО2, используются на синтез олиго- и полисахаридов.
Биосинтез углеводов
Биосинтез полисахаридов осуществляется путем трансгликозилирования (переноса остатков моносахаридов на конец растущей цепи полисахарида) и всегда сопровождается затратой энергии.
Прокариоты-гетеротрофы способны синтезировать углеводы из С2 и С3-соединений, используя при этом реакции гликолитического пути, идущие в обратном направлении.
Все гетеротрофные микроорганизмы, помимо усвоения органических углерод содержащих веществ, фиксируют углекислый газ и используют его в реакциях анаболизма и катаболизма.
Включение СО2 в вещества клетки у гетеротрофных микроорганизмов происходит в реакциях карбоксилирования. В большинстве случаев акцепторами СО2 выступают органические кислоты, например реакции карбоксилирования пировиноградной кислоты с образованием щавелевоуксусной (ЩУК) или яблочной кислот:
СН3-СО-СООН + СО2 +АТФ пируваткарбоксилазаНООС-СН2-СО-СООН + +АДФ+Фн.
СН3-СО-СООН +СО2 +НАД(Ф)Н малатдегидрогеназа НООС-СН2-СНОН-СООН +НАД(Ф)+
Как осуществляется биосинтез углеводов?
Биосинтез крахмала начинается с глюкозо-6-фосфата. Донором глюкозы служит сахароза. На первой стадии синтеза глюкозо-6-фосфат превращается в глюкозо-1-фосфат.
На второй стадии образуется донор активированной глюкозы:
АТФ + глюкозо-1-фосфат АДФГ + пирофосфат
Для большинства растений донором активированной глюкозы является АДФГ.
На третьей стадии синтеза осуществляется перенос активированной глюкозы от АДФГ на акцептор.
Акцептором, или затравкой, в данном случае служит небольшая молекула полисахарида, состоящая иногда всего лишь из 3-4 остатков глюкозы, соединенных гликозидными связями. Реакцию катализирует фермент из подкласса гликозилтрансфераз.
В результате затравка постепенно удлиняется. Так происходит биосинтез амилозы. Затем часть амилозы используется для биосинтеза амилопектина.
Синтез амилопектина подразделяется на синтез неразветвленной и разветвленной частей. Неразветвленная часть образуется аналогично амилозе.
В синтезе разветвленной части участвует ветвящий фермент (Q-фермент), который отщепляет от неразветвленной цепочки фрагмент, построенный из остатков глюкозы, соединенных а-1,4-гликозидными связями, и переносит его к шестому атому углерода одного из остатков глюкозы неразветвленной части амилопектина.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Липиды
Липиды имеют очень большое значение в метаболизме клетки. Все липиды — ϶ᴛᴏ органические водонерастворимые соединения, присутствующие во всех живых клетках. Необходимо отметить, что по своим функциям липиды разделяются на три группы:
— структурные и рецепторные липиды клеточных мембран
— энергетическое ʼʼдепоʼʼ клеток и организмов
— витамины и гормоны ʼʼлипиднойʼʼ группы
Основу липидов составляют жирные кислоты (насыщенные и ненасыщенные) и органический спирт – глицерол.
Основную массу жирных кислот мы получаем из пищи (животной и растительной). Животные жиры — ϶ᴛᴏ смесь насыщенных (40-60%) и ненасыщенных (30-50%) жирных кислот. Растительные жиры наиболее богаты (75-90%) ненасыщенными жирными кислотами и наиболее полезны для нашего организма.
Основная масса жиров используется для энергетического обмена, расщепляясь специальными ферментами – липазами и фосфолипазами.
В результате получаются жирные кислоты и глицерин, которые в дальнейшем используются в реакциях гликолиза и цикла Кребса.С точки зрения образования молекул АТФ — жиры составляют основу энергетического запаса животных и человека.
Эукариотическая клетка получает жиры с пищей, хотя сама может синтезировать большинство жирных кислот (за исключением двух незаменимых– линолевой и линоленовой).
Синтез начинается в цитоплазме клеток с помощью сложного комплекса ферментов и заканчивается в митохондриях или гладком эндоплазматическом ретикулуме.
Исходным продуктом для синтеза большинства липидов (жиров, стероидов, фосфолипидов) служит ʼʼуниверсальнаяʼʼ молекула – ацетил-Коэнзим А (активированная уксусная кислота), являющаяся промежуточным продуктом большинства реакций катаболизма в клетке.
Жиры есть в любой клетке, но особенно много их в специальных жировых клетках – адипоцитах, образующих жировую ткань. Контролируется жировой обмен в организме специальным гормонами гипофиза, а также инсулином и адреналином.
Углеводы (моносахариды, дисахариды, полисахариды) являются важнейшими соединениями для реакций энергетического обмена.
В результате распада углеводов клетка получает большую часть энергии и промежуточные соединения для синтеза других органических соединений (белков, жиров, нуклеиновых кислот).
Основную массу сахаров клетка и организм получает извне – из пищи, но может синтезировать глюкозу и гликоген из неуглеводных соединений.
Субстратами для разного вида углеводного синтеза выступают молекулы молочной кислоты (лактат) и пировиноградной кислоты (пируват), аминокислоты и глицерин. Эти реакции идут в цитоплазме при участии целого комплекса ферментов – глюкозо-фосфотаз. Для всех реакций синтеза требуется энергия – синтез 1 молекулы глюкозы требует 6 молекул АТФ!
Основной объём собственного синтеза глюкозы протекает в клетках печени и почек, но не идет в сердце, мозге и мышцах (там нет необходимых ферментов).
По этой причине нарушения углеводного обмена в первую очередь сказываются на работе этих органов. Углеводный обмен контролируется группой гормонов: гормонами гипофиза, глюкокортикостероидными гормонами надпочечников, инсулином и глюкагоном поджелудочной железы. Нарушения гормонального баланса углеводного обмена приводит к развитию диабета.
Мы кратко рассмотрели основные части пластического обмена.
Модульная единица 8. Обмен углеводов



Лекция 5. Обмен углеводов.
Аннотация.Рассматриваются биохимические реакции первичного синтеза углеводов у С₃- и С₄-растений, взаимопревращения моносахаридов – триоз, эритрозы, пентоз и гексоз. Излагаются молекулярные механизмы синтеза и распада олиго- и полисахаридов. Даются необходимые сведения о ферментах, катализирующих реакции синтеза и превращений углеводов.
Ключевые слова:цикл Кальвина, цикл Хетча-Слэка, рибулозодифосфат-карбоксилаза, фосфопируваткарбоксилаза, фотосинтетически активная радиация (ФАР), С₃- и С₄-растения, гликолиз, цикл Кребса, пентозофосфатный цикл, фотофосфорилирование, окислительное фосфорилирование, нуклеозиддифосфатпро-изводные моносахаридов (УДФ-глюкоза, УДФ-галактоза и др.), сахарозосинтетаза, гликозилтрансферазы, амилазы, инулаза, целлюлозосинтетаза, пектиназы и пртопектиназы.
Рассматриваемые вопросы:
1. Первичный синтез углеводов у С₃- и С₄-растений.
2. Механизмы образования и взаимопревращения триоз, эритрозы, пентоз и гексоз.
3. Синтез и распад олигосахаридов и полисахаридов.
Цели и задачи изучения модульной единицы.Изучить механизмы синтеза, превращений и распада моносахаридов, олигосахаридов и полисахаридов, а также особенности действия ферментов, катализирующих эти реакции. Научить студентов использовать знания по обмену углеводов для прогнозирования биохимических процессов при обосновании технологий выращивания сельскохозяйственных культур и оценке качества растительной продукции.
Первичный синтез углеводов у С₃- и С₄-растений.
В ходе темновых реакций фотосинтеза происходит эндергонический процесс образования углеводов из диоксида углерода (СО2) и воды, в котором в качестве энергетических источников используются продукты световых реакций НАДФ×Н и АТФ. Последовательность химических превращений в темновой стадии фотосинтеза была выяснена американскими биохимиками М Кальвином, А. Бенсоном и Д. Басхемом в 1946-53 г.г. и впоследствии названа циклом Кальвина вследствие того, что открытые ими превращения имели циклический механизм. Все эти реакции протекают в строме – жидкой дисперсионной среде хлоропластов.
Для установления первичных продуктов, которые образуются при фотосинтезе из СО2 и Н2О, М. Кальвин и его сотрудники использовали культуру водорослей хлореллы, в которую вводили на свету меченный 14 С СО2 в виде Н2 14 СО3 и через короткие промежутки времени отбирали пробы клеток суспензии водорослей и фиксировали их метанолом. После этого из клеток хлореллы выделяли углеводы и другие органические вещества и в них определяли наличие радиоактивной метки, обусловленной включением в эти продукты 14 С. При этом было установлено, что при коротких экспозициях (0,1-5 сек.) клеток водорослей в суспензионной среде, содержащей 14 СО2, большая часть радиоактивной метки обнаруживалась в карбоксильной группе 3-фосфоглицериновой кислоты. Последнее свидетельствовало о том, что фосфоглицериновая кислота является первичным продуктом фотосинтеза.
В дальнейшем с использованием радиоактивной метки в виде 14 С и 32 Р было показано, что первичным акцептором, с которым взаимодействует СО2 служит рибулозо-1,5-дифосфат. И эту реакцию катализирует фермент рибулозодифосфаткарбоксилаза (4.1.1.39). Учитывая, что для образования карбоксильной группы кроме СО2 требуется еще молекула воды, первую реакцию цикла Кельвина можно записать следующим образом:
|
Диоксид углерода в ходе реакции взаимодействует с енольной формой рибулозо-1,5-дифосфата, при этом образуется неустойчивый продукт – β–кетокислота, который под действием фермента гидролизуется, превращаясь в 3-фосфоглицериновую кислоту. При этом радиоактивный углерод обнаруживается в карбоксильной группе одной из двух синтезирующихся молекул 3-фосфоглицериновой кислоты.

Рибулозодифосфаткарбоксилаза аллостерически активируется фруктозо-6-фосфатом и аллостерически ингибируется фруктозо-1,6-дифос-фатом, которые образуются при последующих превращениях в цикле Кальвина 3-фосфоглицериновой кислоты, являющейся продуктом действия данного фермента. Образовавшаяся под действием рибулозодифосфаткарбоксилазы 3-фосфоглицериновая кислота в последующих реакциях восстанавливается до альдегида.
Вначале молекула 3-фосфоглицериновой кислоты активируется путём фосфорилирования с участием АТФ. Эту реакцию катализирует фермент фосфоглицераткиназа (2.7.2.3), включающий 355 аминокислотных остатков и активируемый катионами Мg 2+ :
(Р) дегидрогеназа С–Н
риновая кислота риновый альдегид
В ходе восстановительной реакции происходит синтез 3-фосфоглицерино-вого альдегида и отщепление от 1,3-дифосфоглицериновой кислоты минерального фосфата. Участвующие в синтезе 3-фосфоглицеринового альдегида АТФ и НАДФ×Н являются продуктами световой стадии фотосинтеза.
Как было показано ранее, в результате связывания одной молекулы СО2 в первой реакции цикла Кальвина образуются 2 молекулы 3-фосфо-глицериновой кислоты, которые в ходе реакций 2 и 3 превращаются в две молекулы 3-фосфоглицеринового альдегида, а последние довольно легко изомеризуются в фосфодиоксиацетон. Реакцию изомеризации катализирует фермент триозофосфатизомераза (5.3.1.1):
С=О триозофосфат- СН2ОН (4)
риновый альдегид ацетон
Образовавшиеся триозофосфаты не накапливаются в хлоропластах. Под действием фермента альдолазы (4.1.2.13) они конденсируются, превращаясь во фруктозо-1,6-дифосфат:
ацетон новый альдегид Н–С–ОН
После этого от фруктозо-1,6-дифосфата происходит гидролитическое отщепление остатка фосфорной кислоты. Реакцию катализирует фермент фруктозо-1,6-дифосфатаза (3.1.3.11). В ходе этой реакции фруктозодифосфат превращается во фруктозо-6-фосфат:
Фруктозо-1,6-дифосфатаза – активируемый светом фермент. Его активирование происходит с участием восстановленного под действием света ферредоксина, который совместно со специфическим белком переводит фруктозо-1,6-дифосфатазу в активное состояние. От действия этого фермента зависит интенсивность включения СО2 в первой реакции цикла Кальвина. Если активность фруктозо-1,6-дифосфатазы низкая, то повышается концентрация фруктозо-1,6-дифосфата, который аллостерически ингибирует фермент рибулозодифосфаткарбоксилазу, вследствие чего понижается скорость первой реакции цикла Кальвина, катализируемой данным ферментом. А если фруктозо-1,6-дифосфатаза находится в активной форме, то повышается концентрация фруктозо-6-фосфата, являющегося аллостерическим активатором рибулозодифосфаткарбоксилазы. При таких условиях связывание СО2 проходит с максимальной скоростью.
На следующем этапе фотосинтеза фермент транскетолаза (2.2.1.1) катализирует перенос концевого двууглеродного радикала, содержащего кетонную группу, от фруктозо-6-фосфата на 3-фосфоглицериновый альдегид, который образуется в результате присоединения к рибулозо-1,5-дифосфату ещё одной молекулы СО2 и повторения реакций 2 и 3. В результате взаимодействия гексозы и триозы синтезируются новые углеводные продукты – эритрозо-4-фосфат и ксилулозо-5фосфат:
| | транскето- Н–С–ОН + С=О
Н–С–ОН 3-фосфоглицери- эритрозо-4- |
| новый альдегид фосфат СН2О(Р)
Ещё одна молекула 3-фосфоглицеринового альдегида, синтезированная в результате связывания второй молекулы СО2, изомеризуется далее в реакции 4 в фосфодиоксиацетон, который затем соединяется с эритрозо-4-фосфатом, образуя седогептулозо-1,7-дифосфат. Эту реакцию катализирует фермент трансальдолаза (2.2.1.2):
В следующей реакции происходит гидролиз седогептулозо-1,7-ди-фосфата, который катализирует специфическая фосфатаза. В ходе реакции
от седогептулозо-1,7-дифосфата отщепляется остаток фосфорной кислоты и таким образом осуществляется синтез седогептулозо-7-фосфата:
|
После этого снова вступает в действие фермент транскетолаза, катализирующий перенос двууглероного радикала с кетогруппой от седогептулозо-7-фосфата на 3-фосфоглицериновый альдегид, который синтезируется за счёт связывания в первой реакции цикла Кальвина уже третьей молекулы СО2. Продукты реакции, катализируемой транскетолазой, – пятиуглеродные производные моносахаридов ксилулозо-5-фосфат и рибозо-5-фосфат:
| | транскетолаза С=О Н–С–ОН
| 3-фосфоглицери- Н–С–ОН Н–С–ОН
Н–С–ОН новый альдегид | |
Н–С–ОН ксилулозо-5- рибозо-5-
В последующих реакциях цикла Кальвина осуществляется изоме-ризация фосфорнокислых производных пентоз, которая обеспечивает регенерацию первичного акцептора СО2 – рибулозо-1,5-дифосфата. Образовавшиеся в реакциях 7 и10 молекулы ксилулозо-5-фосфата превращаются в рибулозо-5-фосфат под действием фермента рибулозофосфатэпимеразы (5.1.3.1), который способен изменять на противоположную пространственную ориентацию водорода и гидроксильной группы у третьего углеродного атома пентозы:
|
|
Превращение рибозо-5-фосфата в рибулозо-5-фосфат катализирует фермент рибозофосфатизомераза (5.3.1.6):
|
Окончательную регенерацию первичного акцептора СО2 осуществляет фермент фосфорибулокиназа (2.7.1.19), катализирующий фосфорилирование от АТФ рибулозо-5-фосфата:
В ходе указанных выше тринадцати реакций происходит включение в состав углеводных производных трёх молекул СО2 и потребление трёх молекул первичного акцептора рибулозо-1,5-дифосфата, при этом осуществляется синтез шести молекул 3-фосфоглицеринового альдегида, из которых пять затрачиваются на регенерацию трёх молекул рибулозо-1,5-дифосфата и одна молекула 3-фосфоглицеринового альдегида остаётся как продукт темновой стадии фотосинтеза. Её синтез сопряжён с использованием биоэнергетических продуктов световой стадии фотосинтеза АТФ и НАДФ×Н.
Восстановленные динуклеотиды НАДФ×Н участвуют в реакции 3 цикла Кальвина, которая в ходе синтеза 6 молекул 3-фосфоглицери-нового альдегида повторяется 6 раз и, следовательно, в этих реакциях потребляются 6 молекул восстановленных динуклеотидов НАДФ×Н. АТФ участвует в реакции 2, которая, как и реакция 3, повторяется 6 раз, и в реакции 13, которая при синтезе 3 молекул первичного акцептора СО2 рибулозо-1,5-дифосфата повторяется 3 раза. Всего при связывании 3 молекул СО2 и восстановлении их до уровня 3-фосфоглицеринового альдегида потребляется 9 молекул АТФ.
Однако 3-фосфоглицериновый альдегид не накапливается в хлоропластах, он используется для синтеза гексозы. Часть молекул 3-фосфогли-церинового альдегида изомеризуется в фосфодиоксиацетон, который далее под действием альдолазы конденсируется с оставшимися молекулами 3-фосфоглицеринового альдегида и, таким образом, осуществляется синтез фруктозо-1,6-дифосфата. После гидролиза фруктозодифосфата с участием фруктозо-1,6-дифосфатазы образуется фруктозо-6-фосфат. Если учесть, что для синтеза фруктозо-6-фосфата потребуется связывание 6 молекул СО2 в первой реакции цикла Кальвина и все выше указанные превращения, связанные с синтезом одной молекулы 3-фосфоглицеринового альдегида, должны повториться еще раз, суммарное уравнение темновой стадии фотосинтеза может быть записано в следующем виде:
6СО2 + 11Н2О + 18АТФ + 12НАДФ×Н + 12Н + ¾® фруктозо-6-фосфат + 18АДФ +
+ 12НАДФ + + 17Н3РО4 цикла Кальвина
В опытах с использованием СО2, меченного 14 С, было показано, что в течение 1-3 минут после экспозиции растений в атмосфере 14 СО2 все промежуточные продукты цикла Кальвина насыщаются меченым углеродом, а при более длительных экспозициях 14 С обнаруживается уже в составе сахарозы, крахмала, органических кислот, аминокислот, липидов, белков и других органических веществ хлоропластов.
Следует отметить, что из всех реакций цикла Кальвина только первая и последняя (13) специфичны для фотосинтезирующих клеток, тогда как другие реакции могут протекать в любых других клетках и тканях фотосинтезирующих организмов в ходе синтеза, распада и превращений углеводов. При этом промежуточные метаболиты, образующиеся в цикле Кальвина, выводятся из этого цикла и потребляются для синтеза различных органических веществ в хлоропластах и листьях растений. Конечный продукт цикла Кальвина фруктозо-6-фосфат также включается в биосинтетические реакции, происходящие в фотосинтезирующих тканях, или превращается в транспортные формы, которые по сосудам флоэмы поступают в акцепторные органы растений.
Фотодыхание.Изучение механизма действия фермента рибулозоди-фосфаткарбоксилазы показало, что конкурентным ингибитором этого фермента является кислород, который конкурирует с СО2 при взаимодействии последнего с каталитическим центром ферментного белка. Поэтому при высокой концентрации кислорода и низкой концентрации СО2 в воздухе карбоксилирующая активность рибулозодифосфат-карбоксилазы понижается, но усиливается её оксигеназная способность, вследствие чего к рибулозо-1,5- дифосфату присоединяется не СО2, а кислород, в результате происходит расщепление рибулозо-1,5-дифосфата на 3-фосфоглицериновую и фосфогликолевую кислоты:
|
Образовавшаяся фосфогликолевая кислота под действием специфической фосфатазы подвергается гидролизу с образованием неорганического фосфата и гликолевой кислоты:
|
Гликолевая кислота подвергается дальнейшим превращениям в пероксисомах – субклеточных органеллах, функциональная деятельность которых тесно связана с процессами, происходящими в хлоропластах и митахондриях. В пероксисомах гликолевая кислота окисляется с участием фермента гликолатоксидазы и превращается в глиоксиловую кислоту:
|
Продукт данной реакции Н2О2 разлагается под действием каталазы на воду и кислород, а глиоксиловая кислота аминируется от глутаминовой кислоты, превращаясь в аминокислоту глицин:
|
Аминокислота глицин не накапливается в пероксисомах, а транспортируется из пероксисом в митохондрии, где участвует в синтезе аминокислоты серина (рис. …). Эту реакцию катализируют ферменты глициндекарбоксилаза и серинтрансгидрооксиметилаза, имеющая в активном центре в качестве кофермента тетрагидрофолиевую кислоту. В ходе реакции синтеза серина происходит также высвобождение СО2 и NH3, а также образование НАД×Н:
|
Образовавшийся в митахондриях серин может далее транспортироваться в пероксисомы и под действием аминотрансферазы передавать аминогруппу на молекулы пировиноградной кислоты. В результате этой реакции серин превращается в гидроксипировиноградную кислоту, а пировиноградная кислота в аминокислоту аланин:
|
|
Гидроксипировиноградная кислота восстанавливается в глицериновую кислоту с участием дегидрогеназы:
Продукт этой реакции глицериновая кислота может затем в хлоропластах фосфорилироваться и, превращаясь в 3-фосфоглицериновую кислоту, включаться в реакции цикла Кальвина:
|
Таким образом, при взаимодействии пероксисом, хлоропластов и митохондрий в фотосинтезирующих клетках растений осуществляется процесс, связанный с поглощением О2 и высвобождением СО2, который называют фотодыханием. Кислород принимает участие в первой реакции, где он связывается вместо СО2 с молекулами рибулозо-1,5-дифосфата, и при окислении фосфогликолевой кислоты в пероксисомах. Выделение СО2 происходит в митохондриях в ходе синтеза аминокислоты серина.
В связи с тем, что при фотодыхании осуществляются превращения гликолевой кислоты – продукта разложения первичного акцептора СО2, синтезируемого в реакциях цикла Кальвина, за счёт таких превращений уменьшается количество связанной в ходе фотосинтеза СО2, в результате чего понижается урожайность растений. В опытах установлено, что в естественных условиях произрастания при повышенных температурах, снижающих концентрацию СО2 в хлоропластах, продуктивность растений вследствие интенсивного фотодыхания может понижаться на 30-40 %.
Исходя из этих данных, учёными–биохимиками сформулирована важнейшая задача для селекционеров и генетиков по выведению новых сортов сельскохозяйственных культур с пониженной скоростью фотодыхания. Одним из главных направлений такой работы является оптимизация структуры каталитического центра фермента рибулозодифосфаткарбоксилазы, направленная на усиление карбоксилазной и ослабление оксигеназной активности этого фермента. Для решения указанной проблемы большие надежды возлагаются на применение методов генетической и белковой инженерии.