Солидус
Солидус (лат. solidus «твёрдый») — линия на фазовых диаграммах, на которой исчезают последние капли расплава, или температура, при которой плавится самый легкоплавкий компонент. Схожий, но противоположный термин, — ликвидус.
Иными словами, солидус — кривая, которая показывает для каждой температуры состав твёрдой фазы, которая может находиться в равновесии с жидкой.
Ретроградным (от лат. retrogradus «идущий назад») называют солидус, поворачивающий к ординате компонента при понижении температуры. Ретроградное плавление связано с образованием жидкой фазы, резко отличающейся по химическому составу от исходного твёрдого раствора. Ретроградное плавление можно трактовать как процесс выделения из твёрдого раствора легкоплавкого вещества.
В геологии выделяется сухой и мокрый солидус — линия начала плавления породы в безводных и водонасыщенных условиях.
Источники
См. также
Полезное
Смотреть что такое «Солидус» в других словарях:
СОЛИДУС — (от лат. solidus плотный прочный), графическое изображение (линия, поверхность) зависимости температур конца равновесной кристаллизации растворов или сплавов от химического состава … Большой Энциклопедический словарь
солидус — сущ., кол во синонимов: 2 • линия (182) • поверхность (32) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
Солидус — Solidus Солидус. (1) Самая высокая температура, при которой металл или сплав находится полностью в твердом состоянии. (2) В фазовой диаграмме, положение точек линии солидус представляет температуры, при которых соединения с различным химическим… … Словарь металлургических терминов
солидус — (от лат. solidus плотный, прочный), графическое изображение (линия, поверхность) зависимости температуры конца равновесной кристаллизации растворов или сплавов от содержания компонентов. * * * СОЛИДУС СОЛИДУС (от лат. solidus плотный, прочный),… … Энциклопедический словарь
Солидус — [solidus] линия солидуса, поверхность солидуса графическое изображение зависимости температур конца равновесной кристаллизации растворов или сплавов от их состава (Смотри Диаграмма состояния). Температуру солидус определяют методом термического… … Энциклопедический словарь по металлургии
СОЛИДУС — [solidus] линия солидуса, поверхность солидуса – графическое изображение зависимости температуры конца равновесной кристаллизации растворов или сплавов от их состава (см. Диаграмма состояния). Температуру солидуса опредеделяют методом… … Металлургический словарь
солидус — sukietėjimo kreivė statusas T sritis Standartizacija ir metrologija apibrėžtis Būsenos diagramos linija, vaizduojanti pusiausvirosios kristalizacijos temperatūros priklausomybę nuo daugiasandės sistemos sudėties. atitikmenys: angl. solidification … Penkiakalbis aiškinamasis metrologijos terminų žodynas
солидус — solidas statusas T sritis chemija apibrėžtis Būsenų diagramos linija, vaizduojanti pusiausvirosios kristalizacijos temperatūros priklausomybę nuo daugiakomponentės sistemos sudėties. atitikmenys: angl. solidification curve; solidus; solidus line… … Chemijos terminų aiškinamasis žodynas
солидус — sukietėjimo kreivė statusas T sritis fizika atitikmenys: angl. solidification curve; solidus curve; solidus line vok. Solidus, f; Soliduskurve, f; Soliduslinie, f rus. кривая солидуса, f; кривая твёрдой фазы, f; солидус, m pranc. courbe de… … Fizikos terminų žodynas
Солидус — (от лат. solidus плотный, твёрдый) линия солидуса, поверхность солидуса, графическое изображение зависимости температур конца равновесной кристаллизации растворов или сплавов от их состава (см. Двойные системы, Тройные системы) … Большая советская энциклопедия
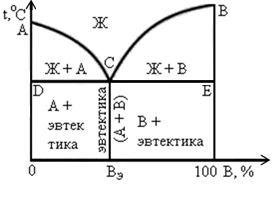
Линия солидус – линия конца кристаллизации



Линия ликвидус – линия начала кристаллизации.
Линия, ограничивающая область полностью кристаллизовавшегося сплава от остальной области на диаграмме состояний, называется линией солидус.
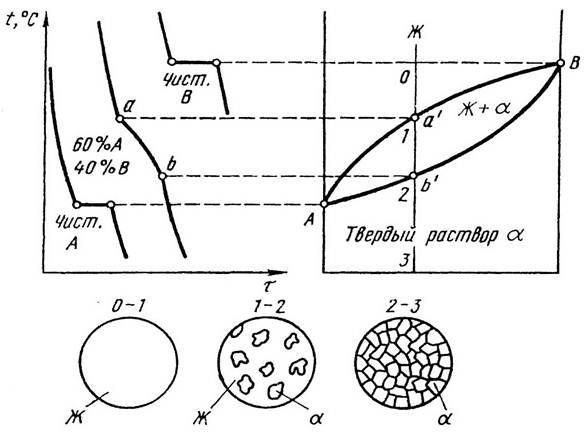
Диаграмма состояния II рода для неограниченных твердых растворов
Примером сплавов с такими диаграммами состояния являются сплавы системы Cu ‑ Ni.
Рис. 6.3. Диаграмма состояния, кривые охлаждения и схемы
структур сплавов с неограниченной растворимостью в твердом состоянии
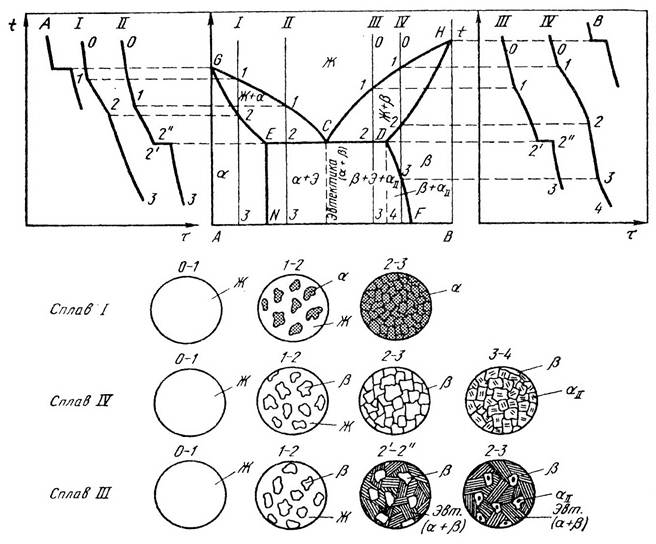
Диаграмма состояния III рода для ограниченных твердых растворов
Этот тип диаграмм очень важен в практическом отношении, так как часто представлен в составе сложных диаграмм широко распространенных промышленных сплавов.
В рассматриваемой системе ограниченная растворимость компонентов в твердом состоянии может быть постоянной и может быть переменной. Оба рассматриваемых случая представлены на рис.6.4 (соответственно линии EN и DF). В итоге имеем диаграмму состояния с двусторонней ограниченной растворимостью компонентов в твердом состоянии.
В такой системе компоненты А и Вне могут при затвердевании образовывать собственных кристаллов, так как они между собой образуют твердые растворы α и βСоответственно в области, лежащей слева от линии EN при кристаллизации из жидкости начинают выделяться кристаллы твердого раствора α. В интервале кристаллизации сплавы имеют двухфазную структуру (Ж + α ). После завершения кристаллизации и вплоть до окончательного охлаждения все эти сплавы имеют структуру однородного твердого раствора α. Аналогичная ситуация имеет место у всех сплавов, расположенных правее точки F, где образуются кристаллы β-твердого раствора.
У сплавов, расположенных в интервале между точкой F и проекцией точки D, первичная кристаллизация в интервале между ликвидусом и солидусом с образованием кристаллов β-твердого раствора. При этом сплавы после завершения кристаллизации вплоть до пересечения с линией DF имеют однородную структуру β-твердого раствора. При дальнейшем же охлаждении этих сплавов (например, сплава IV ниже точки 3) вплоть до полного охлаждения в структуре этих сплавов происходят изменения, связанные с выделением из β-твердого раствора второй фазы αп(например, у сплава IV), причиной появления которой является уменьшение предела растворимости β-твердого раствора при понижении температуры сплава. На это указывает наклонный характер кривой DF. При понижении температуры твердый раствор βстановится пересыщенным компонентом А, и для приведения системы в равновесие из этого твердого раствора β выделяется избыток растворенного компонента А. Но так как в данной системе чистые компоненты не могут существовать как самостоятельные фазы (они должны образовывать твердые растворы), то на базе избыточных кристаллов компонента А образуется сразу же вторичный α-твердый раствор (αп), кристаллы которого и выделяются из β-твердого раствора и располагаются в виде мелкодисперсных включений внутри зерен основной фазы β. Такие избыточные кристаллы, выделяющиеся не из жидкости, а из твердой фазы, обозначаются αII (вторичные кристаллы), а сам процесс выделения новой фазы в твердом состоянии называетсявторичной кристаллизацией.

Рис.6.4. Диаграмма состояния, кривые охлаждения и схемы образования структур сплавов с ограниченной растворимостью в твердом состоянии и с эвтектическим превращением
Все сплавы, расположенные между точками С и Е, называются доэвтектическими. Их кристаллизация будет начинаться с выделения кристаллов α-твердого раствора (например, сплава II в точке 1). В интервале кристаллизации (например, между точками 1 и 2) у этих сплавов будет структура (Ж + α). По линии ЕС в этих сплавах образуется эвтектика (α + β). После окончательного охлаждения Эти сплавы будут иметь структуру α + Эвтектика (α + β).
Все сплавы, расположенные между точками С и D, называются заэвтектическими. Их кристаллизация будет начинаться с выделения кристаллов β-твердого раствора (например, у сплава III в точке 1). В интервале кристаллизации (например, у сплава III между точками 1 и 2) эти сплавы имеют структуру (Ж + β). На линии CD у заэвтектических сплавов будет образовываться эвтектика (α + β).
При дальнейшем охлаждении заэвтектических сплавов в их структуре будут проходить последующие превращения, которых не было в доэвтектических сплавах. Причиной этих превращений является наклонный характер линии DF. Как уже было показано ранее, при наклонном характере кривой растворимости компонента А в компоненте В (линия DF) с понижением температуры предельная растворимость А в В становится меньше того количества А, которое в данный момент присутствует в сплаве. Поэтому из твердого раствора β будет выделяться αп. Следовательно, все заэвтектические сплавы ниже температуры эвтектического превращения (например, сплав III ниже точки 2) будут иметь следующую структуру: β + Эвтектика (α + β) + αп Эта структура содержит три структурных составляющих: β, Э(α + β) и αII.
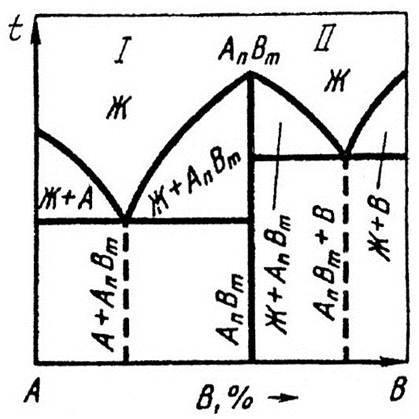
Диаграмма состояния IV рода для химических соединений.
Такая диаграмма изображена на Рис.6.5.
Примером диаграмм этого типа является диаграмма состояния сплавов системы Mg‑Са.
Химическое соединение (например, АnВm) характеризуется определенным соотношением компонентов (например, n% компонента А и m% компонента В). На оси концентрации компонентов (ось абсцисс) химическое соединение обозначает точку, из которой выходит вертикальная линия, фактически разбивающая диаграмму на две простые диаграммы, в которых химическое соединение выступает уже в качестве самостоятельного компонента и, соответственно, образует эвтектики с компонентом А и с компонентом В.
Рис.6.5. Диаграмма состояния с устойчивым химическим соединением
Солидус
ниже которой находится только твердая фаза. Схожий, но противоположный термин, — ликвидус.
Иными словами, солидус — кривая, которая показывает для каждой температуры состав твёрдой фазы, которая может находиться в равновесии с жидкой.
Ретроградным (от лат. retrogradus «идущий назад») называют солидус, поворачивающий к ординате компонента при понижении температуры. Ретроградное плавление связано с образованием жидкой фазы, резко отличающейся по химическому составу от исходного твёрдого раствора. Ретроградное плавление можно трактовать как процесс выделения из твёрдого раствора легкоплавкого вещества.
В геологии выделяется сухой и мокрый солидус — линия начала плавления породы в безводных и водонасыщенных условиях.
Связанные понятия
Углерод — вещество с самым большим числом аллотропических модификаций (более 9 обнаруженных на данный момент).
Диагра́мма фа́зового равнове́сия (диаграмма состоя́ния) желе́зо—углеро́д (иногда эту диаграмму называют «диаграмма железо—цементит») — графическое отображение фазового состояния сплавов железа с углеродом в зависимости от их химического состава и температуры.
30 ГПа), жаропрочностью и стойкостью к действию некоторых кислот (серной и соляной). Однако карбид титана растворим в «царской водке», а также в смесях плавиковой (HF) и азотной (HNO3) кислот и расплавах щелочей. Компонент жаропрочных, жаростойких и твердых сплавов, абразивный материал; его используют для.
Металлические сплавы и диаграммы состояния
Сплавами являются твёрдые вещества, получаемые сплавлением двух или более простых веществ, называемых компонентами. В металлическом сплаве основными компонентами являются металлы. Для металлического сплава меняя соотношение компонентов, можно получить бесчисленное множество вариантов сплава, и каждый вариант будет иметь свою структуру и свойства, температуру плавления, затвердения и т.д.
В технике большинство сплавов получают взаимным растворением их составляющих в жидком состоянии, т.е. доводят компоненты до плавления. Однако сплавы могут быть получены в твёрдом состоянии в процессе смешивания и спекания порошков компонентов под давлением при высоких температурах. Расплавленные компоненты при охлаждении и кристаллизации могут образовывать твердые металлические сплавы с различным строением: смеси, твердые растворы, химические соединения.
Наиболее часто встречающиеся сплавы – твёрдые растворы, в которых компоненты в твердом состоянии частично или полностью растворены друг в друге. Можно просто представить понятие твёрдого раствора можно, если, например, заморозить солёную воду. В этом случае лёд уже будет представлять собой твёрдый раствор соли в воде.
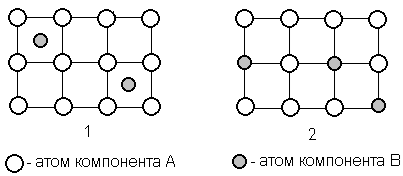
Растворение атомов одного из компонентов в кристаллической решётке другого компонента может идти по типу внедрения, когда атомы растворенного элемента располагаются между атомами растворителя (рисунок 1.1), и по типу замещения, когда атомы растворенного элемента замещают атомы растворителя (рисунок 1.2).
Рисунок 1 – Строение твёрдого раствора внедрения и замещения
При образовании твёрдого раствора внедрения его растворимость всегда ограниченная, что связано с ограниченными размерами межатомных промежутков в кристаллической решётке растворителя.
Чем больше концентрация твёрдого раствора, тем больше увеличены межатомные расстояния в решетке. Такие твёрдые растворы возникают при сплавлении металлов с неметаллами, имеющими малый атомный радиус – углеродом, азотом, бором, водородом. Примером твёрдых растворов внедрения, имеющих промышленное значение, являются твёрдые растворы углерода в ОЦК и ГЦК решётке железа – феррит и аустенит.
Информация о состоянии и структуре сплавов просто и сжато может быть представлена в виде диаграммы состояния – графического изображения состояния сплавов в зависимости от температуры и концентрации компонентов. Такие диаграммы также называют структурными с добавлением слова равновесные, что указывает на образование таких фаз и структур, которые соответствуют наименьшему значению свободной энергии системы.
На любой диаграмме состояния можно выделить следующие точки и линии:
Ликвидус – точка, отвечающая началу кристаллизации.
Линия ликвидус – геометрическое место точек ликвидус.
Солидус – точка, отвечающая концу кристаллизации.
Линия солидус – геометрическое место точек солидус.
Фигуративная точка– точка, взятая в пределах диаграммы состояния, которая показывает температуру сплава, его состояние, процентное соотношение компонентов.
Фигуративная линия – линия, проходящая через фигуративную точку параллельно оси температур.
Рассмотрим основные диаграммы состояния двойных сплавов.
Рисунок 2 – Диаграмма состояния I рода
Диаграмма состояния II рода характерна для сплавов с неограниченной растворимостью компонентов друг в друге, имеющих одинаковые типы кристаллических решеток. Диаграмма (рисунок 3) содержит область жидкой фазы (выше линии ликвидус АСВ), двухфазную область α + Ж, расположенную между линиями АСВ и АDВ, область твердой фазы α (ниже линии солидус АDВ). Фаза α представляет собой твердый раствор компонентов А и В, азерна этой фазы имеют общую кристаллическую решетку.
Рисунок 3 – Диаграмма состояния II рода
Диаграмма состояния III рода характерна для сплавов с ограниченной растворимостью компонентов друг в друге. На диаграмме (рисунок 4) линия АDВ является линией ликвидус, а линия АСDЕВ – линией солидус. Фаза α является твердым раствором компонента В в компоненте А, а фаза β – твердым раствором компонента А в компоненте В. Эвтектика для рассматриваемой диаграммы представляет собой смесь мелкозернистых фаз α и β. Эвтектика кристаллизуется при наименьшей для данной системы температуре, т.е. на линии СЕ.
Линия СF показывает предельную растворимость компонента В в компоненте А, а линия ЕК – предельную растворимость компонента А в компоненте В. Ниже линии СF из α-фазы начинают выделяться атомы компонента В, образуя вторичные кристаллы βIIβ-твер-дого раствора. Аналогично ниже линии ЕК из β-фазы выделяются атомы компонента А, образуя вторичные кристаллы αIIα-твердого раствора. Структура доэвтектических сплавов ниже линии СЕ состоит из первичных зерен α-фазы, эвтектики (α + β) и зерен вторичной βII-фазы. А структура заэвтектических сплавов состоит из первичных зерен β-фазы, эвтектики (α + β) и зерен вторичной αII-фазы.
Рисунок 4 – Диаграмма состояния III рода
Диаграмма состояния IV рода (рисунок 5) относится к сплавам, в которых сплавляемые компоненты образуют устойчивое химическое соединение АтВп. Поэтому в данном случае химическое соединение выступает в роли самостоятельного компонента, способного образовывать сплавы с каждым из исходных компонентов.
Химическое соединение АтВп образует с компонентами А и В сплавы, которые характерны для диаграммы состояния I рода.
Рисунок 5 – Диаграмма состояния IV рода
Рисунок 6 – Изменение твёрдости и электрического сопротивления в зависимости от рода диаграммы
Для сплавов и компонентов, образующих химическое соединение, максимальные значения твердости и электрического сопротивления наблюдаются при концентрации компонентов, соответствующих химическому соединению (рисунок 6,г).
Таким образом, если известны характер взаимодействия между компонентами и тип диаграммы состояния, то возможен выбор состава сплава, обеспечивающего заданные физико-химические свойства.
1. Что такое сплав? Что является компонентами для металлического сплава? Сколько компонентов должно присутствовать, чтобы вещество можно было назвать сплавом?
2. Способы получения сплава.
3. Типы растворения твёрдых растворов. Показать на рисунке. Какой тип растворения способствует увеличению межатомных расстояний.
4. Что такое диаграмма состояния?
5. Ликвидус как точка и как линия (определения).
6. Солидус как точка и как линия (определения).
7. Фигуративная точка, фигуративная линия (определения).
8. Диаграммы состояний I, II, III, IV рода. Для каких сплавов характерна каждая из диаграмм, особенности диаграмм. Уметь показать на каждой из диаграмм ключевые точки и линии (солидус, ликвидус и др.)
9. Диаграммы изменения твёрдости и электрического сопротивления. Уметь изобразить – как изменяются эти свойства для каждого рода диаграмм.
Диаграммы состояния двухкомпонентных сплавов

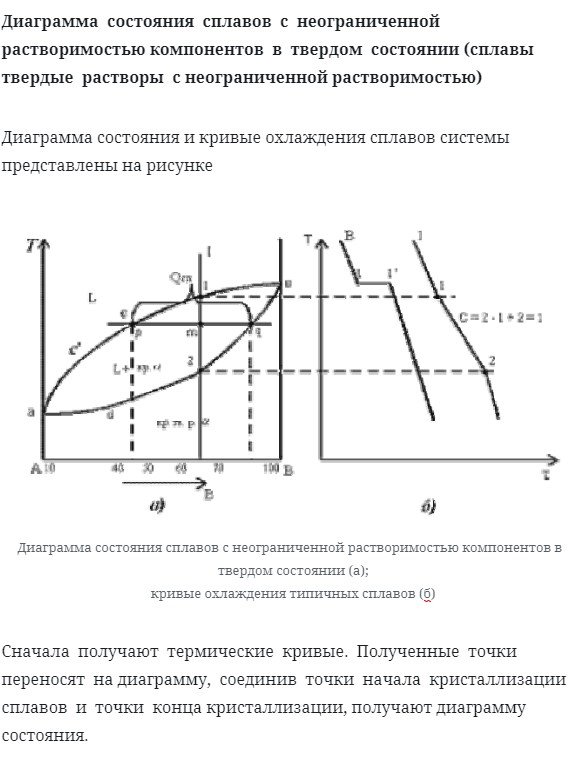



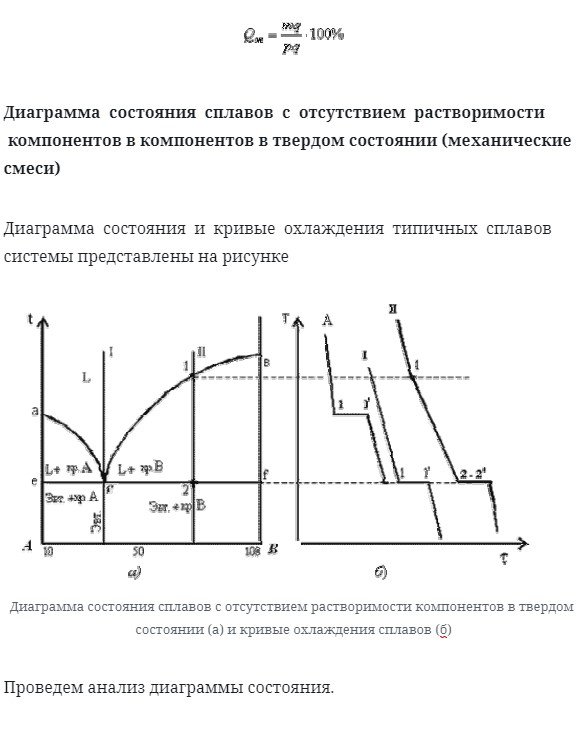



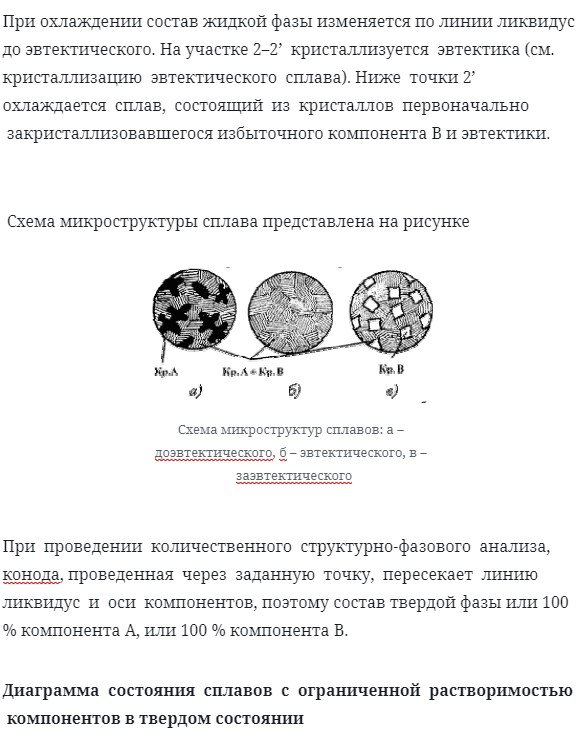

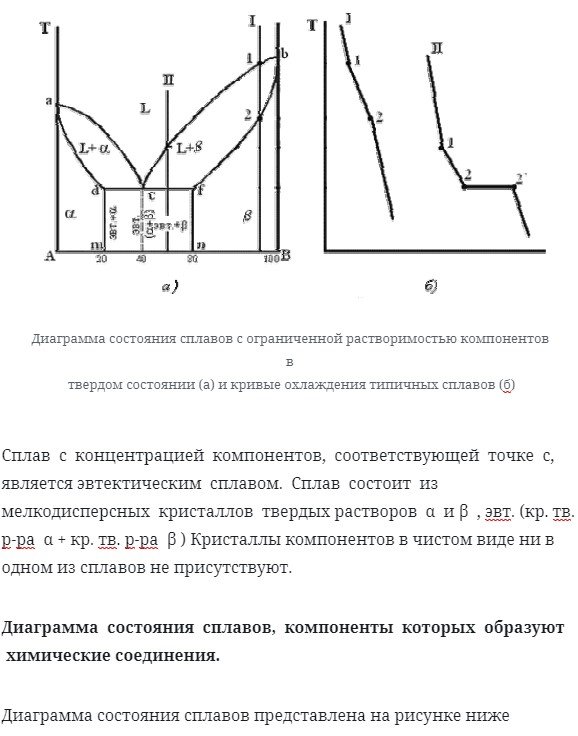
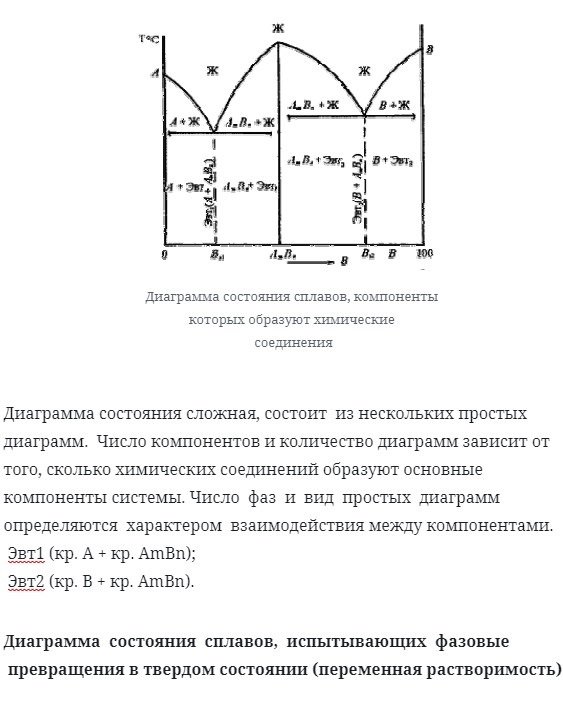

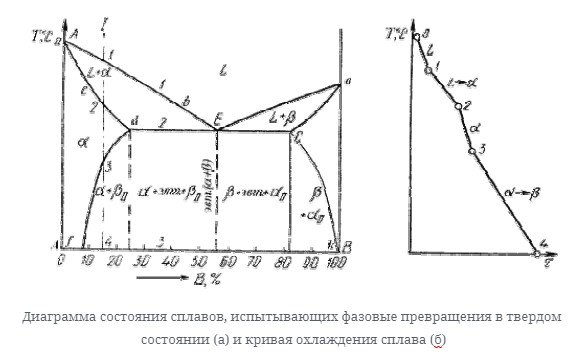

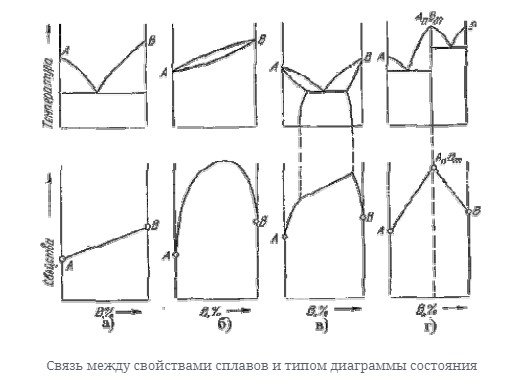

Диаграмма состояния представляет собой графическое представление фазового состояния сплава и его критической точки в зависимости от температуры и концентрации в равновесии.
Фазовая диаграмма служит основой для определения фазового превращения, состава и количества фаз, структурных составляющих сплава, определяющих его механические, физические, химические и технические свойства.
Собственность.
Диаграмма состояния сплавов с неограниченной растворимостью компонентов в твердом состоянии (сплавы твердые растворы с неограниченной растворимостью)
Диаграмма состояния и кривые охлаждения сплавов системы представлены на рисунке
Сначала получается тепловая кривая. Полученная точка переносится на диаграмму и приобретает диаграмму состояния, соединяющую начальную точку кристаллизации сплава и конечную точку кристаллизации.
Давайте проанализируем полученную цифру.
Количество компонентов: k = 2 (компоненты a и b).
Количество фаз: f = 2 (жидкий l, твердый раствор Кристалла)
Основная линия на рисунке: acb-это линия Ликвидуса, а сплав над этой линией-жидкое состояние. АДБ Солидус, и сплав под этой линией в твердом состоянии.
Характеристика сплава системы:
Точка перегиба (критическая точка) регистрируется на кривой охлаждения, что связано с уменьшением скорости охлаждения за счет выделения скрытой теплоты crystallization. In разделы 1-2, процесс кристаллизации продолжается с уменьшением в temperature. In в соответствии с фазовым законом 2-компонентной системы, в присутствии 2-фазы (жидкого и α-твердого раствора кристалла) число степеней свободы равно 1.
При достижении температуры соответствующей точке 2 сплав затвердевает, а при дальнейшем понижении температуры сплав в твердом состоянии охлаждается, состоящий из однородных кристаллов α-твердого раствора.
Количественный структурно-фазовый анализ сплава.
Используя диаграмму состояния, можно определить не только количество фаз, но и их состав и количественное соотношение в сплаве при любой температуре. Для этого используйте правила сегмента. Для количественного структурно-фазового анализа горизонталь (конус) рисуется в заданной точке до пересечения с ближайшей линией на диаграмме (Ликвидус, Солидус или ось компонентов).
Определение фазового состава в точке m:
Чтобы определить его, проведите горизонтальную линию через точку m, пока она не пересечется с Ликвидусом и Солидусом, которые являются ближайшими линиями на диаграмме. Состав жидкой фазы определяется проекцией горизонтального пересечения с линией Ликвидуса р на концентрационную ось.
Состав твердой фазы определяется проекцией горизонтального пересечения с линией Солидуса q (или осью компонента) на ось концентрации. Состав жидкой фазы изменяется вдоль линии Ликвидуса, в то время как состав твердой фазы изменяется вдоль линии Солидуса. При понижении температуры фазовый состав изменяется в сторону уменьшения содержания компонента В.
б) определение количественного соотношения жидкой и твердой фаз при заданной температуре (точка м) :
Количественная масса фазы обратно пропорциональна сегменту коноды. Рассмотрим точку m и конус, проходящий через ее сегмент. Количество всего сплава (qsp) определяется сегментом pq.
Линия, примыкающая к Ликвидусу pm, определяет количество твердой фазы. Сегмент mq, примыкающий к Солидусу (или компонентной оси), определяет количество жидкой фазы.
Диаграмма состояния сплавов с отсутствием растворимости компонентов в компонентов в твердом состоянии (механические смеси)
Диаграмма состояния и кривые охлаждения типичных сплавов системы представлены на рисунке
При образовании сплавов из механических смесей эвтектика состоит из компонентов а и кристаллов в: эвтектика. (возврат каретки. Возврат каретки.)
Эвтектический процесс кристаллизации сплава:к пункту 1, Сплав охлажен в жидкости state. At при температуре, соответствующей точке 1, начинается одновременная кристаллизация 2-х различных компонентов. Кривая температуры отмечена на кривой охлаждения. Процесс протекает при постоянной температуре. Это объясняется тем, что число степеней свободы становится равным нулю по фазовому закону 2-компонентной системы, в которой имеется 3 фазы (жидкости и кристаллы компонентов А и в).
В точке 1 / процесс кристаллизации завершен. Менее 1 балла/
Сплав охлаждается и состоит из неоднородно дисперсных кристаллов компонентов a и b. C) другие сплавы в системе аналогичны сплаву ii. Рисунок 5. 3. См. Кривую охлаждения сплава для процесса кристаллизации b. alloy ii: до пункта 1, Сплав охлажен в жидкости state. At при температуре, соответствующей точке 1, начинает формироваться центр кристаллизации избытка b, а на кривой охлаждения наблюдается точка перегиба (критическая точка), которая связана с уменьшением скорости охлаждения за счет выделения скрытой теплоты crystallization. In разделы 1-2, процесс кристаллизации продолжается с уменьшением в temperature. In в соответствии с фазовым законом 2-компонентной системы, при наличии 2-фазы (жидкой и компонента в-кристалла) число степеней свободы равно 1.
При охлаждении состав жидкой фазы изменяется на эвтектический по линии Ликвидуса. В области 2-2 происходит кристаллизация эвтектики (см. Кристаллизация эвтектического сплава). Ниже пункта 2 сплав, состоящий из кристаллов, сначала охлаждается.
Избыток кристаллизованного компонента В и эвтектики.
Схема микроструктуры сплава представлена на рисунке
При проведении количественного структурно-фазового анализа конноды, проведенные через определенные точки, пересекают линию Ликвидуса и ось компонента, поэтому состав твердой фазы составляет 100% компонента А или 100%компонента В.
Диаграмма состояния сплавов с ограниченной растворимостью компонентов в твердом состоянии
Диаграмма состояния и кривые охлаждения типичных сплавов системы представлены на рисунке ниже
При концентрации компонента, не превышающей предельных значений (сечения am и nâ), сплав кристаллизуется так же, как и сплав, содержащий твердый раствор с неограниченной растворимостью. См. Кривую охлаждения для сплава i на рисунке 1. Если концентрация компонента 5. 5 b превышает предел (в разделе dcf)
Сплав кристаллизуется как сплав в механической смеси. См. Кривую охлаждения сплава ii На рисунке 2. 5. 5 б
Сплав с концентрацией компонентов, соответствующей точке С, является эвтектическим сплавом. Сплав состоит из мелкодисперсных кристаллов твердых растворов α и β. (возврат каретки. Твердый раствор α+Красный твердый раствор β) кристаллов компонента в чистом виде не существует ни в одном сплаве.
Диаграмма состояния сплавов, компоненты которых образуют химические соединения
Диаграмма состояния сплавов представлена на рисунке ниже
Диаграмма состояний является сложной и состоит из нескольких простых диаграмм. Количество компонентов и число фигур зависит от количества соединений, составляющих основные компоненты системы. Количество фаз и внешний вид простого чертежа определяются характером взаимодействия между компонентами.
eut1 (КР. Возврат каретки. Ambn);
eut2 (КР. Б + СГ. Амбн).
Диаграмма состояния сплавов, испытывающих фазовые превращения в твердом состоянии (переменная растворимость)
Диаграмма состояния показана на рисунке.
По внешнему виду этот рисунок напоминает диаграмму состояния сплава, в котором растворимость компонентов в твердом состоянии ограничена. Разница заключается в том, что линия конечной растворимости компонента не перпендикулярна оси концентрации. При понижении температуры появляется область, в которой вторичная фаза осаждается из однородного твердого раствора.
Кривая охлаждения сплава I представлена на рисунке ниже.
Процесс кристаллизации сплава i: до пункта 1, Сплав охлажен в жидкости state. At при температуре, соответствующей точке 1, центр кристаллизации твердого раствора α начинает form. In разделы 1-2, процесс кристаллизации продолжается по мере того как температура уменьшает. Когда вы достигнете
При температуре, соответствующей точке 2, сплав затвердевает, а при дальнейшем понижении температуры сплав охлаждается в твердом состоянии, состоящем из однородных кристаллов твердого раствора α.
При достижении температуры, соответствующей точке 3, оказывается, что твердый раствор α насыщен компонентом в, а при низких температурах растворимость 2-го компонента снижается, поэтому из Альфа-раствора начинают осаждаться избыточные компоненты в виде кристаллов βn. После пункта 3, сплав кристаллы α твердого раствора и
Вторичный Кристалл βn твердого раствора
Связь между свойствами сплавов и типом диаграммы состояния
Вид диаграммы и свойства сплава зависят от соединений или фаз, образующих компоненты сплава, поэтому между ними должна быть определенная связь. Эта зависимость установлена крнаковым на рисунке ниже.
Образовательный сайт для студентов и школьников
Копирование материалов сайта возможно только с указанием активной ссылки «www.lfirmal.com» в качестве источника.
© Фирмаль Людмила Анатольевна — официальный сайт преподавателя математического факультета Дальневосточного государственного физико-технического института