Дистрофии
Дистрофия (от греч. dys – нарушение и trophо – питаю) – это количественные и качественные структурные изменения в клетках и/или межклеточном веществе органов и тканей, обусловленные нарушением обменных процессов. При дистрофиях в результате нарушения трофики в клетках или в межклеточном веществе накапливаются различные продукты обмена (белки, жиры, углеводы, минералы, вода). Морфологическая сущность дистрофий выражается в:
Таким образом, дистрофия является морфологическим выражением нарушений метаболизма клеток и тканей.
Среди механизмов поддержания нормальной трофики выделяют клеточные и внеклеточные.
Клеточные механизмы обеспечиваются структурной организацией клетки и ее ауторегуляцией, обеспечивающейся генетическим кодом.
Внеклеточные механизмы трофики обеспечиваются транспортными (кровь, лимфа) и интегративными (нервная, эндокринная, гуморальная) системами ее регуляции.
Непосредственной причиной развития дистрофий могут служить:
ü Гипогликемия. Низкий уровень глюкозы в крови (гипогликемия) приводит к недостаточному производству молекул аденозинтрифосфата (АТФ), что наиболее выражено в головном мозге.
ü Гипоксия: Недостаток кислорода в клетках (гипоксия) может возникать при:
Морфогенез дистрофий
Среди механизмов, ведущих к развитию характерных для дистрофий изменений, различают инфильтрацию, декомпозицию (фанероз), извращенный синтез и трансформацию.
Инфильтрация – избыточное проникновение продуктов обмена из крови и лимфы в клетки или межклеточное вещество и/или нарушение включения их в метаболизм с последующим накоплением. Например, инфильтрация белком эпителия проксимальных канальцев почек при нефротическом синдроме, инфильтрация липопротеидами интимы аорты и крупных артерий при атеросклерозе.
Декомпозиция (фанероз) – распад сложных в химическом отношении веществ. Например, распад липопротеидных комплексов и накопление в клетке жира в свободном состоянии (жировая дистрофия кардиомиоцитов при дифтерийной интоксикации). Распад полисахаридно-белковых комплексов лежит в основе фибриноидных изменений соединительной ткани при ревматических болезнях.
Трансформация – переход одного вещества в другое. Такова, например, трансформация углеводов в жиры при сахарном диабете, усиленная полимеризация глюкозы в гликоген и др.
Извращенный синтез – это синтез в клетках или в тканях веществ, не встречающихся в них в норме. К ним относятся: синтез аномального белка амилоида в клетке и образование аномальных белково-полисахаридных комплексов амилоида в межклеточном веществе, синтез белка алкогольного гиалина гепатоцитом, синтез гликогена в эпителии узкого сегмента нефрона при сахарном диабете.
Классификация.
В зависимости от локализации нарушений обмена:
По преобладанию нарушений того или иного вида обмена:
В зависимости от влияния генетических факторов:
По распространенности процесса:
ПАРЕНХИМАТОЗНЫЕ ДИСТРОФИИ
К паренхиматозным белковым дистрофиям со времен Р.Вирхова многие патологи причисляли и продолжают причислять так называемую «зернистую дистрофию», которую сам Р.Вирхов обозначил как «мутное набухание». Так принято обозначать процесс, при котором в цитоплазме клеток паренхиматозных органов появляется выраженная зернистость. Органы увеличиваются в размерах, становятся дряблыми и тусклыми на разрезе, как бы ошпаренные кипятком. Электронно-микроскопическое и гистоферментохимическое изучение «зернистой дистрофии» показало, что в ее основе лежит не накопление белка в цитоплазме, а гиперплазия (т.е. увеличение количества) ультраструктур клеток паренхиматозных органов как выражение функционального напряжения этих органов в ответ на различные воздействия.
ПАРЕНХИМАТОЗНЫЕ БЕЛКОВЫЕ ДИСТРОФИИ
В настоящее время к паренхиматозным белковым дистрофиям (диспротеинозам) относят гиалиново-капельную, гидропическую и роговую. Однако, следует подчеркнуть, что роговая дистрофия по механизму своего развития не связана с предыдущими.
Гиалиново-капельная дистрофия
При гиалиново-капельной дистрофии в цитоплазме появляются крупные гиалиноподобные белковые глыбки и капли, сливающиеся между собой и заполняющие тело клетки. В основе этой дистрофии лежит коагуляция белков цитоплазмы с выраженной деструкцией ультраструктурных элементов клетки – фокальный коагуляционный некроз.
Этот вид диспротеиноза часто встречается в почках, реже – в печени, и совсем редко – в миокарде.
Внешний вид органов при этой дистрофии не имеет каких-либо характерных черт. Макроскопические изменения характерны для тех заболеваний, при которых встречается гиалиново-капельная дистрофия.
В почках при микроскопическом исследовании накопление крупных зерен белка ярко-розового цвета – гиалиновых капель – находят в нефроцитах. При этом наблюдается деструкция митохондрий, эндоплазматической сети, щеточной каемки. В основе гиалиново-капельной дистрофии нефроцитов лежит недостаточность вакуолярно-лизосомного аппарата эпителия проксимальных и дистальных извитых канальцев, в норме реабсорбирующего белки. Поэтому этот вид дистрофии нефроцитов очень часто встречается при нефротическом синдроме и отражает реабсорбционную недостаточность извитых канальцев в отношении белков. Этот синдром является одним из проявлений многих заболевании почек, при которых первично поражается гломерулярный фильтр (гломерулонефрит, амилоидоз почек, парапротеинемическая нефропатия и др.)
В печени при микроскопическом исследовании в гепатоцитах находят глыбки и капли белковой природы – это алкогольный гиалин, представляющий собой на ультраструктурном уровне нерегулярные агрегаты микрофибрилл и гиалиновые неправильной формы включения (тельца Маллори). Образование этого белка и телец Маллори служит проявлением извращенной белково-синтетической функции гепатоцита и выявляется постоянно при алкогольном гепатите.
Исход гиалиново-капельной дистрофии неблагоприятен: она завершается необратимым процессом, ведущим к тотальному коагуляционному некрозу клетки.
Функциональное значение этой дистрофии очень велико – происходит резкое снижение функции органа. С гиалиново-капельной дистрофией эпителия почечных канальцев связаны появление в моче белка (протеинурия) и цилиндров (цилиндрурия), потеря белков плазмы (гипопротеинемия), нарушение ее электролитного баланса. Гиалиново-капельная дистрофия гепатоцитов нередко является морфологической основой нарушений многих функций печени.
Гидропическая дистрофия
Характеризуется появлением в клетке вакуолей, наполненных цитоплазматической жидкостью. Жидкость накапливается в цистернах эндоплазматического ретикулума и в митохондриях, реже в ядре клетки. Механизм развития гидропической дистрофии сложен и отражает нарушения водно-электролитного и белкового обмена, ведущие к изменению коллоидно-осмотического давления в клетке. Большую роль играет нарушение проницаемости мембран клетки, сопровождающееся их распадом. Это ведет к активации гидролитических ферментов лизосом, которые разрывают внутримолекулярные связи с присоединением воды. По существу такие изменения клетки являются выражением фокального колликвационного некроза.
Гидропическая дистрофия наблюдается в эпителии кожи и почечных канальцев, в гепатоцитах, мышечных и нервных клетках, а также в клетках коры надпочечников.
Причины развития гидропической дистрофии в разных органах неоднозначны. В почках – это повреждение гломерулярного фильтра (гломерулонефрит, амилоидоз, сахарный диабет), что ведет к гиперфильтрации и недостаточности ферментной системы нефроцитов, в норме обеспечивающей реабсорбцию воды; отравление гликолями, гипокалиемия. В печени гидропическая дистрофия возникает при вирусном и токсическом гепатитах. Причинами гидропической дистрофия эпидермиса могут быть инфекции, аллергии.
Внешний вид органов и тканей мало изменяется при гидропической дистрофии.
Микроскопическая картина: паренхиматозные клетки увеличены в объеме, цитоплазма их заполнена вакуолями, содержащими прозрачную жидкость. Ядро смещается на периферию, иногда вакуолизируется или сморщивается. Нарастание гидропии приводит к распаду ультраструктур клетки и переполнению клетки водой, появлению заполненных жидкостью баллонов, поэтому такие изменения называют баллонной дистрофией.
Исход гидропической дистрофии, как правило, неблагоприятный; она завершается тотальным колликвационным некрозом клетки. Поэтому функция органов и тканей при гидропической дистрофии резко снижена.
Роговая дистрофия
Роговая дистрофия, или патологическое ороговение, характеризуется избыточным образованием рогового вещества в ороговевающем эпителии (гиперкератоз, ихтиоз) или образованием рогового вещества там, где в норме его не бывает – патологическое ороговение на слизистых оболочках, например, в полости рта (лейкоплакия), пищеводе, шейке матки. Роговая дистрофия может быть местной или общей, врожденной или приобретенной.
Причины роговой дистрофии разнообразны: хроническое воспаление, связанное с инфекционными агентами, действием физических и химических факторов, авитаминозы, врожденное нарушение развития кожи и др.
Исход может быть двояким: устранение вызывающей причины в начале процесса может привести к восстановлению ткани, однако в далеко зашедших случаях наступает гибель клеток.
Значение роговой дистрофии определяется ее степенью, распространенностью и длительностью. Длительно существующее патологическое ороговение слизистой оболочки (лейкоплакия) может явиться источником развития раковой опухоли. Врожденный ихтиоз резкой степени, как правило, несовместим с жизнью.
ПАРЕНХИМАТОЗНЫЕ ЖИРОВЫЕ ДИСТРОФИИ (ЛИПИДОЗЫ)
Паренхиматозная жировая дистрофия – это структурные проявления нарушения обмена цитоплазматических липидов, которые могут выражаться в накоплении жира в свободном состоянии в клетках, где он не обнаруживаются и в норме.
Причины жировой дистрофии разнообразны:
Паренхиматозная жировая дистрофия характеризуется, главным образом, накоплением триглицеридов в цитоплазме паренхиматозных клеток. При нарушении связи белков с липидами – декомпозиции, которая возникает под действием инфекций, интоксикаций, продуктов перекисного окисления липидов – возникает деструкция мембранных структур клетки и в цитоплазме появляются свободные липоиды, являющиеся морфологическим субстратом паренхиматозной жировой дистрофии. Наиболее часто она наблюдается в печени, реже в почке и миокарде, и расценивается как неспецифический ответ на большое количество типов повреждения.
Микроскопические признаки жировой дистрофии: любой жир, находящийся в тканях, растворяется в растворителях, которые используются при окраске образцов ткани для микроскопического исследования. Поэтому при обычной проводке и окраске ткани (окраска гематоксилином и эозином) клетки в самых ранних стадиях жировой дистрофии имеют бледную и пенистую цитоплазму. По мере увеличения жировых включений в цитоплазме появляются небольшие вакуоли.
Специфическая окраска на жиры требует использования замороженных срезов, сделанных из свежей ткани. В замороженных срезах жир остается в цитоплазме, после чего срезы окрашиваются специальными красителями. Гистохимически жиры выявляются с помощью ряда методов: судан IV, жировой красный О и шарлах рот окрашивают их в красный цвет, судан Ш – в оранжевый, судан черный B и осмиевая кислота – в черный, сульфат нильского голубого окрашивает жирные кислоты в темно-синий цвет, а нейтральные жиры – в красный. С помощью поляризационного микроскопа можно дифференцировать изотропные и анизотропные липиды. Анизотропные липиды, такие как холестерин и его эфиры, дают характерное двойное лучепреломление.
Жировая дистрофия печени проявляется резким увеличением содержания и изменением состава жиров в гепатоцитах. В клетках печени вначале появляются гранулы липидов (пылевидное ожирение), затем мелкие капли их (мелкокапельное ожирение), которые в дальнейшем сливаются в крупные капли (крупнокапельное ожирение) или в одну жировую вакуоль, которая заполняет всю цитоплазму и отодвигает ядро на периферию. Измененные таким образом печеночные клетки напоминают жировые. Чаще отложение жиров в печени начинается на периферии, реже – в центре долек; при значительно выраженной дистрофии ожирение клеток печени имеет диффузный характер.
Макроскопически печень при жировой дистрофии увеличена, малокровна, тестоватой консистенции, имеет желтый или охряно-желтый цвет, с жирным блеском на разрезе. При разрезе на лезвии ножа и поверхности разреза виден налет жира.
Типы жировой дистрофии печени:
Острая жировая дистрофия печени – редкое, но серьезное состояние, связанное с острым поражением печени. При острой жировой дистрофии печени триглицериды накапливаются в цитоплазме как маленькие, ограниченные мембраной вакуоли (мелкокапельная жировая дистрофия печени).
Хроническая жировая дистрофия печени может возникать при хроническом алкоголизме, недоедании и при отравлении некоторыми гепатотоксинами. Жировые капли в цитоплазме соединяются, формируя большие вакуоли (крупнокапельная жировая дистрофия печени). Локализация жировых изменений в дольке печени зависит от причин, которые их обусловили. Даже при тяжелой хронической жировой печени редко имеются клинические проявления дисфункции печени.
Жировая дистрофия миокарда характеризуется накоплением триглицеридов в миокарде.
Причины жировой дистрофии миокарда:
хронические гипоксические состояния, особенно при выраженной анемии. При хронической жировой дистрофии желтые полосы чередуются с красно-коричневыми участками («тигровое сердце»). Клинические признаки обычно не сильно выражены.
токсическое поражение, например дифтеритический миокардит, вызывает острую жировую дистрофию. Макроскопически сердце дряблое, имеется желтое диффузное окрашивание, сердце выглядит увеличенным в объеме, камеры его растянуты; в клинической картине появляются признаки острой сердечной недостаточности.
Жировая дистрофия миокарда рассматривается как морфологический эквивалент его декомпенсации. Большинство митохондрий при этом распадается, поперечная исчерченность волокон исчезает. Развитие жировой дистрофии миокарда чаще всего связывают не с разрушением комплексов клеточных мембран, а с деструкцией митохондрий, что ведет к нарушению окисления жирных кислот в клетке. В миокарде жировая дистрофия характеризуется появлением в мышечных клетках мельчайших жировых капель (пылевидное ожирение). При нарастании изменений эти капли (мелкокапельное ожирение) полностью замещают цитоплазму. Процесс имеет очаговый характер и наблюдается в группах мышечных клеток, расположенных по ходу венозного колена капилляров и мелких вен, чаще субэндо- и субэпикардиально.
В почках при жировой дистрофии жиры появляются в эпителии проксимальных и дистальных канальцев. Обычно это нейтральные жиры, фосфолипиды или холестерин, который обнаруживают не только в эпителии канальцев, но и в строме. Нейтральные жиры в эпителии узкого сегмента и собирательных трубок встречаются как физиологическое явление.
Внешний вид почек: они увеличены, дряблые (при сочетании с амилоидозом плотные), корковое вещество набухшее, серое с желтым крапом, заметным на поверхности и разрезе.
Механизм развития жировой дистрофии почек связан с инфильтрацией эпителия почечных канальцев жиром при липемии и гиперхолестеринемии (нефротический синдром), что ведет к гибели нефроцитов.
Исход жировой дистрофии зависит от ее степени. Если она не сопровождается грубым поломом клеточных структур, то, как правило, оказывается обратимой. Глубокое нарушение обмена клеточных липидов в большинстве случаев заканчивается гибелью клетки.
Функциональное значение жировой дистрофии велико: функционирование органов при этом резко нарушается, а в ряде случаев и прекращается. Некоторые авторы высказывали мысль о появлении жира в клетках в период реконвалесценции и начала репарации. Это согласуется с биохимическими представлениями о роли пентозофосфатного пути утилизации глюкозы в анаболических процессах, что сопровождается также синтезом жиров.
ПАРЕНХИМАТОЗНЫЕ УГЛЕВОДНЫЕ ДИСТРОФИИ
Углеводы, которые определяются в клетках и тканях и могут быть идентифицированы гистохимически, делят на полисахариды, из которых в животных тканях выявляются лишь гликоген, гликозаминогликаны (мукополисахариды) и гликопротеиды. Среди гликозаминогликанов различают нейтральные, прочно связанные с белками, и кислые, к которым относятся гиалуроновая, хондроитинсерная кислоты и гепарин. Кислые гликозаминогликаны как биополимеры способны вступать в непрочные соединения с рядом метаболитов и осуществлять их транспорт. Главными представителями гликопротеидов являются муцины и мукоиды. Муцины составляют основу слизи, продуцируемой эпителием слизистых оболочек и железами, мукоиды входят в состав многих тканей.
Гистохимические методы выявления углеводов. Полисахариды, гликозаминогликаны и гликопротеиды выявляются ШИК-реакцией. Сущность реакции заключается в том, что после окисления йодной кислотой (или реакции с перйодатом калия) образующиеся альдегиды дают с фуксином Шиффа красное окрашивание. Для выявления гликогена ШИК-реакцию дополняют ферментативным контролем – обработкой срезов амилазой. Гликоген окрашивается кармином Беста в красный цвет. Гликозаминогликаны и гликопротеиды определяют с помощью ряда методов, из которых наиболее часто применяют окраски толуидиновым синим или метиленовым синим. Эти окраски позволяют выявлять хромотропные вещества, дающие реакцию метахромазии. Обработка срезов ткани гиалуронидазой (бактериальной, тестикулярной) с последующей окраской теми же красителями позволяет дифференцировать различные гликозаминогликаны; это возможно также при изменении рН красителя.
Паренхиматозная углеводная дистрофия может быть связана с нарушением обмена гликогена или гликопротеидов.
Нарушение обмена гликогена
Нарушения содержания гликогена проявляются в уменьшении или увеличении количества его в тканях и появлении там, где он обычно не выявляется. Эти нарушения наиболее ярко выражены при сахарном диабете и при наследственных углеводных дистрофиях – гликогенозах.
При сахарном диабете, развитие которого связывают с патологией β-клеток островков поджелудочной железы, что обусловливает недостаточную выработку инсулина, происходит недостаточное использование глюкозы тканями, увеличение ее содержания в крови (гипергликемия) и выведение с мочой (глюкозурия). Тканевые запасы гликогена резко уменьшаются. Это в первую очередь касается печени, в которой нарушается синтез гликогена, что ведет к инфильтрации ее жирами – развивается жировая дистрофия печени; при этом в ядрах гепатоцитов появляются включения гликогена, они становятся светлыми («пустые» ядра).
С глюкозурией связаны характерные изменения почек при диабете. Они выражаются в гликогенной инфильтрации эпителия канальцев, главным образом узкого и дистального сегментов. Эпителий становится высоким, со светлой пенистой цитоплазмой; зерна гликогена видны и в просвете канальцев. Эти изменения отражают состояние синтеза гликогена (полимеризация глюкозы) в канальцевом эпителии при резорбции богатого глюкозой ультрафильтрата плазмы.
При диабете страдают не только почечные канальцы, но и клубочки, их капиллярные петли, базальная мембрана которых становится проницаемой для сахаров и белков плазмы. Возникает одно из проявлений диабетической микроангиопатии – интеркапиллярный (диабетический) гломерулосклероз.
Морфологическая диагностика гликогеноза того или иного типа возможна при исследовании биопсии с помощью гистоферментных методов, а также с учетом локализации накапливаемого гликогена.
Углеводные дистрофии, связанные с нарушением обмена гликопротеидов
При нарушении обмена гликопротеидов в клетках или в межклеточном веществе происходит накопление муцинов и мукоидов, называемых также слизистыми или слизеподобными веществами. В связи с этим при нарушении обмена гликопротеидов говорят о слизистой дистрофии.
Микроскопическое исследование. Оно позволяет выявить не только усиленное слизеобразование, но и изменения физико-химических свойств слизи. Многие секретирующие клетки погибают и десквамируются, выводные протоки желез обтурируются слизью, что ведет к развитию кист. Нередко в этих случаях присоединяется воспаление. Слизь может закрывать просветы бронхов, следствием чего является возникновение ателектазов и очагов пневмонии.
Иногда в железистых структурах накапливается не истинная слизь, а слизеподобные вещества (псевдомуцины). Эти вещества могут уплотняться и принимать характер коллоида. Тогда говорят о коллоидной дистрофии, которая наблюдается, например, при коллоидном зобе.
Причины слизистой дистрофии разнообразны, но чаще всего это воспаление слизистых оболочек в результате действия различных патогенных раздражителей (катаральное воспаление).
Слизистая дистрофия лежит в основе наследственного системного заболевания, называемого муковисцидозом, для которого характерно изменение качества слизи, выделяемой эпителием слизистых желез: слизь становится густой и вязкой, она плохо выводится, что обусловливает развитие ретенционных кист и склероза (кистозный фиброз). Поражаются экзокринный аппарат поджелудочной железы, железы бронхиального дерева, пищеварительного и мочевого тракта, желчных путей, потовые и слезные железы.
Исход в значительной мере определяется степенью и длительностью избыточного слизеобразования. В одних случаях регенерация эпителия приводит к полному восстановлению слизистой оболочки, в других – она атрофируется, в дальнейшем склерозируется, что, естественно, отражается на функции органа.
Что такое гидропическая дистрофия
Функциональное проявление заключается в нарушении морфофункционального состояния органов (при ослаблении сердечной деятельности при белковой дистрофии миокарда). После устранения причины клеточный метаболизм обычно нормализуется, в результате чего поврежденные органы восстанавливаются. Если же причинный фактор продолжает действовать, дистрофические изменения усиливаются и могут быть необратимыми, т.е. закончиться омертвением или некрозом тканевых и клеточных элементов.
Этиология дистрофий. Причиной дистрофии могут быть самые разнообразные факторы:
Патогенез. Механизм или патогенез дистрофий сложный и не всегда одинаковый. Развитие морфологических изменений в органах и тканях может быть связано:
Классификация дистрофий окончательно еще не разработана. В настоящее время рациональным считают классифицировать дистрофии по виду нарушения обмена веществ. Исходя из этого принципа дистрофии подразделяют на белковые, жировые, углеводные, минеральные. Нарушение белкового обмена называют диспротеинозами. Различают клеточные диспротеинозы, внеклеточные и смешанные.
Клеточные диспротеинозы
1.1. Зернистая дистрофия
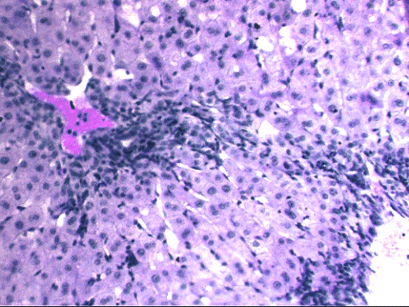
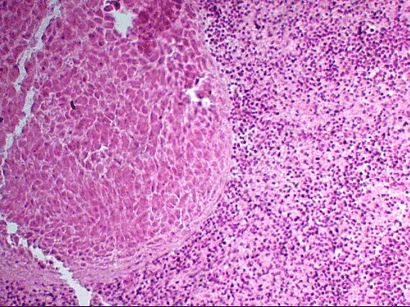
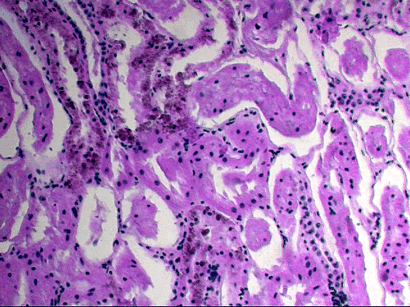
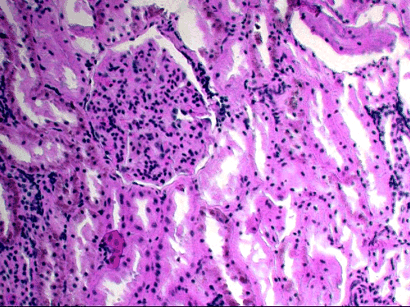
Зернистая дистрофия, или мутное набухание печени, вид белковой дистофии, характеризующийся появлением в цитоплазме клеток зерен и капель белковой природы. В этот дистрофический процесс вовлекаются паренхиматозные органы (печень(рис.1, 1а), почки (рис.2), миокард), реже скелетные мышцы. Этот вид дистрофии наиболее часто развивается при острых инфекционных и септических заболеваниях с/х животных. Таких как сибирская язва, пастереллез, рожа, свиней, колибактериоз и др. при вирусных заболеваниях (чума свиней, птиц, ящур, ЗКГ и др.).
Рис.1. Зернистая дистрофия печени.
Микроскопические признаки зернистой дистофии характеризуются набуханием (увеличением клеток и зерностостью цитоплазмы, уменьшаются просветы внутридольковых синусоидных капилляров; цитоплазма печеночных клеток становится мутной, богатой гранулами или каплями, белковая природа которых определяется гистохимичечкими методами.
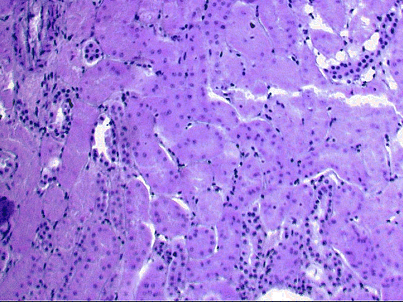
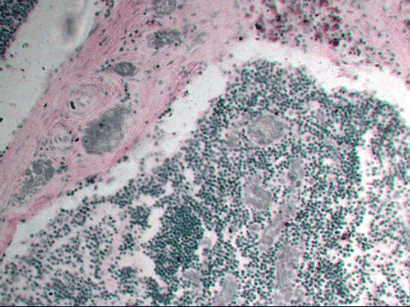
Рис.2. Зернистая дистрофия печени.
Макроскопически органы при зернистой дистрофии набухшие, дряблой консистентности, окрашены бледнее, чем в норме. На разрезе паренхима выбухает за капсулу, поверхность разреза тусклая, суховатая. Сердечная скеленая мышца напоминает ошпаренное кипятком мясо, а печень и почки серовато-бурый цвет.
Дифференциальный диагноз. При посмертной тусклости (бледности) при разрезе паренхима не выбухает за капсулу, т.е. не происходит его увеличения.
Исход зернистой дистрофии.
Зернистая дистрофия печени сопровождается функциональной недостаточностью органа. При устранении причин, вызывающих зернистую дистрофию, возможно возврат к исходному состоянию, т.е. она является обратимым процессом. При далеко зашедших процессах развивается некроз тканей.
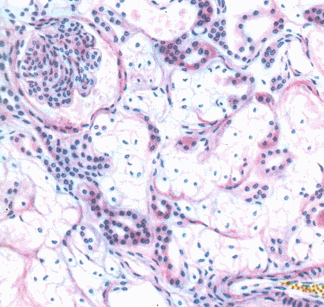
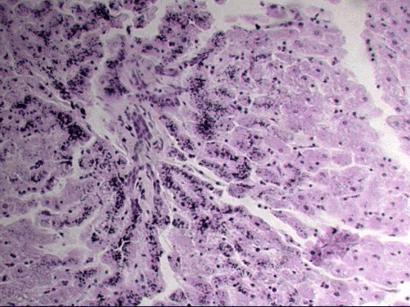
Рис.3. Зернистая дистрофия почки.
Значение для организма.
1.2. Водяночная
(гидропическая дистрофия)
Этот вид белковой дистрофии проявляется образованием в цитоплазме клеток вакуолей различной величины, содержащих прозрачную жидкость.
Мироскопически ганглиозные клетки увеличины, содержат мелкую, пылевидную, частично растворенную нисслевскую зернистость, с образованием светлых, оптических пустых пространств в нейроплазме и вокруг ядра. Частичный хроматолиз ведет к появлению разного размера и локализации вакуолей, содержащих прозрачную жидкость; возможны полное растворение, гибель клеток (кариоцитолиз). Необходимо учитывать, что сходную картину дают жировая дистрофия, когда образцы органов обрабатывают спиртом, а также гликоген из органов, обработанных в водных растворах фиксаторов(рис.3).
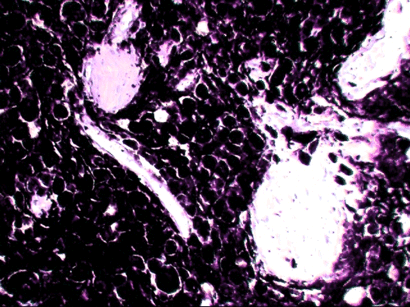
Рис.4. Гидропическая дистрофия.
Макроскопически органы при слабых формах поражения не имеют характерной картины. Как правило, этот вид дистрофии наблюдается при серозном воспалении (чаще эпидермиса кожи), связанным с таким заболеванием как ящур крупного рогатого скота, оспа млекопитающих животных, лучевая болезнь и др.
В дифференциально – диагностическом плане необходимо водяночную дистрофию отличать от жировой. При окраске на жир суданом III жировые капли окрашиваются в оранжево-красный цвет, окрашивание вакуолей с жидкостью не происходит.
Функция органов резко снижена. В ранней стадии процесса восстановление клеток возможно, но чаще клетки подвергнувшиеся водяночной дистрофии некротизируются. Процесс необратимый.
1.3. Роговая дистрофия
Роговая дистрофия (патологическое ороговевание, гиперкератоз кожи) – образование в клетках эпидермиса или эпителия кужанного типа рогового вещества (кератина). В норме процессы ороговевания наблюдаются в эпидермисе. В патологических условиях может быть избыточное образование рога (гиперкератоз) и качественное нарушение рогообразования (паракератоз). Ороговение может быть и в слизистых оболочках (лейкоплакия). Возникает как нарушение обмена веществ в коже при механических, физико-химических и биологических воздействиях на орган, а также в связи с витаминной, минеральной или белковой недостаточностью.
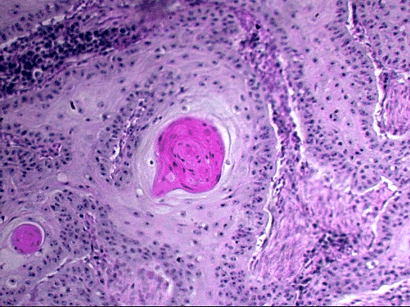
Мироскопически отмечают неравномерное утолщение эпидермиса при гиперплазии клеток мальпигиевого слоя и утолщение рогового слоя в результате избыточного накопления в клетках рогового вещества, или кератина.При гиповитаминозе А возможна метаплазия железистого эпителия в ороговевающий (рис.4).
Рис.5. Роговая дистрофия.
Примерами гиперкератоза могут быть сухие мозоли, ихтиоз (рыбья кожа), рак канкроид (твердый рак).
Паракератоз выражается в утрате способности клеток эпидермиса вырабатывать кератогиалин. При этом состоянии роговой слой утолщен, рыхлый на поверхности кожи образуются чешуйки.
Гиалиново-капельная дистрофия. Этот вид дистрофии наблюдается при хронических пиэлонефритах и характеризуется отложением в извитых, прямых канальцах, а также в клубочках почек гиалинового вещества.
Целевая установка темы:
Изучить морфологическую характеристику (макро- и микрокартину клеточных диспротеинозов). Зернистая дистрофия. Гиалиново – капельная. Водяночная (гидропическая). Роговая. При каких инфекциях наиболее часто встречаются эти виды диспротеинозов. Примеры. Исходы.
Основное внимание уделяется следующим вопросам:
Внеклеточные диспротеинозы
К внеклеточным диспротеинозам относят патологический процесс, характеризующийся отложением между клетками соединительной ткани белковых веществ. К внеклеточным диспротеинозам относят гиалиноз и амилоидоз.
2.1. Амилоидоз
Амилоидная дистрофия характеризуется отложением в ткани гомогенного бесцветного плотного вещества, называемого амилоидом, то есть крахмалоподобным. Это название амилоид получил благодаря способности окрашиваться так же, как и крахмал, в синий цвет при обработке его йодом и серной кислотой, хотя он не имеет ничего общего с крахмалом.
По химической природе амилоид представляет собой белок (амилоидпротеид, близкий к глобулинам), находящийся в соединении с другими, недостаточно еще изученными химическими веществами. Установлено, что химический состав амилоида не всегда одинаков, чем объясняется неодинаковые его физические свойства.
Амилоидная дистрофия бывает общего и местного характера.
Общий амилоидоз проявляется отложением амилоидного вещества сразу во многих органах. Амилоид откладывается под аргирофильной мембраной мелких кровеносных сосудов, по ходу ретикулярных волокон и под базальной мембраной эпителиального покрова желез. При общем амилоидозе чаще поражается печень, селезенка, почки, надпочечники и др. органы.
При амилоидозе орган увеличивается в объеме, бледнее окрашен, плотной консистенции, у лошадей дряблой, поверхность разреза, особенно при сильной степени амилоидоза, восковидная, сухая.
В селезенке наблюдается отложение гомогенного бесструктурного вещества вокруг фолликулов селезенки и по ходу ретикулярных волокон; в печени между эндотелием капилляров и печеночными клетками; в почках под базальной мембраной эндотелия извитых канальцев или под аргирофильной мембраной эндотелия сосудистых клубочков и др. (рис.5).
Рис.6. Амилоидная дистрофия селезенки (саговая форма).
Характеризуется отложением амилоида на ограниченном участке в соединительную ткань или в стенку кровеносного сосуда.
Этиология амилоидоза связана с различными заболеваниями, сопровождающимися нагноениями и некрозами тканей (абсцесс, актиномикоз, туберкулез и др.). Избыток белкового питания может привести к амилоидозу органов. Например, при откорме уток и гусей. Как правило, амилоидная дистрофия встречается у лошадей – продуцентов иммунных сывороток на биофабриках. Патогенез окончательно не выяснен.
Как правило, амилоидоз необратимый процесс. Клетки органов и тканей при амилоидозе атрофируются и подвергаются некрозу. Часто наблюдается разрыв органа с последующим кровоизлиянием в брюшную полость, что часто наблюдается у лошадей продуцентом сыворотки на биофабриках.
Значение для организма.
Клиническое значение имеет лишь общий амилоидоз, приводя к потере функциональной деятельности органа. Местный не оказывает влияния на функцию органа.
2.2. Гиалиноз
Рис.7. Гиалиноз соединительной ткани капсулы.
Макрокартина. Органы и ткани подвергаются гиалинозу плотные сходны по внешнему виду с гиалиновым хрящем.
Исход. Как правило процесс необратим.
Клиническое значение. Если поражаются сосуды в органах ослабляется функция и процесс может закончится разрывом сосудов. Если местного характера гиалиноз, то как правило клинического значения не имеет.
Смешанные диспротеинозы
3.1. Нарушение обмена нуклеопротеидов
Конечным продуктом обмена нуклеопротеидов является мочевая кислота и ее соли. В нормальных условиях эти продукты находятся в растворенном состоянии и выделяются почками. При нарушении обмена нуклеопротеидов происходит избыточное образование мочевой кислоты и ее соли откладываются в тканях, что наблюдается при мочекислом диатезе и мочекислом инфаркте почек.
Характеризуется отложением у млекопитающих животных мочекислых солей в различные ткани и органы. Обычно отложение солей происходит в суставные поверхности пальцев, сухожилия, в хрящ ушной раковины, почки и на серозные покровы. На месте отложения развиваются некрозы с последующим развитием вокруг них воспаления и в итоге разростом соединительной ткани.
У птиц отложение мочекислых солей происходит в виде густой беловатой массы на серозных покровах грудо-брюшной полости, на перикарде, эпикарде, в почках, в суставных поверхностях пальцев ног. Собаки болеют реже чем птицы. У птиц почки увеличены в объеме, усеяны беловатым налетом, на разрезе видны беловато-серые и желтовато-белые очажки. Под микроскопом находят лучистые кристаллы уратов, эпителий почечных канальцев в состоянии зернистой дистрофии и некроза, а строма инфильтрирована лимфоидными и гигантскими клетками.
Исход процесс необратимый.
Клиническое значение. Осложняется процесс воспалением органов и тканей и анкилозом суставов, пальцев.
3.2. Нарушение обмена глюкопротеидов
(слизистая дистрофия)
Мукоиды— слизеподобные вещества встречаются в различных тканях (костях, хрящах, сухожилиях, стенки артерий и др.).
Нарушение обмена глюкопротеидов выражается в накоплении слизи и слизеподобных веществ в тканях, т.е. слизистая дистрофия, которая наблюдается в эпителии слизистых оболочек и желез и в соединительной ткани.
При острых воспалениях слизистых оболочек наблюдается слизистая дистрофия покровного эпителия, при этом увеличивается количество бокаловидных клеток, а на поверхности ее большое количество легко смываемой слизи. При этом слизистые оболочки покрасневшие, набухшие. При хроническом воспалении вследствие закупорки густым экссудатом выводных протоков желез густой слизью или сдавливания их разрастающейся соединительной тканью образуются кисты.
Слизистая дистрофия соединительной ткани (волокнистой, хрящевой, костной и жировой) проявляется ослизнением их, когда ткани принимают отечный или студневидный вид.
Исход может быть двояким.
В слабой степени поражения или своевременном устранении причины, вызвавшей дистрофию, ткани приобретают нормальный вид. При далеко зашедшем процессе, вследствие распада тканей, образуются полости, содержащие слизь.
Клиническое значение. Зависит от степени поражения.
3.3. Нарушение обмена хромопротеидов
(пигментные дистрофии)
Всем тканям и органам свойственна определенная окраска, которая обусловливается пигментами. Одни пигменты находятся в органах и тканях в растворенном состоянии, другие имеют вид зернистых или аморфных, или кристаллических отложений.
Цвет ткани и органов при различных патологических состояниях зависит не только от содержания пигментов, а также от степени кровенаполнения, отложения жира, гликогена, солей, структурных нарушений тканевых элементов и других факторов.
Пигменты по своему происхождению делятся на эндогенные (образующиеся в самом организме) и экзогенные, привносимые извне.
Эндогенные пигменты подразделяются на:
Ангемоглобиногенные образуются при метаболических процессах из белка и жира.
Гемоглобиногенные пигменты являются производными гемоглобина.
К ангемоглобиногенным пигментам относятся мелании, липохром, липофусцин и лютеин.
Мелании обусловливает окраску кожи, волос, оперения, глаз и других органов при нарушении его обмена. В физиологических и патологических условиях образование меланина идет ферментативным путем из тирозина и триптофана в клетках мальпигиева слоя эпидермиса, сетчатки и радужки глаз.
Нарушение обмена меланина выражается в исчезновении или увеличении его содержания по сравнению с нормой, а также в появлении пигмента в органах, где обычно он не встречается. Врожденное исчезновение меланина называется альбинизмом, а индивиды с этими свойствами альбиносами. Приобретенное отсутствие меланина в участках на коже называется лейкодермией. Повышенное содержание меланина в органах и тканях называется меланозом (рис.7).
Рис.8. Меланоз печени.
Оно может быть местным и общим, врожденным и приобретенным. (Избыток пигмента в коже физиологически наблюдается у животных с черным окрасом и является врожденным, загар на коже приобретенным.).
При меланозах органы и ткани или отдельные части приобретают черный цвет (рис.8).
Рис.9. Меланома кожи.
Нарушение обмена гемоглобиногенных пигментов
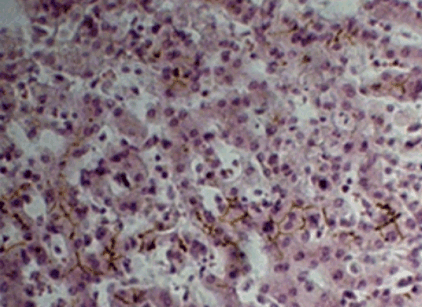
Рис.10. Гемосидероз почек.
Гемосидерин дает реакции: при обработке срезов по Перльсу пигмент окрашивается в зеленовато-синий цвет, от действия сернистого аммония гемосидерин чернеет, не обесцвечивается перекисью водорода, чем и диффенерцируется от меланина.
Различают местный и общий гемосидероз.
Общий гемосидероз наблюдается при внутрисосудистом гемолизе эритроцитов, который развивается в результате интоксикаций гемолитическими ядами (мышьяк, фосфор и др.), при некоторых инфекционных заболеваниях (сепсис, ИНАН, сибирская язва, пираплазмидозы и др.).При этом эритроциты распадаются в кровеносном русле и продукты распада их фагоцитируются многими ретикулярными клетками различных органов и преобразуют его в гемосидерин. В результате органы приобретают ржаво-бурую окраску различной интенсивности, в зависимости от количества образовавшегося гемосидерина. Если организм не погибает от интоксикации, то гемосидерин в органах рассасывается бесследно (рис.10).
Рис.11. Гемосидероз почек.
Местный гемосидероз возникает при внесосудистом гемолизе эритроцитов, что отмечается при кровоизлияниях, и тогда местные ретикулярные клетки синтезируют гемосидерин и продукты распада эритроцитов. Участки эти выглядят бурыми или ржаво-бурыми пятнами (в органах и тканях называют их следами кровоизлияний). С течением времени он рассасывается и орган принимает нормальный цвет. Желчный пигмент (биллирубин) входит в состав желчи. Биллирубин продукт распада гемоглобина, образуется клетками ретикуло-эндотелиальной системы печени, селезенки, костного мозга и лимфатических узлов. В норме биллирубин образуется в печени и вместе с желчью поступает в желчный пузырь и кишечник. В патологических условиях биллирубин может поступать в кровь и окрашивать различные органы и ткани в желтый цвет. Желтая окраска органов и тканей носит название желтуха (рис.11).
Желтуха как симптом характеризует целую группу инфекционных заболеваний (ИЭМ, лептоспироз, гемоспоридиоз и др.). При резко выраженной желтухе все органы и ткани (за исключением мозга) окрашиваются в желто-зеленый цвет; особенно ярко окрашиваются в желтый цвет слизистые оболочки, подкожная клетчатка, жировая ткань, интима сосудов и сердечных клапанов. При фиксации формалином ткани, пропитанные пигментами, приобретают зеленый цвет.
По этиологическими и патогенетическим признакам различают 3 вида желтухи:
Этот пигмент появляется в патологических условиях. Как правило, в кровоизлияниях, в тромбах в виде игольчатых единичных или множественных оранжево-зеленоватых кристаллов гематоидина.
© ФГБОУ ВПО Красноярский государственный аграрный университет