ОПТИЧЕСКАЯ АКТИВНОСТЬ
Полезное
Смотреть что такое «ОПТИЧЕСКАЯ АКТИВНОСТЬ» в других словарях:
ОПТИЧЕСКАЯ АКТИВНОСТЬ — свойство некоторых веществ вызывать вращение плоскости поляризации проходящего через них плоско поляризованного света. Оптически активные вещества бывают двух типов. У веществ первого типа (сахар, камфора, винная кислота) оптическая активность не … Большой Энциклопедический словарь
ОПТИЧЕСКАЯ АКТИВНОСТЬ — ОПТИЧЕСКАЯ АКТИВНОСТЬ, способность среды вызывать вращение плоскости поляризации проходящего через неё света. Впервые обнаружена французским учёным Д. Араго в кварце в 1811; в 1815 французский физик Ж.Б. Био открыл оптическую активность в чистой… … Современная энциклопедия
Оптическая активность — ОПТИЧЕСКАЯ АКТИВНОСТЬ, способность среды вызывать вращение плоскости поляризации проходящего через неё света. Впервые обнаружена французским учёным Д. Араго в кварце в 1811; в 1815 французский физик Ж.Б. Био открыл оптическую активность в чистой… … Иллюстрированный энциклопедический словарь
ОПТИЧЕСКАЯ АКТИВНОСТЬ — ОПТИЧЕСКАЯ АКТИВНОСТЬ, свойство некоторых химических соединений в растворах, а также некоторых кристаллов и прозрачных веществ, под действием сильного магнитного поля, вызывать вращение ПЛОСКОСТИ ПОЛЯРИЗОВАННОГО СВЕТА. Оптически активные… … Научно-технический энциклопедический словарь
оптическая активность — Свойство среды, заключающееся в различии показателей преломления для оптического излучения с правой и левой круговой поляризацией при распространении их в этой среде. [ГОСТ 23778 79] Тематики оптика, оптические приборы и измерения EN optical… … Справочник технического переводчика
оптическая активность — свойство некоторых веществ вызывать вращение плоскости поляризации проходящего через них плоскополяризованного света. Оптически активные вещества бывают двух типов. У веществ первого типа (сахара, камфара, винная кислота) оптическая активность не … Энциклопедический словарь
Оптическая активность — способность среды вызывать Вращение плоскости поляризации проходящего через неё оптического излучения (См. Оптическое излучение) (света). Впервые обнаружена в 1811 Д. Ф. Араго в кварце. В 1815 Ж. Б. Био открыл О. а. чистых жидкостей… … Большая советская энциклопедия
Оптическая активность — Оптически активные вещества среды, обладающие естественной оптической активностью. Оптическая активность это способность среды (кристаллов, растворов, паров вещества) вызывать вращение плоскости поляризации проходящего через неё оптического… … Википедия
оптическая активность — optinis aktyvumas statusas T sritis Standartizacija ir metrologija apibrėžtis Medžiagos savybė sukti šviesos poliarizacijos plokštumą. atitikmenys: angl. optical activity vok. optische Aktivität, f rus. оптическая активность, f pranc. activité… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
оптическая активность — optinis aktyvumas statusas T sritis chemija apibrėžtis Medžiagos savybė sukti šviesos poliarizacijos plokštumą. atitikmenys: angl. optical activity rus. оптическая активность … Chemijos terminų aiškinamasis žodynas
Оптически активные вещества
Оптически активные вещества — среды, обладающие естественной оптической активностью. Оптическая активность — это способность среды (кристаллов, растворов, паров вещества) вызывать вращение плоскости поляризации проходящего через неё оптического излучения (света). Метод исследования оптической активности — поляриметрия.
Содержание
Типы оптически активных веществ
Оптически активные вещества подразделяются на 2 типа:
Относящиеся к 1-му из них оптически активны в любом агрегатном состоянии (сахара, камфора, винная кислота), ко 2-му — активны только в кристаллической фазе (кварц, киноварь). У веществ 1-го типа оптическая активность обусловлена асимметричным строением их молекул, 2-го типа — специфической ориентацией молекул (ионов) в элементарных ячейках кристалла (асимметрией поля сил, связывающих частицы в кристаллической решётке).
Кристаллы оптически активных веществ всегда существуют в двух формах — правой и левой; при этом решётка правого кристалла зеркально-симметрична решётке левого и не может быть пространственно совмещена с нею (т. н. энантиоморфные формы). Оптической активности правой и левой форм оптически активных веществ 2-го типа имеют разные знаки (и равны по абсолютной величине при одинаковых внешних условиях), поэтому их называется оптическими антиподами (иногда так называют и кристаллы оптически активных веществ 1-го типа).
Молекулы правого и левого оптически активных веществ 1-го типа являются оптическими изомерами (см. Изомерия, Стереохимия), то есть по своему строению представляют собой зеркальные отражения друг друга. Их можно отличить одну от другой, в то время как частицы оптических антиподов (оптически активные вещества 2-го типа) просто неразличимы (идентичны). Физические и химические свойства чистых оптических изомеров совершенно одинаковы в отсутствие какого-либо асимметричного агента, реагирующего на зеркальную асимметрию молекул. Продукт химической реакции без участия такого агента — всегда смесь оптических изомеров в равных количествах, т. н. рацемат. Физические свойства рацемата и чистых оптических изомеров зачастую различны. Например, температура плавления рацемата несколько ниже, чем чистого изомера. Рацемат разделяют на чистые изомеры либо отбором энантиоморфных кристаллов, либо в химической реакции с участием асимметричного агента — чистого изомера или асимметричного катализатора, либо микробиологически. Последнее свидетельствует о наличии асимметричных агентов в биологических процессах и связано со специфическим и пока не нашедшим удовлетворительного объяснения свойством живой природы строить белки из левых оптических изомеров аминокислот — 19 из 20 жизненно важных аминокислот оптически активны. (Применительно к Оптически активным веществам 1-го типа термины «левый» и «правый» — L и D — условны в том смысле, что не соответствуют непосредственно направлению вращения плоскости поляризации в них, в отличие от этих же терминов — l и d — для Оптически активных веществ 2-го типа или терминов «левовращающий» и «правовращающий».)
Влияние на организм
Физиологическое и биохимическое действие оптических изомеров часто совершенно различно. Например, белки, синтезированные искусственным путём из D-аминокислот, не усваиваются организмом; бактерии сбраживают лишь один из изомеров, не затрагивая другой; L-никотин в несколько раз ядовитее D-никотина. Удивительный феномен преимущественной роли только одной из форм оптических изомеров в биологических процессах может иметь фундаментальное значение для выяснения путей зарождения и эволюции жизни на Земле.
Оптическая активность
Вы будете перенаправлены на Автор24
Поляриметрия
Под оптической активностью понимают способность растворов, паров веществ, кристаллов вызывать вращение плоскости поляризации проходящего через данную среду оптического излучения.
Оптически активные вещества делят на правовращающие (вращающие положительно) и левовращающие (вращающие отрицательно) виды. Разновидность зависит от поворота плоскости поляризации (по или против часовой стрелки, если смотреть навстречу ходу лучей света).
Вращающая способность вещества зависит от длины волны излучения и от температуры. При определении оптической активности вещества используют монохроматическое излучение при постоянной температуре.
Величина, зависящая от угла φ, определенного на поляриметре, длины l (в дециметрах) пропускающего слоя вещества, называют удельным вращением [α].
Удельное вращение представляет собой угол, на который 1 г вещества в 1 мл жидкости отклоняет плоскость поляризации света при длине пропускающего слоя, равной 1 дм.
Часто удельное вращение изменяется с природой растворителя.
В одном и том же растворителе удельное вращение не всегда меняется пропорционально концентрации в результате явлений сольватации, ассоциации, ионизации.
Принцип свободного вращения
Два атома, связанные между собой простой связью, согласно классической стереохимии, свободно вращаются вместе с заместителями вокруг общей связи.
Готовые работы на аналогичную тему
Принцип свободного вращения подходит не для всех соединений. Известны вещества, в которых свободное вращение относительно общей связи заторможено, что приводит к возникновению оптически активных изомеров.
Существуют соединения, в которых в определенных положениях вращение затруднено, то есть является ограниченным вращением.
Молекулярная асимметрия – условие оптической активности
Еще Пастер установил, что только вещества, обладающие асимметрическим строением, будут оптически активными. Молекула является асимметричной, если при любом вращении она не совпадает со своим зеркальным отражением.
Молекула является асимметричной, если не обладает плоскостью и центром симметрии. Оптические изомеры отличаются расположением атомов и групп атомов в трехмерном пространстве.
В молекуле, содержащей два асимметричных атома углерода, каждый атом сохраняет свою индивидуальность. В таком случае наблюдаемый эффект является суммой действия каждого атома.
Например: В алкалоиде эфедрине оба асимметричных атома могут быть поочередно правовращающими или левовращающими. Следовательно, возможны конфигурации:
В случае 1,2, когда оба симметричных атома правовращающие или левовращающие, их действие суммируется. В первом случае молекула будет правовращающей, во втором – левовращающей. Если же атомы имеют разные направления вращения, то оптичекая активность будет разностью активностей этих двух атомов.
Следовательно, молекула с двумя асимметричными атомами может обладать четырьмя оптически активными формами. Существуют две рацемические смеси с разными физическими свойствами.
Формы 1 и 2 не будут оптическими антиподамидля форм 3 и 4, они не относятся друг к другу как предметы к своему зеркальному отражению. Изомеры 1 и 2 являются диастереоизомерами форм 3 и 4.
Число оптических изомеров молекул, которые содержат n асимметричных атомов, равно 2n.
Например: Молекула, имеющая три асимметричных атома будет обладать 23=8 изомерами (четыре пары антиподов), молекула с четырьмя асимметричнымиатомами – 16 изомерами или 8 парами антиподов и т.д.
Внутримолекулярная компенсация
Иногда, оба асимметричных атома в молекуле обладают тождественным строением, то есть каждый из асимметричных атомов замещен одинаковыми группами.
Неактивные вследствие внутримолекулярной компенсации изомеры отличаются от неактивных рацемических форм тем, что их нельзя расщепить на оптические антиподы.
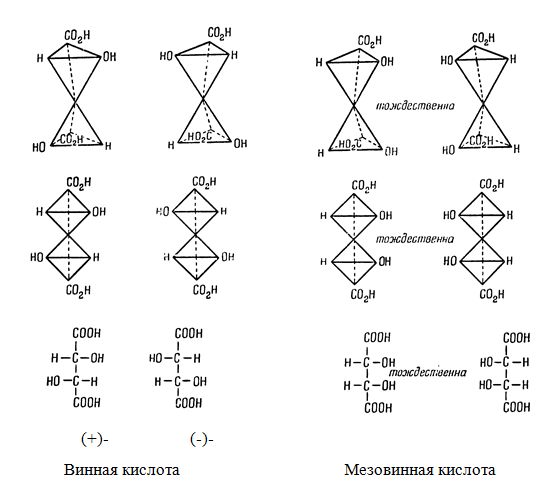
Для изображения винных кислот и аналогичных соединений пользуются:
Конфигурационные формулы (+), (-) винных кислот не имеют плоскости симметрии. Так как они в пространстве несовместимы ни при каких вращениях, то представляют собой два оптических антипода.
Молекула мезовинной кислоты обладает плоскостью симметрии, а при определенном положении тетраэдров относительно друг друга, и центром симметрии. Поэтому данное соединение оптически неактивное.
Получи деньги за свои студенческие работы
Курсовые, рефераты или другие работы
Автор этой статьи Дата последнего обновления статьи: 05 06 2021
Что такое оптическая активность
В теоретической стереохимии атомы рассматриваются как безразмерные точки, и структура молекул описывается пространственной группой таких точек, которые образуют шестиугольник в случае бензола, прямую линию в случае ацетилена, тетраэдр в случае метана и т.д. Благодаря такому упрощению можно легко провести классификацию молекул по топологии симметрии и найти аналогию между, казалось бы, совершенно разными структурами, например, между метаном и адамантаном (см. раздел 8.2.2.г).
Основными стереохимическими понятиями являются хиральность, конфигурация и конформация, смысл которых будет рассмотрен в следующих разделах.
8.2. Оптическая активность и хиральность
8.2.1. Оптическая активность
Впервые оптическая активность была обнаружена в 1811 г. Д.Араго в кристаллах кварца. В 1815 г. Ж.Био открыл оптическую активность чистых жидкостей (скипидара), а затем растворов и паров многих, главным образом органических веществ. Ж.Био установил, что поворот плоскости поляризации происходит либо по часовой стрелке, либо против нее, если посмотреть навстречу ходу лучей света и в соответствии с этим разделил оптически активные вещества на правовращающие (вращающие положительно, т.е. по часовой стрелке) и левовращающие (отрицательно вращающие) разновидности. Наблюдаемое значение угла поворота плоскости поляризации в случае раствора связано с толщиной образца (l) и концентрацией оптически активного вещества (С) следующей формулой:
Коэффициент [a ] называется удельной оптической активностью или удельным вращением.
Оптически активными веществами называют лишь те вещества, которые проявляют естественную оптическую активность. Существует также и искусственная или наведенная оптическая активность. Ее проявляют оптически неактивные вещества при помещении в магнитное поле (эффект Фарадея). Различить естественную или наведенную оптическую активность довольно просто: если линейно поляризованный свет (см. раздел 8.2.1.б), прошедший через слой вещества с естественной оптической активностью отражается и проходит через вещество в обратном направлении, то исходная поляризация света восстанавливается (суммарный угол вращения j = 0). В среде же с наведенной оптической активностью в аналогичном опыте угол поворота удваивается. В дальнейшем мы будем рассматривать лишь вещества с естественной оптической активностью и для краткости будем их называть просто «оптически активными веществами».
8.2.1.а. Оптически активные вещества
У соединений второго типа оптическая активность обусловлена диссимметрическим строением самих молекул. Если зеркальное отображение молекулы никакими вращениями и перемещениями не может быть наложено на оригинал, молекула оптически активна; если такое наложение осуществить удается, то молекула оптически неактивна. (Под зеркалом понимают отражатель, лежащий вне молекулы, и отражение дает отображение всей молекулы). Следует особо подчеркнуть, что необходимо употреблять выражение «диcсимметрическое строение», а не «асимметрическое строение». Асимметрические молекулы не имеют никаких элементов симметрии (кроме операции идентичности; см.раздел 8.2.2.в), тогда как в дисcимметрических молекулах некоторые элементы симметрии остаются. Диcсимметрия есть нарушение максимальной симметрии объекта.
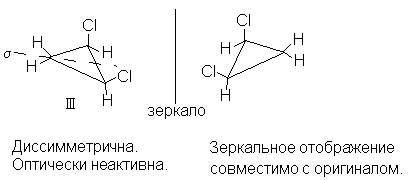
Молекула бромхлофторметана (I ) асимметрична, а молекула транс-1,2-дихлорциклопропана (I I ) лишь диcсимметрична, т.к. имеет ось симметрии второго порядка (С2), но оба вещества оптически активны, т.к. не идентичны своим зеркальным отображениям.
Следовательно, оптическая активность связана лишь с определенным видом диcсимметрии (см. раздел 8.2.2), а именно с дисcимметрией, обусловливающей несовместимость объекта с его зеркальным отображением. Такой же вид диссимметрии, как сказано выше, получил название хиральность. Хиральные объекты относятся друг к другу как правая и левая рука, или винты с правой и левой резьбой, т.е. они несовместимы в пространстве и представляются как зеркальные отображения друг друга. Оптически активная молекула хиральна, а оптически неактивная ахиральна, однако если молекулу нельзя совместить с ее зеркальным отображением, то зеркальное отображение соответствует другой, отличной молекуле, которую, в принципе, можно синтезировать. Синтезированное зеркальное отображение хиральной молекулы будет ее реальным оптическим изомером (не рекомендуется употреблять термин оптический антипод, как в случае кристаллов). Чистое оптически активное соединение имеет два и только два оптических изомера (т.к. каждому объекту соответствует лишь одно зеркальное отображение). Оптические изомеры называются энантиомерами (или иногда энантиоморфами). Удельное вращение ([a ] в формуле (1)) энантиомеров одинаково по абсолютной величине и противоположно по знаку: один энантиомер левовращающий, а второй правовращающий. Кроме знака вращения все другие физические и химические свойства энантиомеров в газовой фазе, а также в ахиральных жидких средах одинаковы. Однако, если жидкая среда хиральна (например, в раствор добавлен хиральный реагент или катализатор, или сам растворитель хирален) свойства энантиомеров начинают различаться. При взаимодействии с другими хиральными соединениями, отзывающимися на зеркальную изомерию молекул, энантиомеры реагируют с различными скоростями. Особенно ощутимо различие в физиологическом и биохимическом действии энантиомеров, что связано с энантиомерией биологических реагентов и катализаторов. Так, природные белки состоят из левых оптических изомеров аминокислот и поэтому искусственно синтезированные правые аминокислоты организмом не усваиваются; дрожжи сбраживают лишь правые изомеры сахаров, не затрагивая левые и т.д.
Общее правило состоит в том, что энантиомеры проявляют идентичные свойства в симметричном (ахиральном) окружении, а в несимметричном (хиральном) окружении их свойства могут изменяться, Это свойство используется в асимметрическом синтезе и катализе (см. раздел 8.6).
8.2.1.б. Физические причины оптической активности
Феноменологическую модель оптической активности предложил Френель еще в 1823 г. Она основана на волновой теории света и с позиций современной науки не является достаточно строгой. Тем не менее эта модель дает очень наглядное представление о причинах оптической активности и других явлениях, связанных с поглощением света хиральным веществом, в рамках классической электродинамики, поэтому ее часто используют и в настоящее время.
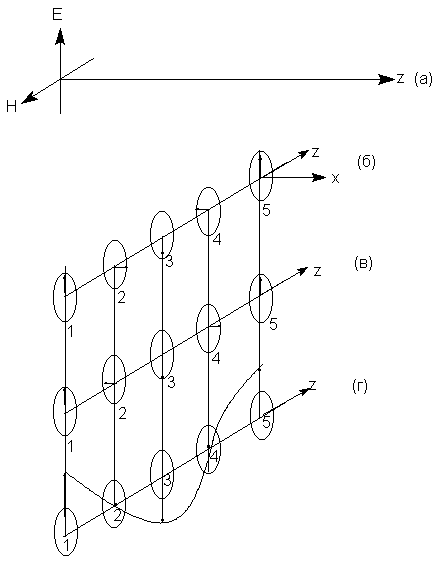
Согласно классическим представлениям, линейнополяризованный (плоскополяризованный) свет характеризуется тем, что векторы составляющих его зависимых от времени электрического (Е) и магнитного (Н) полей осциллируют во взаимно перпендикулярных плоскостях и их изменения носят синусоидальный характер во времени и в пространстве (рис. 8.1.а). Плоскополяризованный свет можно рассматривать как комбинацию левого и правого циркулярнополяризованных лучей, движущихся в фазе по отношению друг к другу. На рис. 8.1.б-г магнитные составляющие не показаны, а показаны лишь электрические векторы в моменты времени 1,2,3,4 и 5. (Этого вполне достаточно т.к. магнитные векторы всегда ориентированы ортогонально электрическим). Если в начальной точке времени 1 электрические векторы левого и правого циркулярнополяризованных лучей ориентированы вверх, то в точке 2 вектор правого луча ориентирован вправо, а вектор левого луча влево (если смотреть в направлении движения света по оси z). В точке 3 векторы обоих лучей ориентированы вниз, в точке 4 вектор правого луча ориентирован влево, а вектор левого луча вправо, и т.д. Таким образом, правый и левый циркулярнополяризованные лучи обладают соответственно правой и левой спиральностью вращения вектора электрического поля. Сумма этих лучей дает плоскополяризованный луч (рис. 8.1.г), причем в пространственно-временных точках 1,3 и 5 векторы суммируются, а в точках 2 и 4 взаимно уничтожаются. Расстояние между точками 1 и 5 соответствует одному витку правой или левой спирали или длине плоской волны (рис.8.1.г).
При попадании света на любую молекулу в прозрачной среде, скорость его замедляется (уменьшение скорости пропорционально показателю преломления среды), так как свет взаимодействует с электронными оболочками молекул. Степень такого взаимодействия зависит от поляризуемости молекулы.
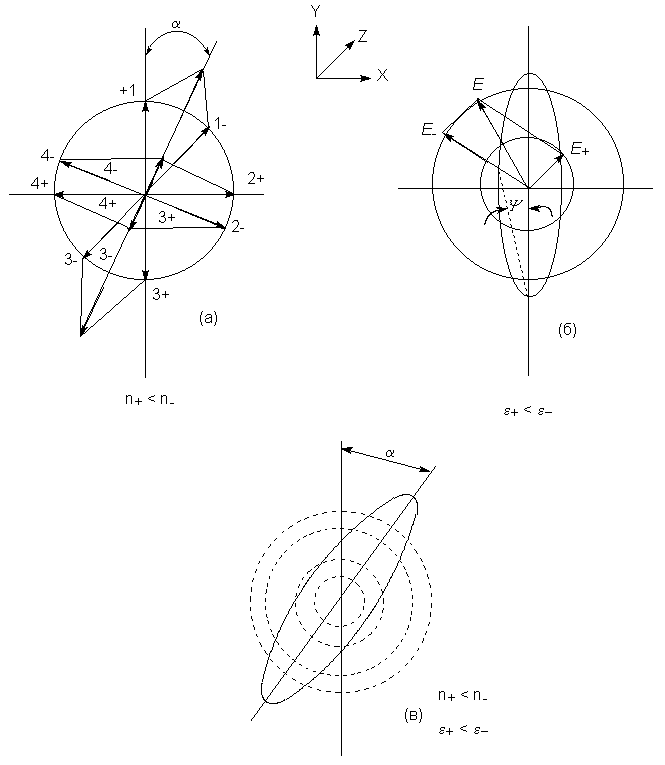
Если среда ахиральна, две циркулярнополяризованные составляющие проходят с одинаковой скоростью (т.е. с одинаковыми показателями преломления для правого и левого лучей). Однако хиральные молекулы проявляют анизотропию поляризуемости, которая зависит от того, левую или правую спиральность имеет циркулярнополяризованный луч. Например, левый циркулярнополяризованный луч может замедлиться сильнее правого, тогда произойдет сдвиг по фазе. Так как левый луч отстает от правого, векторы равной амплитуды не будут находиться в одинаковых фазах. В результате плоскость прошедшего через хиральный раствор луча будет вращаться на некоторый угол относительно плоскости падающего луча (рис. 8.2.а). При прохождении через хиральную среду в общем случае неодинаковы не только скорости, но и коэффициенты поглощения левого и правого циркулярнополяризованных компонент плоскополяризованного света. В результате векторы для правого и левого прошедшего через образец лучей будут иметь разную амплитуду, а результирующий вектор будет описывать эллиптическую траекторию (рис. 8.2.б). В общем, при прохождении плоскополяризованного света через хиральную среду вектор электрического поля начинает описывать эллипс (эллиптическая поляризация) с повернутой главной осью (рис. 8.2.в).
Полученное Френелем выражение для угла поворота плоскости поляризации имеет вид:
Разность поглощения правой и левой компонент называется круговым дихроизмом (КД). Количественной характеристикой КД служит угол эллиптичности y (рис. 2), величина которого обратно пропорциональна длине волны
Квантовую теорию оптической активности построил в 1928 г. бельгийский физик Л. Розенфельд. С позиций современной науки эта теория рассматривается как более строгая. Для объяснения оптической активности оказалось необходимым учитывать взаимодействие электрических и магнитных дипольных моментов, наведенных в молекуле полем проходящей световой волны.
Поскольку фотоны обладают целочисленным спином, в одном и том же состоянии может находится любое число фотонов. Это обусловливает возможность описания электромагнитных взаимодействий с участием большого числа фотонов в рамках классической (а не только квантовой) механики. Циркулярно-поляризованный свет можно рассматривать как поток фотонов, имеющих только правую или только левую спиральность. Плоскополяризованный свет состоит из одинакового количества «левых» и «правых» фотонов. Взаимодействие по-разному поляризованных фотонов с хиральной анизотропной средой происходит неодинаково, что приводит к хироптическим эффектам.
Следует подчеркнуть, что ахиральная молекула не вращает плоскость поляризации света только при определенной ее ориентации по отношению к падающему лучу. Например, ахиральная молекула, имеющая плоскость симметрии, не вращает плоскость поляризации лишь в том случае, если плоскость поляризации совпадает с плоскостью симметрии. Все же остальные молекулы, не ориентированные таким образом, вращают плоскость поляризации, даже не будучи хиральными. Однако в целом образец не вращает, так как в массе молекулы ориентированы беспорядочно, и одни молекулы вращают плоскость поляризации в одном направлении, а другие молекулы, встречающиеся на пути светового луча, вращают ее в противоположную сторону. Таким образом коллектив ахиральных молекул имеет суммарное вращение, равное нулю, хотя каждая молекула может вращать плоскость поляризации. В случае хиральных соединений молекул противоположной ориентации (если это не рацемическая смесь) просто не может существовать, и вращение наблюдается.
8.2.1.в. Зависимость угла вращения от условий измерения
Известны случаи обращени знака вращения при изменении длины волны, растворителя и концентрации. Теоретически удельное вращение не должно зависеть от концентрации, т.к. концентрация уже учитывается в уравнении (8.1). Тем не менее возможны отклонения от линейной зависимости [a ] от С за счет ассоциации, диссоциации и взаимодействия между растворителем и растворенным веществом. Например, хиральные карбоновые кислоты могут менять знак и величину вращения в зависимости от рН и основности растворителя, поскольку недиссоциированная кислота и ее анион обладают разным вращением.
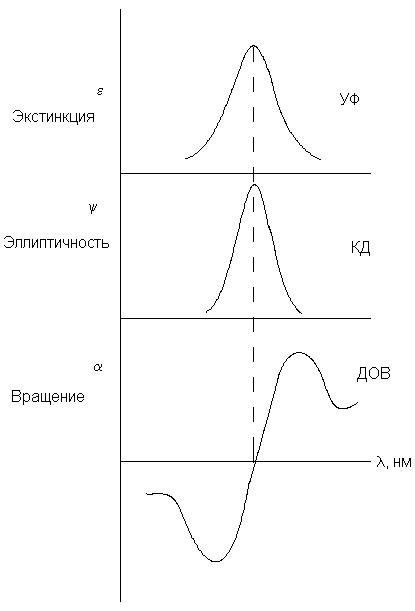
Кривые ДОВ и КД тесно связаны с электронными спектрами хиральных молекул (рис.8.3). В случае индивидуального электронного перехода максимумы на УФ- и КД-кривых и точка, в которой кривая ДОВ меняет знак, почти совпадают. Пример на рис.8.3 отвечает положительному эффекту Коттона. Если же максимум на кривой КД и длинноволновой экстремум кривой ДОВ отрицательны (направлены вниз), то эффект Коттона называется отрицательным. Энантиомеры дают зеркально-симметричные кривые ДОВ и КД.
Если имеется несколько максимумов в УФ-спектре, эффект Коттона может быть довольно сложным. Хироптические методы щироко используются для установления относительных конфигураций молекул (см. раздел 8.4).
8.2.2. Хиральные молекулы
Теперь необходимо рассмотреть вопрос: как определить, будет ли данная молекула хиральна? Обязательным условием хиральности является несовместимость объекта с зеркальным отображением:
В случае простых молекул легко проводится зрительное распознавание несовместимости с зеркальным отображением. Однако многие органические молекулы настолько сложны, что такой способ требует очень развитого пространственного воображения, которым обладают далеко не все.
Рис.3. Соотношение между УФ-спектром, КД и ДОВ (в случае индивидуальной полосы УФ-поглощения).
Следовательно, необходимо установить какие-то общие критерии, облегчающие распознавание хиральных молекул. Прежде всего обратимся к теории симметрии и кратко рассмотрим элементы, операции и группы симметрии.
8.2.2.а. Точечные группы симметрии
Шар самый симметричный объект, поскольку как бы мы его не повернули, не переместили в пространстве, не отразили в зеркале, он всегда выглядит одинаково. Тетраэдр «менее симметричен», чем шар, поскольку вокруг высоты его нужно повернуть лишь на определенный угол (120 0 ), чтобы он выглядел так же, как до поворота. Вращение вокруг оси является одной из операций симметрии. Операцией симметрии называется действие над объектом, которое приводит к его новой ориентации, неотличимой от исходной и совмещаемой с нею.
Рассмотрим несколько подробнее два главных вида элементов симметрии и связанные с ними операции симметрии: собственную и несобственную оси вращения.
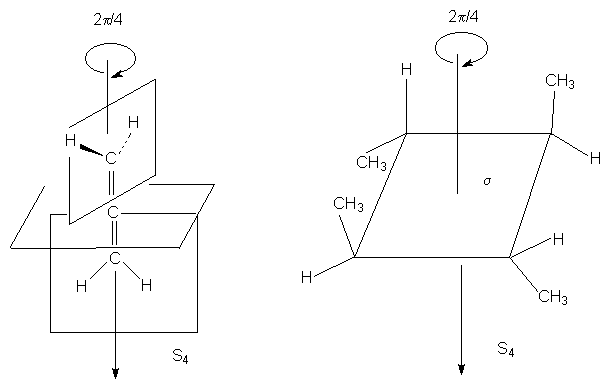
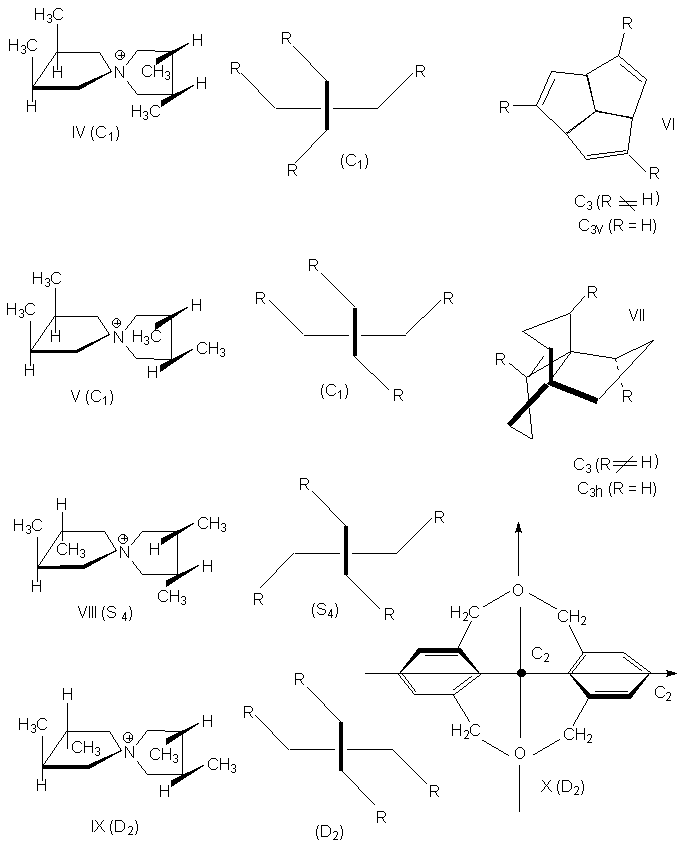
Несобственная ось симметрии. Простейшая зеркально поворотная ось S1 эквивалентна перпендикулярной ей плоскости симметрии (S1 є s ). Примером является молекула хлорфторметана. Зеркально-поворотные оси более высокого порядка (Sn) можно рассматривать как комбинацию вращения на угол 2p /n с последующим отражением в плоскости, перпендикулярной оси вращения. Так, аллен и изображенный ниже изомер 1,2,3,4-тетраметилциклобутана имеет зеркально-поворотную ось S4:
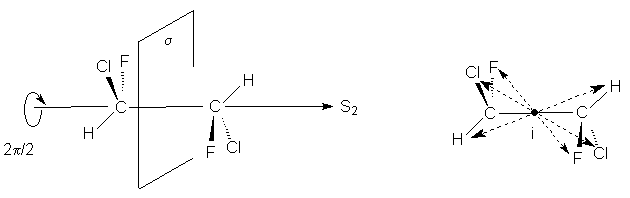
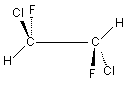
1,2-Дихлор-1,2-дифторэтан обладает осью S2, которая совпадает со связью С-С. Как видно операция S2 эквивалентна инверсии в центр симметрии, который в данном случае находится посредине связи С-С (S2 є i)
Точечные группы симметрии. Поскольку у молекул может быть не один, а несколько элементов симметрии, их удобнее классифицировать по точечной группе симметрии. Набор все операций симметрии объекта образует его группу симметрии. Если при всех этих преобразованиях остается неподвижным центр тяжести фигуры, то группа симметрии называется точечной. Известны четыре типа точечных групп симметрии, которые представлены в табл. 8.1.
Точечные группы симметрии
Элементы симметрии
Примеры
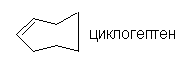
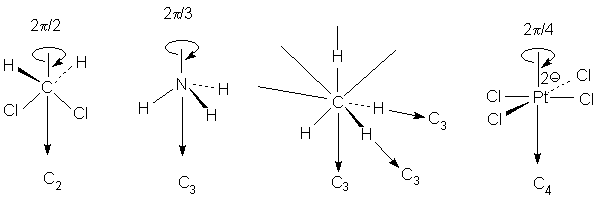
Отметим, что термины «тетраэдрическое строение» и «симметрия Td» не идентичны. Например, молекула хлороформа CHCl3 имеет тетраэдрическое строение, однако ее симметрия не является тетраэдрической; она принадлежит к группе C3v (как аммиак), а не к группе Td.


Сервер создается при поддержке Российского фонда фундаментальных исследований
Не разрешается копирование материалов и размещение на других Web-сайтах
Вебдизайн: Copyright (C) И. Миняйлова и В. Миняйлов
Copyright (C) Химический факультет МГУ
Написать письмо редактору