Что такое основания 8 класс
Основания

Всего получено оценок: 1701.
Всего получено оценок: 1701.
Один из классов сложных неорганических веществ – основания. Это соединения, включающие атомы металла и гидроксильную группу, которая может отщепляться при взаимодействии с другими веществами.
Строение
Основания могут содержать одну или несколько гидроксо-групп. Общая формула оснований – Ме(ОН)х. Атом металла всегда один, а количество гидроксильных групп зависит от валентности металла. При этом валентность группы ОН всегда I. Например, в соединении NaOH валентность натрия равна I, следовательно, присутствует одна гидроксильная группа. В основании Mg(OH)2 валентность магния – II, Al(OH)3 валентность алюминия – III.
Количество гидроксильных групп может меняться в соединениях с металлами с переменной валентностью. Например, Fe(OH)2 и Fe(OH)3. В таких случаях валентность указывается в скобках после названия – гидроксид железа (II), гидроксид железа (III).
Физические свойства
Характеристика и активность основания зависит от металла. Большинство оснований – твёрдые вещества белого цвета без запаха. Однако некоторые металлы придают веществу характерную окраску. Например, CuOH имеет жёлтый цвет, Ni(OH)2 – светло-зелёный, Fe(OH)3 – красно-коричневый.

Основания классифицируются по двум признакам:
Щёлочи образуются щелочными металлами – литием (Li), натрием (Na), калием (K), рубидием (Rb) и цезием (Cs).
Все остальные основания, например, Mg(OH)2, Cu(OH)2, Al(OH)3, относятся к нерастворимым.
По-другому щёлочи называются сильными основаниями, а нерастворимые – слабыми основаниями. При электролитической диссоциации щёлочи быстро отдают гидроксильную группу и быстрее вступают в реакцию с другими веществами. Нерастворимые или слабые основания менее активные, т.к. не отдают гидроксильную группу.
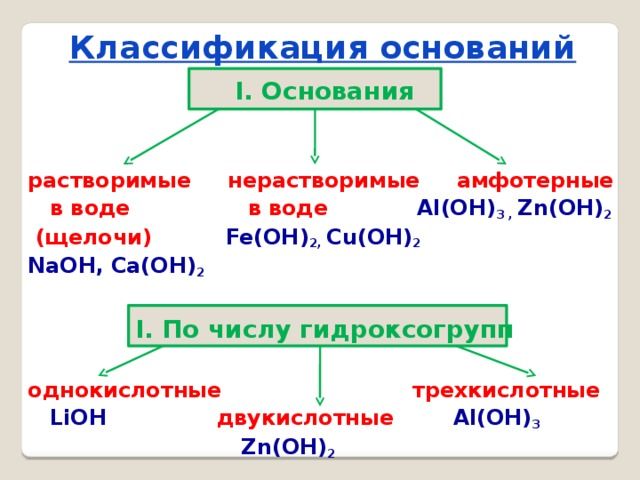
Особое место в систематизации неорганических веществ занимают амфотерные гидроксиды. Они взаимодействуют и с кислотами, и с основаниями, т.е. в зависимости от условий ведут себя как щёлочь или как кислота. К ним относятся Zn(OH)2, Al(OH)3, Pb(OH)2, Cr(OH)3, Be(OH)2 и другие основания.
Получение
Основания получают различными способами. Самый простой – взаимодействие металла с водой:
Щёлочи получают в результате взаимодействия оксида с водой:
Нерастворимые основания получаются в результате взаимодействия щелочей с солями:
Химические свойства
Основные химические свойства оснований описаны в таблице.
Реакции
Что образуется
Примеры
Соль и вода. Нерастворимые основания взаимодействуют только с растворимыми кислотами
Разложение при высокой температуре
Оксид металла и вода
С кислотными оксидами (реагируют щёлочи)
С неметаллами (вступают щёлочи)
Щелочей с некоторыми металлами
Сложная соль и водород
С помощью индикатора проводится тест на определение класса основания. При взаимодействии с основанием лакмус становится синим, фенолфталеин – малиновым, метилоранж – жёлтым.
Что мы узнали?
Из урока 8 класса химии узнали об особенностях, классификации и взаимодействии оснований с другими веществами. Основания – сложные вещества, состоящие из металла и гидроксильной группы ОН. Они делятся на растворимые или щёлочи и нерастворимые. Щёлочи – более агрессивные основания, быстро реагирующие с другими веществами. Основания получают при взаимодействии металла или оксида металла с водой, а также в результате реакции соли и щёлочи. Основания реагируют с кислотами, оксидами, солями, металлами и неметаллами, а также разлагаются при высокой температуре.
Основания. Химические свойства и способы получения
Перед изучением этого раздела рекомендую прочитать следующую статью:
Получение оснований
1. Взаимодействие основных оксидов с водой. При этом с водой реагируют в обычных условиях только те оксиды, которым соответствует растворимое основание (щелочь). Т.е. таким способом можно получить только щёлочи:
основный оксид + вода = основание
Na2O + H2O → 2NaOH
При этом оксид меди (II) с водой не реагирует:
CuO + H2O ≠
2. Взаимодействие металлов с водой. При этом с водой реагируют в обычных условиях только щелочные металлы (литий, натрий, калий. рубидий, цезий) , кальций, стронций и барий. При этом протекает окислительно-восстановительная реакция, окислителем выступает водород, восстановителем является металл.
металл + вода = щёлочь + водород
2K 0 + 2 H2 + O → 2 K + OH + H2 0
2NaCl + 2H2O → 2NaOH + H2↑ + Cl2↑
4. Основания образуются при взаимодействии других щелочей с солями. При этом взаимодействуют только растворимые вещества, а в продуктах должна образоваться нерастворимая соль, либо нерастворимое основание:
щелочь + соль1 = соль2↓ + щелочь
щелочь + соль1 = соль2↓ + щелочь
Например: карбонат калия реагирует в растворе с гидроксидом кальция:
Например: хлорид меди (II) взаимодействет в растворе с гидроксидом натрия. При этом выпадает голубой осадок гидроксида меди (II):
CuCl2 + 2NaOH → Cu(OH)2↓ + 2NaCl
Химические свойства нерастворимых оснований
1. Нерастворимые основания взаимодействуют с сильными кислотами и их оксидами (и некоторыми средними кислотами). При этом образуются соль и вода.
нерастворимое основание + кислота = соль + вода
нерастворимое основание + кислотный оксид = соль + вода
При этом гидроксид меди (II) не взаимодействует с кислотным оксидом слабой угольной кислоты – углекислым газом:
2. Нерастворимые основания разлагаются при нагревании на оксид и воду.
3. Нерастворимые основания не взаимодействуют с амфотерными оксидами и гидроксидами.
нерастворимое оснвоание + амфотерный оксид ≠
нерастворимое основание + амфотерный гидроксид ≠
4. Некоторые нерастворимые основания могут выступать в качестве восстановителей. Восстановителями являются основания, образованные металлами с минимальной или промежуточной степенью окисления, которые могут повысить свою степень окисления (гидроксид железа (II), гидроксид хрома (II) и др.).
Химические свойства щелочей
щёлочь(избыток)+ кислота = средняя соль + вода
щёлочь + многоосновная кислота(избыток) = кислая соль + вода
При этом дигидрофосфаты образуются в избытке кислоты, либо при мольном соотношении (соотношении количеств веществ) реагентов 1:1.
При мольном соотношении количества щелочи и кислоты 2:1 образуются гидрофосфаты:
В избытке щелочи, либо при мольном соотношении количества щелочи и кислоты 3:1 образуется фосфат щелочного металла.
щёлочь (расплав) + амфотерный оксид = средняя соль + вода
щёлочь (расплав) + амфотерный гидроксид = средняя соль + вода
щёлочь (раствор) + амфотерный оксид = комплексная соль
щёлочь (раствор) + амфотерный гидроксид = комплексная соль
А в растворе образуется комплексная соль:
Обратите внимание, как составляется формула комплексной соли: сначала мы выбираем центральный атом (к ак правило, это металл из амфотерного гидроксида). Затем дописываем к нему лиганды — в нашем случае это гидроксид-ионы. Число лигандов, как правило, в 2 раза больше, чем степень окисления центрального атома. Но комплекс алюминия — исключение, у него число лигандов чаще всего равно 4. Заключаем полученный фрагмент в квадртаные скобки — это комплексный ион. Определяем его заряд и снаружи дописываем нужное количество катионов или анионов.
3. Щёлочи взаимодействуют с кислотными оксидами. При этом возможно образование кислой или средней соли, в зависимости от мольного соотношения щёлочи и кислотного оксида. В избытке щёлочи образуется средняя соль, а в избытке кислотного оксида образуется кислая соль:
щёлочь(избыток) + кислотный оксид = средняя соль + вода
щёлочь + кислотный оксид(избыток) = кислая соль
А при взаимодействии избытка углекислого газа с гидроксидом натрия образуется только гидрокарбонат натрия:
2NaOH + CO2 = NaHCO3
щёлочь + растворимая соль = соль + соответствующий гидроксид
Щёлочи взаимодействуют с растворами солей металлов, которым соответствуют нерастворимые или неустойчивые гидроксиды.
Cu 2+ SO4 2- + 2Na + OH — = Cu 2+ (OH)2 — ↓ + Na2 + SO4 2-
Также щёлочи взаимодействуют с растворами солей аммония.
Таким образом, получаем 2 схемы взаимодействия солей металлов, которым соответствуют амфотерные гидроксиды, с щелочами:
соль амф.металла(избыток) + щёлочь = амфотерный гидроксид↓ + соль
соль амф.металла + щёлочь(избыток) = комплексная соль + соль
5. Щёлочи взаимодействуют с кислыми солями. При этом образуются средние соли, либо менее кислые соли.
кислая соль + щёлочь = средняя соль + вода
Свойства кислых солей очень удобно определять, разбивая мысленно кислую соль на 2 вещества — кислоту и соль. Например, гидрокарбонта натрия NaHCO3 мы разбиваем на уольную кислоту H2CO3 и карбонат натрия Na2CO3. Свойства гидрокарбоната в значительной степени определяются свойствами угольной кислоты и свойствами карбоната натрия.
6. Щёлочи взаимодействуют с металлами в растворе и расплаве. При этом протекает окислительно-восстановительная реакция, в растворе образуется комплексная соль и водород, в расплаве — средняя соль и водород.
! Обратите внимание! С щелочами в растворе реагируют только те металлы, у которых оксид с минимальной положительной степенью окисления металла амфотерный!
2Al + 2NaOH + 6 H2 + O = 2Na[ Al +3 (OH)4] + 3 H2 0
7. Щёлочи взаимодействуют с неметалами. При этом протекают окислительно-восстановительные реакции. Как правило, неметаллы диспропорционируют в щелочах. Не реагируют с щелочами кислород, водород, азот, углерод и инертные газы (гелий, неон, аргон и др.):
NaOH +О2 ≠
NaOH +N2 ≠
NaOH +C ≠
Сера, хлор, бром, йод, фосфор и другие неметаллы диспропорционируют в щелочах (т.е. самоокисляются-самовосстанавливаются).
2NaOH +Cl2 0 = NaCl — + NaOCl + + H2O
6NaOH +Cl2 0 = 5NaCl — + NaCl +5 O3 + 3H2O
Кремний окисляется щелочами до степени окисления +4.
2NaOH + Si 0 + H2 + O= Na2Si +4 O3 + 2H2 0
Фтор окисляет щёлочи:
Более подробно про эти реакции можно прочитать в статье Окислительно-восстановительные реакции.
8. Щёлочи не разлагаются при нагревании.
Исключение — гидроксид лития:
2LiOH = Li2O + H2O
Основания. Их свойства и применение (8 класс)
Выбранный для просмотра документ osnovanija.ppt
Описание презентации по отдельным слайдам:
Основания Химия 8 класс Шелехова Л.С. *
Определение оснований Ме(ОН)n КОН Ca(ОН)2 Al(ОН)3 Ba(ОН)2 Гидроксиды KOH K+1 + OH-1 Ba(ОН)2 Ba+2 + 2 OH-1 Основания – вещества, в растворах которых содержатся гидроксильные ионы
Щёлочи Щёлочи — гидроксиды щелочных и щелочноземельных металлов и аммония. К щелочам относят хорошо растворимые в воде основания. При диссоциации щелочи образуют ионы OH− и ион металла. К щелочам относятся гидроксиды металлов подгрупп I-ой и II-ой периодической системы, например NaOH (едкий натр), KOH (едкое кали), Ba(OH)2. Едкие щёлочи — тривиальное название гидроксидов лития LiOH, натрия NaOH, калия КОН, рубидия RbOH, и цезия CsOH.
Растворимость Растворимые в воде Нерастворимые в воде Щелочи Металлы I А и II А групп КОН NaOH Ca(ОН)2 LiOH Fe(OH)3 Cu(OH)2 Al(ОН)3 Металлы III А и Б групп
Классификация оснований В зависимости от того, является ли соответствующий оксид основным, кислотным или амфотерным, соответственно различают: Основные гидроксиды (основания) — гидроксиды, проявляющие основные свойства (например, гидроксид кальция Ca(ОН)2, гидроксид калия KOH, гидроксид натрия NaOH и др.); Кислотные гидроксиды (кислородосодержащие кислоты) — гидроксиды, проявляющие кислотные свойства (например, азотная кислота HNO3, серная кислота H2SO4, сернистая кислота H2SO3 и др.) Амфотерные гидроксиды, проявляющие в зависимости от условий либо основные, либо кислотные свойства (например, гидроксид алюминия Al(ОН)3, гидроксид цинка Zn(ОН)2).
Сильные и слабые основания
Получение оснований Щелочи 2Na + 2H2O 2NaOH + H2 K2O + H2O 2KOH Активный металл + вода Основной оксид + вода
Нерастворимые в воде основания Реакция обмена = соль + щелочь Косвенный способ CuSO4 +2NaOH Na2SO4 + Cu(OH)2 Zn(NO3)2 +2KOH 2KNO3 + Zn(OH)2 FeCl2 +Ba(OH)2 BaCl2 + Fe(OH)2
Химические свойства оснований Щелочи изменяют окраску индикаторов Лакмус Метиловый оранжевый Фенолфталеиновый Синий Желтый Малиновый
Свойства оснований Растворимые (щелочи) Нерастворимые Реагируют с кислотами При умеренном нагревании не разлагаются Разъедают многие органические вещества Реагируют с растворами солей Реагируют с кислотными оксидами Действуют на индикаторы Реагируют с жирами с образованием мыла. Реагируют с кислотами При нагревании разлагаются На большенство органических веществ не действуют Реакции с растворами солей нехарактерны Реакции с кислотными оксидами нехарактерны
Фенолфталеиновый в щелочах малиновый Индикатор фиксирует наличие ионов ОН- в растворе щелочи рН 7
Основания реагируют с кислотами Нейтрализация щелочи нерастворимые основание соль кислота вода
Индикатор Изменение рН среды
Щелочи реагируют с кислотными оксидами
6NaOH + P2O5 2Na3PO4 + 3H2O Н3 PO4 Н2 CO3 Щелочь Кислотный оксид + Вода Соль + Нейтрализация
Нерастворимые основания при нагревании разлагаются 2Fe(OH)3 Fe2O3 + 3H2O Гидроксид Оксид металла Вода +
Физические свойства щелочей Гидроксиды щелочных металлов (едкие щёлочи) представляют собой твердые, белые, очень гигроскопичные вещества. Щёлочи — сильные основания, очень хорошо растворимые в воде, причём реакция сопровождается значительным тепловыделением. Сила основания и растворимость в воде возрастает с увеличением радиуса катиона в каждой группе периодической системы. Кроме того, едкие щёлочи растворимы в этаноле и метаноле.
Как вы думаете, имеют ли основания практическое значение? Конечно же, да.
2) Гидроксид калия. Называют «едкое кали» по аналогии с гидроксидом натрия. Используется при «варке» тугоплавкого стекла, производстве бумаги, жидкого мыла. 3) Гидроксид бария. Гидроксид бария – «баритовая вода» – применяют для качественного и количественного определения содержания углекислого газа в газах.
4) Гидроксид кальция. В технической литературе и в быту часто встречаются такие названия веществ: «воздушная», или «негашеная известь», «известковое молоко», «известковая вода». Негашеная известь – это оксид кальция, получаемый при обжиге мела; гашеная известь – это гидроксид кальция, получаемый при обработке оксида кальция водой. Этот процесс протекает с большим выделением теплоты. Известковое молоко – суспензия гидроксида кальция в воде, применяемая для побелки потолков, стен, стволов деревьев по весне для защиты от обморожений и вредных насекомых. Оксид кальция можно использовать для простейшей химической грелки: два пакетика, один большой, другой – маленький, из водонепроницаемого и химически стойкого материала. Чтобы грелка заработала, заполняют негашеной известью маленький пакет и добавляют в него немного воды. Потом пакет тщательно закрывают, вставляют в большой и еще раз закупоривают. Грелка готова. Гидроксид кальция входит в состав «бордосской жидкости» в смеси с медным купоросом для борьбы с возбудителями грибковых заболеваний плодовых, овощных и декоративных культур. Применяется для распознавания углекислого газа.
Выбранный для просмотра документ Разработка ОСНОВАНИЯ 8 В КЛ. 3.02. 2011.docx
Цель урока: Ознакомить учащихся с составом, названиями, классификацией, отдельными представителями оснований, физическими и химическими свойствами.
Показывать различия между степенью окисления и зарядами ионов.
Классифицировать и давать название основаниям.
Определять основания по качественным реакциям и действию на индикаторы.
Дать определения: индикаторы, физические свойства, химические свойства, способы получения.
Определять практическое использование оснований в быту, народном хозяйстве.
Распределять вещества по классам веществ.
Общеучебные и предметные умения (анализировать, сравнивать, делать выводы).
Логико – смысловые мышления, памяти, умение осуществлять самостоятельную деятельность на уроке.
Коммуникативные качества личности.
Умение работать коллективно (в парах), оценивать свои возможности и знания.
Средства обучения: наглядные и ТСО.
Формы организации обучения: лекция с элементами беседы, фронтальная, индивидуальная, групповая, самостоятельная работа.
Методы обучения: словесные (беседа, рассказ); наглядные (демонстрация слайдов); практические (самостоятельная работа).
Оборудование: Таблица растворимости, интерактивная доска, слайд – лекция, карточки с заданием на самостоятельную работу.
I Актуализация опорных знаний.
Урок начинается с проверки домашнего задания (устный опрос и работа у доски).
Дайте определение оксидам.
Ответ: Оксиды – это бинарные соединения, одним из элементов которого является кислород.
Назовите виды оксидов и приведите примеры.
Ответ: Основные (СаО, С uO )
Дайте определение основным и кислотным оксидам.
Ответ: Оксиды, которым соответствуют основания, называют основными.
Оксиды, которым соответствуют кислоты, называют кислотными.
Назовите основные способы получения оксидов.
Ответ: 1) при горении простых и сложных веществ; 2) при разложении сложных веществ (а) нерастворимых оснований, б) кислот; в) солей.)
Распределите нижеприведенные вещества по соответствующим столбикам. По какому признаку вы так распределили вещества? Что общего между ними?
На доске написаны вещества и таблица.
Металлы и неметаллы
Учитель вводит учащихся в тему урока, говоря о том, что им сегодня предстоит еще раз убедиться, что химия многолика и задает неожиданный вопрос: чем мыли волосы женщины в Древней Руси? И сам же отвечает: «Раствором золы» (показывает). А рецепт был такой: взять ковш золы, да не простой, а еловой или от подсолнечника, замочить в дубовом ведре ключевой или дождевой водой. Постоит такая смесь сутки, потом ее надо процедить или просто слить верхний слой, развести фильтрат чистой водой, подогреть на камельке в рубленой бане и вымыть косы.
Учитель объясняет, что полученный раствор, мыльный на ощупь – это средство под названием «щелок». А вспомнили о нем потому, что реакция среды раствора щелока такая же, как и растворов веществ, которые мы начинаем изучать.
II Закрепление опорных знаний
2) Дайте определение оснований:
4) А сколько гидроксильных групп присоединяет к себе металл? Для ответа на этот вопрос к формулам, выписанным ранее. ( Металл присоединяет к себе столько групп ОН какова его степень окисления)
5) У нас есть вещества, есть их молекулярные формулы. А как же называется каждое из них? Каждый человек имеет свою фамилию, имени, отчество. Так и химические соединения имеют свое название:
название металла в родительном падеже
(римская цифра, обозначающая числовое значение степени окисления металла) для металлов с переменной ст. ок.
«Соответствие основания – оксид металла»
Правило: степени окисления элемента в оксиде и соответствующем ему гидроксиде равны.
III Практическое применение полученных знаний.
Выполнение самостоятельной работы на закрепление изученного материала.
Учащиеся производят взаимоконтроль. Ответы:
Что такое основания 8 класс
Основаниями или гидроксидами называют соединения металлов с гидроксогруппами ОН (одна или несколько групп ОН на каждый атом металла М, т.е. МОН или М(ОН)n). Гидроксогруппа ОН – это ион, ее заряд равен 1–, валентность I.
Названия оснований
В названии основания два слова: КОН – гидроксид калия. Если металл имеет переменную валентность, то ее указывают римской цифрой в скобках: Сг(ОН)3 – гидроксид хрома(III).
Щелочи – это растворимые в воде основания (LiOH, NaOH, КОН, Ва(ОН)2, Са(ОН)2 ). Щелочи – очень едкие вещества, вызывают ожоги. При работе с ними надо особенно тщательно соблюдать правила техники безопасности, надевать очки и перчатки.
Для распознавания растворов щелочей используют индикаторы.
Индикаторы – это органические красители, изменяющие окраску в зависимости от состава раствора. Так, бесцветный раствор фенолфталеина в растворе щелочи становится малиновым. Фиолетовый раствор лакмуса в растворах щелочей становится синим, а оранжевый раствор метилоранжа приобретает интенсивно желтый цвет.
Нерастворимые основания – это практически нерастворимые в воде вещества, например гидроксид железа(III), гидроксид меди(II), гидроксид магния.
Основные оксиды – это оксиды, которым соответствуют основания. Если элемент образует несколько оксидов, то оксид, соответствующий низшей степени окисления, является основным оксидом. Например, СrО и МnО – основные оксиды.
Формулы основных оксидов можно вывести, вычитая необходимое число молекул воды из формулы основания. Например, для формул основных оксидов Na2O, СаО, Fe2O3:
а) 2NaOH – Н2O = Na2O;
б) Са(ОН)2 – Н2O = СаО;
в) 2Fe(OH)3 – 3Н2O = Fe2O3.
Получение оснований
Растворимые основания получают:
а) реакцией оксидов щелочных и щелочноземельных металлов с водой: ВаО + Н2O = Ва(ОН)2;
б) взаимодействием активных металлов (электроотрицательность которых 1,2 и меньше) с водой: 2 Li + 2Н2O = 2LiOH + Н2 ↑;
в) электролизом водного раствора соли, например хлорида натрия; при пропускании постоянного электрического тока через раствор на катоде выделяется водород, на аноде – хлор, а в растворе остается гидроксид натрия:
2NaCl + 2Н2O →электролиз→ Н2 ↑ + 2NaOH + Cl2 ↑.
Нерастворимые основания получают по реакции обмена растворимых солей со щелочами:
CuCl2 + 2NaOH = Cu(OH)2 ↓ + 2NaCl.
Химические свойства оснований
Нерастворимые основания – довольно неустойчивые соединения. Нагревание (300–400 °С) приводит к потере ими воды. Например, голубой гидроксид меди(II) при нагревании отщепляет воду и превращается в черный оксид меди(II):
Сu(ОН)2 → t → СuО + Н2O.


















