Что такое овр в медицине
Процессы обмена веществ, дыхания, гниения, брожения, фотосинтеза являются окислительно-восстановительными процессами (ОВП). В живых организмах, вследствие наличия многочисленных мембран, направленного транспорта веществ и прохождения различных ОВП между его частями, возникает разность зарядов, называемая биопотенциалами. По своей природе биопотенциалы могут быть диффузными, мембранными и редокс-потенциалами. Мембранный потенциал имеет ионную природу, а редокс-потенциал – электронную природу. Биопотенциалы играют важнейшую роль в направленном транспорте веществ, работе мембранных систем, процессах биосинтеза, выделения и запасания энергии. Выделение и запасание организмом энергии тесно связано с процессами окисления и восстановления. Биопотенциалы являются качественной и количественной характеристикой направления, глубины и интенсивности протекания биохимических процессов. Поэтому регистрация биопотенциалов органов и тканей широко применяется в клинической практике при изучении их деятельности, в частности, при диагностике сердечно-сосудистых заболеваний снимают электрокардиограмму, при измерении биопотенциалов мышц снимают электромиограмму. Регистрация потенциалов мозга – энцефалография – позволяет судить о патологических нарушениях нервной системы. Источником энергии жизнедеятельности клеток служит мембранный потенциал, равный 80 мВ, обусловленный возникновением ионной асимметрии, т.е. неодинаковым распределением по обе стороны мембраны катионов и анионов.
Важными процессами в организмах являются реакции ферментативного окисления веществ-субстратов: углеводов, жиров, аминокислот. В результате этих процессов организмы получают большое количество энергии. Приблизительно 90 % всей потребности взрослого мужчины в энергии покрывается за счет энергии, вырабатываемой в тканях при окислении углеводов и жиров. Остальную часть энергии
10 % дает окислительное расщепление аминокислот.
Все биохимические ОВП, скорость и глубина которых контролируется организмом, протекают под действием ферментов – оксидоредуктаз, которые делятся на кофакторы и коферменты и могут быть и окислителями и восстановителями [1]. Системы с более низким окислительно-восстановительным потенциалом отдают электроны, с высоким – их принимают. Электроны переносятся по дыхательной цепи ферментов постепенно с нарастанием редокс-потенциала. В качестве переносчиков электронов в дыхательную цепь митохондрий входят различные белки, содержащие разнообразные функциональные группы, которые предназначены для переноса электронов. По мере продвижения по цепи от одного интермедиата к другому электроны теряют свободную энергию. На каждую пару электронов, переданных по дыхательной цепи кислороду, синтезируется три молекулы АТФ. Свободная энергия, высвобождающаяся при переносе двух электронов на кислород, составляет 220 кДж/моль.
В течение жизни человек подвергается воздействию различных вредных внешних факторов – плохая экология, неправильное и зачастую некачественное питание, употребление некачественной питьевой воды, стрессовые ситуации, курение, злоупотребление алкоголем, употребление лекарственных препаратов, болезни и многое другое. Все эти факторы способствуют разрушению окислительно-восстановительной системы регуляции организма, в результате чего процессы окисления начинают преобладать над процессами восстановления, защитные силы организма и функции жизненно важных органов человека начинают ослабевать и уже не в состоянии самостоятельно противостоять различного рода заболеваниям. Замедлить преобладание окислительных процессов над восстановительными процессами возможно с помощью антиокислителей (антиоксидантов). Нормализовать баланс окислительно-восстановительной системы регуляции (с тем, чтобы укрепить защитные силы организма и функции жизненно важных органов человека и позволить организму самостоятельно противостоять различного рода заболеваниям) возможно с помощью антиоксидантов. Чем сильнее антиоксидант, тем более ощутим его противоокислительный эффект. Многочисленные исследования показали, что аскорбиновая кислота является эффективным антиоксидантом, выступая в качестве донора электронов в таких процессах, как гидроксилирование коллагена, биосинтез карнитина и норадреналина, метаболизм тирозина и аминирование гормонов.
Окислительный стресс – основная опасность современности
В организме человека постоянно протекают миллионы различных биохимических превращений. Большинство из них важно для правильного функционирования всей этой сложной системы, но иногда течение некоторых реакций выходит из-под контроля, что может отрицательно сказываться на состоянии клеток и работе организма в целом. Одним из таких явлений может стать окислительный стресс.
Что такое окислительный стресс
Окислительным или оксидативным стрессом называют резкую активизацию окислительных процессов на фоне недостаточного функционирования антиоксидантной системы. Это приводит к накоплению в организме продуктов свободнорадикального окисления, которые обладают весьма высокой активностью и способностью повреждать молекулы жиров, белков, ДНК и др. Это не может пройти для человеческого организма не замеченным, особенно при длительном нарушении баланса между стимуляцией окислительных процессов с образованием свободных радикалов и снижением активности антиоксидантов. Поэтому следствием окислительного стресса становится возникновение и прогрессирование самых различных патологий.
Впервые термин «окислительный стресс» был введен Х. Зисом в 1985 году.
Свободными радикалами называют молекулы или их отдельные части, у которых присутствует на внешней орбите неспаренный электрон. Поскольку такое состояние нестабильно, а в природе все стремится к гармонии, свободные радикалы приобретают чрезвычайную химическую активность и стремятся стабилизироваться за счет присоединения недостающего электрона.
Баланс между концентрацией прооксидантных и антиоксидантных компонентов называется перекисным гомеостазом.
Механизм развития
Наиболее часто окислительный стресс становится следствием образования активных форм кислорода (АФК), хотя существуют и активные формы азота и других элементов. Существенная доля поступающего в организм человека кислорода принимает участие в реакциях митохондриального окисления.
Митохондрии представляют собой органеллы клетки, в которых производится энергия. В них содержатся дыхательные ферменты, которые посредством окислительно-восстановительных реакций расщепляют глюкозу с помощью доставленного посредством гемоглобина кислорода, что называют циклом Кребса.
Во время митохондриального окисления к молекуле кислорода происходит синхронная транспозиция 4-х свободных электронов с последующим образованием 2-х молекул воды или других соединений. Это всегда сопровождается реакциями одноэлектронного восстановления, в результате которых образуются промежуточные продукты восстановления молекулы кислорода, имеющие как радикальную, так и нерадикальную природу. Но во всех случаях они отличаются высокой реакционной способностью, благодаря чему они и были названы активными формами кислорода. К их числу относятся:
Таким образом, АФК могут взаимно превращаться друг в друга и образуются в ходе одноэлектронного восстановления молекулярного кислорода после митохондриального окисления. Но их количество напрямую зависит от содержания кислорода в клетке. Образование АФК может осуществляться различными путями, в том числе:
Каждый из перечисленных ферментов отвечает за протекание процессов окисления в определенных органах и тканях, что и обуславливает характер возникающих при окислительном стрессе последствий.
Но все клетки имеют специализированные системы для трансформации АФК в не столь реакционноспособные соединения. Тем не менее их активность может снижаться на фоне:
Эти и ряд других факторов приводят к активизации окислительных процессов и подавлению антиоксидантной системы, что провоцирует повышенное образование активных форм кислорода, которые и оказывают разрушающее действие на клетки и в частности ДНК. Это становится причиной развития ряда патологических изменений и в конечном итоге заболеваний.
Наиболее велика роль оксидативного стресса в развитии сердечно-сосудистых и нейродегенеративных заболеваний, в особенности ишемической болезни сердца, атеросклероза, ишемических изменений в головном мозге, болезней Альцгеймера и Паркинсона. Также доказано, что окислительный стресс провоцирует инфекционные, онкологические заболевания и сахарный диабет. Все эти заболевания становятся причиной смерти миллионов людей ежегодно, что требует серьезного отношения к проблеме развития окислительного стресса и поиску вариантов ее решения.
Тем не менее нельзя рассматривать процесс образования АФК только с отрицательной стороны. Они важны для организма, поскольку принимают участие в регуляции апоптоза (необходимой клеточной гибели, обеспечивающей поддержание постоянства количества клеток и избегания их неконтролируемого деления) и клеточной адаптации. Поэтому опасным стоит считать только дисбаланс между образующимися АФК и другими высоко реакционноспособными соединениями и антиоксидантами, т. е. непосредственно окислительный стресс.
Возможные последствия
Под воздействием свободных радикалов могут повреждаться белки, нуклеиновые кислоты, а также происходить разрушение мембранных фосфолипидов и образование межмолекулярных комплексов. Молекулы ДНК в основном мутируют в результате воздействия гидроксид-радикалов и реже под влиянием супероксид-анионов, что приводит к нарушениям в структуре хромосом и может стать причиной развития онкологических заболеваний, генетически обусловленных патологий, передающихся по наследству.
Белки также подвергаются окислительным видоизменениям, в результате чего они теряют свои функциональные возможности и могут трансформироваться в соединения, способные взаимодействовать с другими. Кроме того, при окислительном стрессе существенно активизируются процессы гликозилирования белков, что приводит к повреждению тканей, что характерно для сахарного диабета.
Отражается оксидативный стресс и на структуре липидов, которые являются элементами клеточных мембран. Свободные радикалы провоцируют разрыв их молекулы, что приводит к повышению проницаемости клетки для разных соединений, некоторые из которых могут оказывать гибельное цитотоксическое действие на них. Из клетки вымываются важные микроэлементы, но увеличивается концентрация солей, а также наблюдается снижение внутриклеточного pH.
pH крови является одним из наиболее стабильных показателей для человеческого организма. Венозная кровь содержит углекислоту, подлежащую выведению из организма легкими, и имеет pH – 7,35. В то же время для артериальной крови характерно pH – 7,4. Другие биологические жидкости также имеют свой нормальный уровень pH: для слюны это 6,8—7,4, для мочи – 6—7, для желудочного сока – 1,53—1,67.
Организм стремится поддерживать постоянный кислотно-щелочной баланс всех биологических жидкостей, смещение которого в ту или иную сторону немедленно отражается на самочувствии и состоянии здоровья. Увеличение кислотности называют ацидозом, а сдвиг pH в сторону щелочной реакции – алкалозом. Оба состояния являются опасными для организма и требуют принятия соответствующих мер, но чаще наблюдается смещение pH в кислую сторону, т. е. закисление организма.
Изменение кислотно-щелочного баланса организма приводит к нарушениям протекания нормальных биохимических процессов в клетках и их гибели. В результате возникают изменения в работе внутренних органов. При окислительном стрессе в первую очередь меняется pH мочи и слюны.
Процессы окисления липидов также провоцируют повышение синтеза простагландинов, известных науке в качестве мощных индукторов сокращения или расслабления гладкой мускулатуры стенок сосудов, бронхов, матки, ЖКТ и ряда других физиологических изменений. Их окисление может становиться причиной развития нарушений микроциркуляции, ишемии, глаукомы, катаракты, цирроза.
Таким образом, признаками возникновения окислительного стресса могут выступать:
Окислительный стресс также становится причиной преждевременного старения, ухудшения состояния кожи, волос и ногтей.
Заболевания ЦНС
Окислительный стресс оказывает мощное влияние на состояние головного мозга, поскольку он не только является одним из основных потребителей кислорода в организме, но и во многом состоит из липидов, которые крайне чувствительны к действию свободных радикалов. Под их действием наблюдается нарушение нейроциркуляции, ослабление связей между частями головного мозга, что и приводит к возникновению когнитивных, а также поведенческих расстройств.
Особенно чувствительны к действию оксидативного стресса клетки гиппокампа, миндалин, префронтальной коры и мозжечка.
Сегодня существуют свидетельства, подтверждающие повышение риска развития заболеваний центральной нервной системы, в результате развития окислительного стресса. Его следствием могут стать:
Заболевания сердечно-сосудистой системы
Окислительный стресс крайне негативно сказывается на работе сердечно-сосудистой системы. Существуют убедительные доказательства повреждения свободными радикалами эндотелиальных клеток и развитие на фоне этого нарушений состояния сосудистых стенок.
В результате создаются весомые предпосылки для возникновения атеросклероза, при котором в толще стенок кровеносных сосудов образуются холестериновые бляшки, что приводит к уменьшению просвета сосуда. Вследствие подобных изменений повышается артериальное давление, что становится причиной развития гипертонии, а затем и ишемической болезни сердца, сопровождающейся нарушением движения крови в коронарных сосудах. Результатом их закупорки может стать инфаркт миокарда, для которого характерна выраженная ишемия с последующим некрозом части миокарда. При отсутствии своевременной медицинской помощи инфаркт миокарда способен унести жизнь больного.
Ишемия миокарда развивается, когда потребность сердечной мышц в кислороде превышает его поступление.
Сахарный диабет
Активные формы кислорода способны оказывать отрицательное влияние на состояние β-клеток поджелудочной железы, что сказывается на продукции инсулина. Кроме того, они активизируют процессы гликозилирования белков. В результате не только может ухудшаться течение сахарного диабета с развитием осложнений, но и формироваться предпосылки для его возникновения.
Остеопороз
Остеопорозом называют заболевание, при котором кости теряют свою исходную прочность, становятся более пористыми и в результате более хрупкими. Это резко увеличивает риск получения переломов, в том числе компрессионных переломов позвоночника. Данное заболевание наиболее характерно для лиц пожилого возраста, но мало кто задумывается, что истоки его развития также лежат в окислительном стрессе.
При оксидативном стрессе потребляемые с пищей минералы не успевают доставляться к костям, а используются для решения более неотложных задач – нейтрализации кислот и повышения pH до нормальных показателей. В результате костная ткань, не имея возможности должным образом обновляться, постепенно истончается, разрушаются присутствующие внутри костей костные перегородки, что приводит к увеличению пор и повышению хрупкости кости.
Онкологические заболевания
Повреждение ДНК при окислительном стрессе может становиться причиной нарушения процессов из репликации и транскрипции, что приводит к возникновению мутаций и возможному преобразованию нормальных клеток в злокачественные. При этом напомним, что любой воспалительный процесс сопровождается повышением активности окисления и усиленной продукцией активных форм кислорода. Они могут инициировать процесс синтеза противовоспалительных цитокинов, а также играют значительную роль в активации онкогенов.
Поэтому на фоне длительно текущего воспалительного процесса или окислительного стресса, обусловленного действием других факторов, резко увеличивается риск образования злокачественных клеток, которые не поддаются апоптозу, а напротив, активно делятся и растут. Это приводит к формированию злокачественных опухолей разного типа и степени агрессивности, в том числе способных уносить жизнь человека в течение нескольких лет после образования.
Антиоксиданты, как средства для борьбы с окислительным стрессом
Как уже говорилось, в организме постоянно образуются свободные радикалы и постоянно уничтожаются антиоксидантами. Окислительный стресс – следствие нарушения этого баланса. Таким образом, антиоксиданты являются естественной защитой организма от старения и развития патологических изменений в организме.
Часть антиоксидантов вырабатывается организмом, другие же поступают в него вместе с пищей. Первые представляют собой ферменты или высокомолекулярные белки. Они принимают участие в раскладывании вырабатывающихся внутри клетки свободных радикалов нерадикальным путем или связывают их, чтобы они не смогли нанести ей повреждений. Антиоксиданты, поступающие с пищей, действуют по типу «ловушки». Они отдают свои электроны свободным радикалам, тем самым нейтрализуя их.
Каждый антиоксидант имеет свою локализацию в организме и механизм действия на свободные радикалы. Поэтому один и тот же антиоксидант не способен инактивировать все присутствующие свободные радикалы.
В процессе эволюции сформировалось 2 системы защиты от АФК. Первичная, в состав которой входят как ферментные, так и неферментные антиоксиданты, препятствуют образованию новых радикалов. Элементы вторичной системы захватывают уже сформировавшиеся радикалы и образуют комплекс, который включается в работу при возникновении окислительных повреждений клеточных структур для быстрого их восстановления.
К числу ферментных антиоксидантов принадлежат:
Неферментными антиоксидантами являются:
Таким образом, естественным способом защиты от свободных радикалов является снижение количества потребляемых вредных продуктов, в особенности фастфуда, полуфабрикатов и пр., с увеличением объема съедаемых ежедневно свежих фруктов или овощей. Наибольшее количество антиоксидантов содержится в помидорах, цитрусовых, орехах, винограде, фруктах, ягодах и овощах оранжевого и красного цвета. Полезным будет увеличить количество потребляемой рыбы и других продуктов, богатых на омега-3.
«Живая» вода – сильнейший антиоксидант
«Живой» водой или католитом называют воду, получившую в результате электролиза отрицательный редокс-потенциал и pH в рамках 8,5—10,5. Она не отличается от обычной ни по цвету, ни по запаху, ни по вкусу. Тем не менее отличия все таки есть и заключаются они в окислительно-восстановительном потенциале, а именно в наличии «лишних» электронов у молекул, которые и присоединяются к свободным радикалам, нейтрализуя их.
Таким образом, с точки зрения физики такая вода является восстановителем, а само название «живая» является данью исконно русским традициям. Главным ее достоинством является то, что взаимодействуя со свободными радикалами, она сама не превращается в таковые, становясь полностью нейтральной, а также стимулирует синтез в организме собственных антиоксидантов, усиливает действие имеющихся.
Электролиз – физико-химический процесс, заключающийся в получении под действием электрического тока и специальных электродов или с помощью особых минералов двух разнозаряженных веществ, в нашем случае католита (живой воды с отрицательным потенциалом и щелочной реакцией) и анолита (мертвой воды с положительным потенциалом и высокой кислотностью).
Хотя еще нет систематизированных данных, подтверждающих эффективность живой воды, практика показывает, что она является сильным и при этом многофункциональным антиоксидантом, поскольку не только сама проявляет антиоксидантные свойства, но и многократно усиливает действие ферментных и неферментных антиоксидантов.
Кроме того, что она является прекрасным и целиком безопасным антиоксидантом, живая вода:
В природе также существуют источники «живой» воды, более известные нам в качестве минеральных. Но мало кто знает, что кроме уникального набора солей, они ионизированы, т. е. имею положительный или отрицательный заряд. Это и объясняется тот факт, что ранее люди стремились попасть на воды, чтобы поправить свое здоровье, а сегодня бутилированная минеральная вода не оказывает такого выраженного эффекта. Дело в том, что большинство ионов нейтрализуется в течение двух суток, что делает бутилированную минералку далеко не такой полезной, как вода, выпитая непосредственно из того же источника.
Одновременно с получением живой воды образуется так называемая мертвая вода или анолит. Они также по вкусовым свойствам не отличается от обычной, но имеет положительный окислительно-восстановительный потенциал. Это обеспечивает приобретение ею выраженных бактерицидных свойств, что делает такую воду весьма эффективным средством для лечения различных инфекционных заболеваний, дезинфекции помещений и пр.
Получить живую и мертвую воду можно в домашних условиях с помощью бытовых активаторов или ионизаторов. Процесс занимает 10—40 минут, после чего оба типа воды готовы к употреблению.
Но употреблять живую и мертвую воду нужно правильно. Прежде всего, следует понимать, что в зависимости от способа получения и конкретного прибора она имеет разные окислительно-восстановительные потенциалы. Если они не высоки, такую воду, особенно живую, можно использовать для ежедневного применения. Но вода с высоким отрицательным зарядом должна использоваться короткими курсами, в противном случае она также сможет нанести вред организму. Этим и объясняется тот факт, что одни хвалят живую воду и считают ее панацеей, а другие не заметили никаких изменений в самочувствии. Все дело в правильном подборе величины восстановительного потенциала и дозе.
Профилактика окислительного стресса
Значительно лучше своевременно заботиться о поддержании здоровья в норме, чем затем бороться с последствиями оксидативного стресса. Для этого важно обеспечить организм достаточным поступлением в организм естественных антиоксидантов с пищей, т. е. стараться придерживаться здорового питания с выделением существенной доли в ежедневном рационе свежим фруктам и овощам.
Важно отказаться от курения и злоупотребления алкоголем. Тем не менее красное вино может оказаться полезным в профилактике окислительного стресса, так как содержит биологически активные вещества, которые обладают антиоксидантными свойствами. Поэтому бокал красного вина в день вполне допустим.
Также рекомендуется повысить уровень физической активности, но отказаться от изнурительных тренировок, так как они заставляют организм испытывать гипоксию. При этом не лишним будет периодически контролировать уровень сахара в крови, особенно лицам старше 45 лет. Не стоит забывать и о роле ультрафиолета в развитии окислительного стресса. Поэтому рекомендуется использовать солнцезащитные кремы, причем не только в летнее время, но и в течение года.
Таким образом, с окислительным стрессом сегодня может столкнуться каждый, поскольку вызывающие его факторы крайне распространены и избежать их негативного влияния невозможно. Поэтому каждый, особенно жители мегаполиса, нуждаются в использовании антиоксидантов даже на фоне отсутствия проблем со здоровьем, а при возникновении таковых следует обратиться к врачу и на фоне лечение имеющегося заболевания, обязательно обогатить ежедневный рацион природными источниками антиоксидантов, в качестве которых также может выступать «живая» вода.
Свободнорадикальное окисление и сердечно-сосудистая патология: коррекция антиоксидантами
В основе ведущих метаболических процессов человека лежат окислительно-восстановительные реакции. Среди них особую роль играют свободнорадикальные реакции, при которых в результате метаболических процессов образуются перекисные соединения. Инициатором обр
В основе ведущих метаболических процессов человека лежат окислительно-восстановительные реакции. Среди них особую роль играют свободнорадикальные реакции, при которых в результате метаболических процессов образуются перекисные соединения. Инициатором образования таких соединений обычно являются свободные радикалы — молекулы или фрагменты молекул, имеющие в одном из атомов кислорода неспаренный электрон. Активные формы кислорода чаще всего представлены супероксидным (О2 о ) и гидроксипероксидным (НО2 о ) радикалами.
Одним из основных субстратов для свободнорадикальных реакций служат липиды, в первую очередь молекулы полиненасыщенных жирных кислот (ЖК), липидные компоненты липопротеидов низкой и очень низкой плотности (ЛОНП и ЛНП). В результате окисления ЖК образуются гидроперекиси (диеновые конъюгаты), которые затем метаболизируются во вторичные — малоновый диальдегид (МДА) и третичные продукты перекисного окисления липидов (ПОЛ) — шиффовы основания. Процессы ПОЛ протекают во всех клетках, однако наиболее мощным генератором свободных радикалов служат лейкоциты и тромбоциты, а также гепатоциты [3].
Физиологическая роль свободных радикалов достаточно велика. Большая часть свободных радикалов генерируются фагоцитами, Т-лимфоцитами при воспалительных реакциях и выполняют защитную роль, лизируя патогенные микроорганизмы, мутировавшие (раковые) клетки. Свободнорадикальные процессы лежат в основе синтеза циклических и алифатических гидроперекисей, служащих интермедиаторами ферментативного синтеза простагландинов и лейкотриенов. Важнейшую физиологическую роль выполняет генерируемый в эндотелии сосудов оксид азота NO (эндотелий-зависимый релаксирующий фактор), обеспечивающий расслабление гладкой мускулатуры сосудистой стенки и регулирующий уровень артериального давления, коронарный и органный кровоток, а также предотвращающий агрегацию тромбоцитов.
Сами по себе свободные радикалы, перекиси крайне токсичны. Они окисляют фосфолипиды и белки клеточных мембран, нарушая их целостность, инактивируют клеточные и мембранные ферменты.
В противовес свободнорадикальным процессам в организме существует антиоксидантая система, представленная в первую очередь системой антиоксидантных ферментов: супероксиддимутазой (СОД), связывающей активные формы кислорода с образованием перекиси водорода; каталазой, деструктирующей перекиси в липидные гидропероксиды, глютатионпероксидазой (ГПО), редуцирующей липидные гидропероксиды за счет окисления глютатиона, глютатионредуктазой, восстанавливающей глютатион путем окисления НАДФН, последний восстанавливается через цитохромную цепь и систему природных антиоксидантов — α-токоферол, аскорбиновая кислота, флавоноиды.
Таким образом, про- и антиоксидантная системы находятся в состоянии динамического равновесия, что поддерживается определенной организацией плазменных и клеточных липидов, динамической системой обмена мембранных фосфолипидов и холестерина, определяющих исходный уровень жесткости и окисляемости клеточных мембран.
Чрезмерная активация свободнорадикальных процессов влечет за собой целый каскад негативных реакций и патологических процессов, лежащих в основе ряда заболеваний. Среди наиболее изученных на сегодняшний день свободнорадикальных патологий являются атеросклероз, ишемическая болезнь сердца, артериальная гипертония, в развитии которых большое значение приобретает неконтролируемая генерация пероксидов. Исходная активация свободнорадикальных процессов при атеросклерозе обусловлена снижением активности естественных антиоксидантных ферментов и дефицитом природных антиоксидантов, а также наличием дислипидемии, при которой содержащиеся в высокой концентрации в крови атерогенные липиды служат легким субстратом для перекисного окисления.
В последнее время, говоря о механизмах атерогенеза, многие авторы придают большое значение перекисной модификации липопротеидов низкой плотности (ЛНП) — липидно-белковых комплексов, обеспечивающих транспорт холестерина в эндотелиальные клетки. У модифицированных липопротеидов низкой плотности замедляется катаболизм, что становится причиной развития дислипидемии. Они приобретают способность быстрее связываться с эндотелиальными рецепторами и транспортировать в эндотелий больше холестерина. Накопление в эндотелиальных клетках перекисно модифицированных ЛП, в состав которых входит окисленный ХС, а также хемотаксическое действие тромбина и ряда других факторов свертывания, активированных липопероксидами, стимулируют миграцию в эндотелий из кровяного русла моноцитов и захват холестерина. Проникшие через межклеточные пространства макрофаги начинают интенсивно захватывать модифицированные ЛП, при этом модифицированные ЛП захватываются в десятки раз быстрее, чем обычные. Пересыщенные ХС макрофаги превращаются в пенистые клетки, подавляющая часть которых быстро погибает, в результате чего в интиму изливается накопленный ЭХС, НЭХС, кристаллы моногидрата ХС, формируется липидная инфильтрация артериальной стенки. Гибели пенистых клеток способствуют перекиси, нарушающие структурную целостность клеточной и плазматических мембран. Накопившиеся в интиме липопероксиды, ХС, тромбоцитарные и фибробластные факторы роста стимулируют миграцию гладкомышечных клеток из медии с последующей их пролиферацией, что в итоге приводит к формированию атеросклеротической бляшки. Доказательством главенствующей роли перекисно модифицированных ЛНП в развитии атеросклероза служит тот факт, что в экспериментальных работах на культуре клеток in vitro инактивация окисления ЛНП с помощью природных или синтетических антиоксидантов предотвращала миграцию макрофагов в интиму, задерживала формирование атеросклеротической бляшки. Применение антиоксидантов (пробукола) у кроликов линии Watanabe с гиперхолестеринемией также препятствовало развитию атеросклероза, при этом ПОЛ инактивировалось как в гепатоцитах, так и в интиме сосудов. У больных атеросклерозом применение антиоксиданта пробукола предотвращало развитие рестенозов после ангиопластики [3].
При стенокардии активация перекисных процессов обусловлена частыми ангинальными приступами, вызывающими гиперкатехоламинемию, стимулирующую липолиз, в результате которого увеличивается содержание свободных жирных кислот, являющихся доступным субстратом для окисления. При гипоксии (ишемии) миокарда окислительные процессы в митохондриях кардиомиоцитов нарушаются (как бы не доходят до конца), в результате чего накапливаются промежуточные метаболиты цикла Кребса, крайне легко подверженные восстановлению с образованием свободных радикалов и перекисных соединений, угнетающих систему антиоксидантной защиты. В конечном итоге создается парадоксальная ситуация — уменьшение кислорода в клетке приводит к увеличению кислородных радикалов. Развивающаяся после каждого эпизода транзиторной ишемии реперфузия миокарда также сопровождается значительной активацией (в сотни раз) свободнорадикальных процессов и выбросом липопероксидов в кровоток. Выраженная активация процессов свободнорадикального окисления и следующая за ним реакция тканей и систем организма получили название оксидативного стресса.
Активация свободнорадикальных процессов при артериальной гипертензии ведет к уменьшению синтеза эндогенного NO, связывает NO при реакции липидными радикалами, тем самым снижает эндотелий-зависимую вазодилатацию, уменьшает эффективность многих классов гипотензивных препаратов, так как они реализуют свою фармакологическую активность через систему эндогенного NO.
Одна из популярных в настоящее время гипотез старения основана на положении о накоплении клеточных повреждений, вызванных воздействием свободных радикалов, что косвенно подтверждается угасанием активности антиоксидантной системы организма с возрастом.
Как показали клинико-экспериментальные исследования, проведенные за последние 10 лет в этой области, коррекция прооксидантных нарушений в проантиоксидантной системе при атеросклерозе, различных формах ишемической болезни сердца, артериальной гипертонии значительно улучшает клиническое течение нестабильной стенокардии, инфаркта миокарда, артериальной гипертензии, уменьшает прогрессирование атеросклероза.
Основной группой препаратов, способной противостоять оксидативному стрессу, являются антиоксидантные средства, инактивирующие свободные радикалы и препятствующие их образованию, участвующие в восстановлении антиоксидантов, или препараты, обладающие опосредованной антиоксидантной активностью. Последние непосредственно не являются антиоксидантами, но способны либо активировать антиоксидантную систему, либо повышать эффективность природных антиоксидантов, либо препятствовать окислению потенциальных субстратов.
Как указывалось выше, система антиоксидантной защиты имеет несколько «эшелонов обороны» и включает целый комплекс ферментативных систем и природных соединений, позволяющих утилизировать свободные радикалы, предотвратив их негативное воздействие на организм. Однако терапевтическое использование таких соединений на практике для лечения пациентов во многих случаях нереально либо по причине их нестойкости, либо из-за того, что они не усваиваются организмом. Кроме того, некоторые антиоксиданты идеально эффективны в биохимическом плане как утилизаторы пероксидов в экспериментах in vitro, но при парентеральном или пероральном применении вызывают серьезные побочные эффекты, исключающие их применение в клинической практике.
Недостаточная популярность антиоксидантных средств и отсутствие традиций их широкого применения в практической медицине обусловлены рядом причин: недостаточной изученностью этого вопроса, сложностью адекватной оценки состояния параметров перекисного окисления в организме, отсутствием эффективных медикаментозных средств, обладающих антиоксидантной активностью и способных быстро уменьшить последствия оксидативного стресса.
К сожалению, в настоящее время не существует общепринятой классификации антиоксидантных препаратов. Как правило, антиоксиданты разделяют на природные и синтетические. К природным антиоксидантам относятся α-токоферол (витамин Е), β-каротин. Их применение уменьшает риск развития и прогрессирования атеросклероза, несколько снижает высокий уровень липопероксидов в крови больных хроническими формами ИБС, артериальной гипертонии. Однако для достижения эффекта их применение должно быть достаточно долгим (месяцы), в связи с чем указанные средства представляют интерес только в качестве профилактических препаратов.
Определенными антиоксидантными свойствами обладает аскорбиновая кислота. Она способна восстанавливать окисленные α-токоферольные радикалы, возвращая α-токоферолу его антиоксидантные свойства, а также непосредственно связывать супероксидионы и активные радикалы. Однако ее антиоксидантная активность невелика и проявляется лишь в малых концентрациях. В высоких концентрациях она выступает как прооксидант. Указанные свойства аскорбиновой кислоты позволяют использовать ее преимущественно как профилактическое средство.
В последние годы довольно активно стали использоваться в качестве пищевых добавок или в составе витаминных комплексов ионы металлов с переменной валентностью (селен, марганец, медь, цинк), которые входят в состав активных центров ряда природных антиоксидантных ферментов (супероксиддисмутаз) и потому способны существенно увеличивать их активность. Особую значимость использование таких препаратов приобретает в географических зонах с низким содержанием указанных элементов в воде и пище.
К другим природным антиоксидантным соединениям относятся флавоноиды, в большом количестве содержащиеся в виноградных косточках, ягодах черники, листьях гинкго билобы, сухом красном вине. Флавоноиды тормозят свободнорадикальные процессы на уровне инициации, взаимодействуя с активными радикалами. Однако в настоящее время доказана их эффективность только in vitro, убедительных данных о доминирующей антиоксидантной активности флавоноидов in vivo пока не получено.
Определенную антиоксидантную активность имеют SH-содержащие аминокислоты (цистеин, цистин, метионин), при этом SH-группы выступают как конкурирующие с другими субстратами объекты окисления, не дающие свободных радикалов и фактически гасящие цепную реакцию свободнорадикального окисления. SH-содержащие соединения способны пролонгировать продолжительность «жизни» молекулы NO. Однако терапевтическое применение соединений, содержащих SH-группы (глютатион, тиоловая кислота, N-ацетилцистеин), ограничивается из-за невысокой их проницаемости через цитоплазматические мембраны, где они могут являться защитниками от внутриклеточного оксидативного стресса, а также из-за способности активировать перекисные реакции во внеклеточной среде.
Умеренной антиоксидантной активностью обладают женские половые гормоны (эстрадиол, эстрагон, эстриол), чем, вероятно, обусловлена нераспространенность атеросклероза у женщин в детородном возрасте. Описана опосредованная антиоксидантная активность у мелатонина. Однако клиническое использование гормональных средств в качестве антиоксидантов представляется весьма проблематичным.
В последние годы предпринимаются небезуспешные попытки клинического использования коэнзима Q (убихинона) — одного из самых распространенных соединений в клетках бактерий и животных, сходного по химической структуре с α-токоферолом. Однако возможности, которыми обладает коэнзим Q, и целесообразность его применения служат в настоящее время предметом изучения.
Большой интерес представляют в клиническом плане синтетические антиоксиданты или препараты, обладающие антиоксидантной активностью. Наибольшей эффективностью, отсутствием токсичности и минимальными побочными эффектами характеризуются производные 3-оксипиридина — эмоксипин, мексикор. Эмоксипин является, пожалуй, одним из первых синтетических антиоксидантных средств, вошедших в широкую клиническую практику. Опыт применения раствора эмоксипина у больных с острым инфарктом миокарда на фоне традиционной терапии показал, что препарат существенно улучшал клиническое течение болезни, снижал частоту фатальных осложнений, увеличивал выживаемость больных в острый и подострый период инфаркта.
Мексикор, сходный с эмоксипином по механизмам действия, обладает значительно большей антиоксидантной активностью, выпускается в разрешенной к клиническому применению капсулированной (для перорального приема) и водорастворимой инъекционной форме для парентерального введения. Это позволяет использовать препарат в любых фазах инфаркта и при нестабильной стенокардии, а также сохранить преемственность терапии, переходя с инъекционных форм (на острой стадии болезни) на капсулированную форму (в последующий подострый период или период стабилизации).
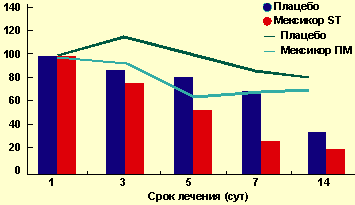
Рандомизированное плацебо-контролируемое исследование мексикора у больных с нестабильной стенокардией показало, что пероральное применение препарата в дозе 6 мг/кг/сут на фоне комплексной традиционной терапии антикоагулянтами, антиагрегантами и антиангинальными средствами, в сравнении с контрольной группой, значительно ускоряло стабилизацию стенокардии, снижало частоту и продолжительность периодов ишемии, а также суммарный интеграл суточного смещения сегмента ST (рисунок 1) и, кроме того, сокращало частоту желудочковых нарушений ритма по результатам холтеровского мониторирования. Указанные изменения сопровождались быстрой нормализацией концентрации продуктов перекисного окисления липидов в крови.
| Рисунок 1. Изменения интеграла смещения ST и отношения болевых/безболевых периодов ишемии у больных нестабильной стенокардией на фоне терапии мексикором. |
 |
Как показали экспериментальные исследования на изолированных сегментах артерий собак, мексикор существенно усиливал вазодилатирующие эффекты нитроглицерина, а при экспериментальной модели окклюзионного инфаркта миокарда у собак повышал объемную скорость коронарного кровотока, сохраняя положительное действие на его фазовую структуру.
Клинические исследования подтверждают способность мексикора увеличивать антиангинальную эффективность пролонгированных нитратов у больных стабильной стенокардией II—III функционального класса: применение мексикора в дозе 0,3-0,4 г/сут. в течение двух месяцев на фоне неизменной дозы пролонгированных нитратов позволило повысить пороговую мощность при велоэргометрическом тесте через один месяц (рисунок 2).
| Рисунок 2. Изменения величины пороговой мощности ВЭМ на фоне терапии мексикором и нитратами больных стабильной стенокардией. |
 |
Открытое рандомизированное исследование инъекционной формы мексикора (6 мг/кг/сут в течение двух недель с последующим переходом на капсулированную форму до одного месяца) у больных острым инфарктом миокарда показало, что мексикор существенно ускорял, в сравнении с контролем, восстановление диастолической функции левого желудочка (оценка производилась по параметрам трансмитрального потока). Мексикор улучшал сегментарную сократимость левого желудочка, ускоряя переход отдельных сегментов миокарда левого желудочка в периинфарктной зоне из состояния акинеза в гипокинез, гипокинеза — в нормокинез (рисунок 3).
| Рисунок 3. Число зон акинезии у больных острым инфарктом на фоне терапии мексикором. |
 |
Мексикор уменьшал частоту и продолжительность эпизодов желудочковых аритмий в острый период инфаркта, а также существенно ускорял нормализацию содержания липопероксидов в крови. Применение мексикора улучшало клиническое течение инфаркта, снижало частоту пролонгированного и рецидивирующего течения болезни, достоверно уменьшало госпитальную и отдаленную (в течение шести месяцев) летальность.
Клиническое использование мексикора в комплексной терапии артериальной гипертонии с кризовым течением позволяет сократить сроки стабилизации давления, уменьшить частоту рецидивирования кризов на постгоспитальном этапе, повысить эффективность гипотензивной терапии.
Преимущество мексикора как средства выбора при лечении острой сердечно-сосудистой патологии, наряду с высокой эффективностью, обусловлено наличием парентеральной формы препарата, применение которой позволяет быстро создать терапевтическую концентрацию и получить клинический эффект.
Определенной опосредованной антиоксидантной активностью обладают некоторые гипохолестеринемические препараты — статины (симвастатин), противоишемический препарат триметазидин, некоторые ингибиторы АПФ, а также β-адреноблокаторы. Механизм действия последних обусловлен ограничением катехоламинемии, снижением интенсивности липолиза и уменьшением содержания в крови легко окисляемых свободных жирных кислот. Однако позитивные антиоксидантные эффекты указанных средств, хотя и позволяют отдать им предпочтение при выборе лекарств у больных с атеросклерозом и артериальной гипертонией, все же являются второстепенными, что следует учитывать при назначении этих лекарственных средств по основным показаниям.
Пробукол долгое время считался перспективным антиоксидантным препаратом, однако отсутствие инъекционной формы, позднее развитие антиоксидантного эффекта (месяцы), наличие осложнений (удлинение интервала QT) не позволили использовать этот препарат достаточно широко.
Следует также помнить, что позитивная фармакодинамика кардиопротективных и противоишемических лекарственных средств (триметазидин, милдронат) лишь в некоторой степени связана с подавлением в ишемизированных тканях свободнорадикальных процессов, все-таки основной точкой приложения этих препаратов является оптимизация клеточного энергетического обмена, уменьшение потребности ишемизированной ткани в кислороде.
Таким образом, имеющийся на сегодняшний день клинический опыт и результаты экспериментальных исследований свидетельствуют о важной роли оксидативного стресса в формировании и прогрессировании сердечно-сосудистой патологии и необходимости его ранней, планомерной и комплексной антиоксидантной коррекции.
Литература
А. П. Голиков, доктор медицинских наук, профессор, академик РАМН
С. А. Бойцов, доктор медицинских наук, профессор
В. П. Михин, доктор медицинских наук, профессор
В. Ю. Полумисков, кандидат медицинских наук, доцент
НИИ СП им. Н. В. Склифосовского, Государственный медицинский центр, Медицинский центр УД Президента РФ (Москва), Курский ГМУ














