Что такое паренхима мозга у новорожденных
Установление причины острой перинатальной гипоксии у детей вызывает большие трудности [1], вследствие которых в детском возрасте в 20-30 % случаев проходят под другими ошибочными диагнозами [3, 4].
Перинатальная гипоксия, повреждая цито-хемо-ангио-архитектонику нервной системы, приводит к полиорганным нарушениям, влияющим на адаптацию организма, степень тяжести и прогноз течения заболевания [1, 2].
Применяемые в клинической практике методы лечения постгипоксических изменений головного мозга у новорожденных, без учета анатомо-физиологических, возрастных особенностей детского организма.
Цель исследования – изучение клинических особенностей последствии постгипоксических изменений головного мозга у новорожденных.
Материалы и методы исследования
Методом ультразвуковой диагностики изучены нейросонографические признаки перинатальной постгипоксической энцефалопатии (ППЭ), выявлены клинические особенности постгипоксических повреждений головного мозга у новорожденных.
Изучены клинические особенности и результаты обследования головного мозга у 240 новорожденных с постгипоксическими повреждениями головного мозга.
Данная патология требует помимо клинико-неврологического обследования, эхоэнцефалографии, нейросонографии, исчерпывающих методик исследования: компьютерной томографии, магнитно-резонансной томографии, электроэнцефалографии, реоэнцефалографии, допплеросонографии, церебральной ангиографии.
В клинической практике используется адаптированная Международная Классификация Болезней X пересмотра, 2000 г.
Всем детям проведен дифференцированный комплекс консервативно-восстановительной терапии, адаптированный к особенностям возраста ребенка и нюансам морфологического субстрата в остром и реабилитационном периодах.
Результаты исследования и их обсуждение
Среди 240 новорожденных по срокам гестации преобладали доношенные дети 132 (55 %), недоношенные дети составили 108 (45 %). Изучение течения беременности выявило в 100 % случаев наличие патологического фактора – в 15 % случаев установлена патология плода: хроническая фетоплацентарная недостаточность, маловодие, в 85 % – патология матери: анемия, острые вирусные заболевания, гипертония, хронические заболевания.
Хроническая гипоксия плода, выявлена у 40 % беременных женщин. Среди новорожденных: 65 % дети (6-8 баллов по шкале Апгар) – в состоянии легкой степени тяжести асфиксии, дети средней степени тяжести и тяжелые составили соответственно 35 %.
Больные поступали в клинику в сроки от 1 часа до 9 суток от начала заболевания. До 60 % больных поступили из непрофильных клиник – обычных инфекционных больниц, после консультации невропатологов. Причиной поздней диагностики, является недостаточная осведомленность врачебного персонала об постгипоксических изменений головного мозга у новорожденных, сложность диагностики и необходимость дифференцировки с целой группой различных состояний.
У большинства детей в кругу семьи родственники страдали разнообразными цереброваскулярными заболеваниями и переносили инсульты головного мозга. У детей старшего возраста отмечались фоновые заболевания неврологического характера с элементами метеозависимости, протекавшие с обширной группой субъективных жалоб, эпизодами транзиторных нарушений мозгового кровообращения в прединсультном периоде.
При нейросонографических исследовании выявлены:
– перивентрикулярные кровоизлияния (ПВК) – 96 (40 %), с дилятацией желудочковой системы (гидроцефалией) – 48 (20 %), с ишемией подкорковых ядер – 24 (10 %);
– диффузные изменения мозговой ткани: отек мозговой паренхимы (36) и перивентрикулярная (субкортикальной) ишемия мозга (70).
Особенностью при УЗИ головного мозга острого периода ППЭ у 240 новорожденных являлось преобладание перивентрикулярной ишемии мозговой ткани (преимущественно у недоношенных новорожденных), с внутрижелудочковыми кровоизлияниями (преимущественно у доношенных новорожденных) и с отеком мозговой ткани (преимущественно у доношенных детей). Перивентрикулярная ишемия мозговой ткани – признак функциональной незрелости мозга [3,4] выявлялась и у недоношенных новорожденных, и у доношенных детей (15 %), что является проявлением нарушения мозгового кровообращения.
Отечность и ишемия мозговой ткани у детей с перенесенной гипоксией головного мозга, впервые появлялась именно в течение нескольких суток жизни.
Этиологическими факторами перинатальных поражений нервной системы у новорожденных явились: асфиксия у 75 % детей, у 10 % – инфекции, 8 % – эндокринные воздействия и 7 % – травма.
В острый период перинатальных поражений нервной системы у новорожденных чаще всего встречались следующие клинические синдромы:
– с повышенной нейрорефлекторной возбудимостью – 70 детей из 206 (34 %),
– в 2 раза реже встречались дети с синдромом общего угнетения – 17,5 %,
– в 7 раз реже – судорожный синдром (4,8 %).
У детей с церебральной ишемией в клинике преобладали синдромы возбуждения ЦНС, признаки внутричерепной гипертензии и угнетения ЦНС.
Среди новорожденных с внутричерепными кровоизлияниями в остром периоде ППЭ преобладали дети с ВЖК 2 степени (перивентрикулярными кровоизлияниями 2-3 степени) с доминированием в клинике признаков внутричерепной гипертензии, в том числе у 30 % пациентов – с развитием гидроцефального синдрома (у недоношенных новорожденных), а у 25 % детей – с симптомами угнетения ЦНС (у доношенных новорожденных).
У 25 % детей с ВЖК 2 степени выявлялся судорожный синдром (только у доношенных новорожденных).
Факт выявления клинических синдромов у части детей с отсутствием ультразвуковой патологии головного мозга во всех периодах перинатальной постгипоксической энцефалопатии (преимущественно в возрасте 1-3 месяца жизни), указывает на наличие нарушений мозговой гемодинамики как у новорожденных, подтвергшихся гипоксии, так и в более позднем возрасте.
При соотношении детей с ПВК различной степени тяжести встречались легкие формы патологии – 55 % детей с ПВК 1-2 степени.
Сочетанные формы патологии (ПВК и ишемии подкорковых ядер, гидроцефалии и ишемии подкорковых ядер) впервые выявлялся у детей 1-3 месяцев жизни (55 %), у 90 (37,5 %) детей – данная патология появлялась в возрасте от 4 до 9 месяцев, реже 18 (7,5 %) – в возрасте 6-30 дней.
Изучение обратного развития нейросонографических признаков ППЭ позволили установить, что компенсация патологии при образовании ее в остром периоде ППЭ (1 мес. жизни) составляет лишь 35 %, в раннем восстановительном периоде (1-3 мес. жизни) увеличивается почти в два раза – 75 %, а в позднем восстановительном периоде (4 мес.-З года жизни) сокращается до 31,4 %. Из 240 новорожденных с различными повреждениями нервной системы у 70 (27,5 %) компенсации патологии в дальнейшем не произошло.
Нейросонография является ценным методом диагностики постгипоксической патологии головного мозга у новорожденных, позволяющим вследствии неинвазивности, отсутствию лучевой нагрузки, возможности многократного исследования (мониторирование), не требуют специальной подготовки пациентов, выявлять сроки появления нейросонографических признаков ППЭ: ПВК, гидроцефалию, ишемические изменения мозговой ткани и подкорковых ядер, отечность мозговой паренхимы и их сочетания.
Профилактика перинатальной энцефалопатии заключается в возможной минимизации факторов риска при беременности, прежде всего в отказе матери от употребления потенциально опасных для ребенка веществ.
При соблюдении этих условий исключить перинатальную энцефалопатию, полностью нельзя. Своевременное лечение гарантирует полное выздоровление 20-30 % детей.
У остальных возможна незначительная мозговая дисфункция, вегето-сосудистая дистония, временная генерализация гидроцефального синдрома. В случае запоздалого диагностирования и лечебных процедур не исключены тяжелые исходы (ДЦП, эпилепсия, стойкое поражение ЦНС и прочие заболевания мозга), требующие очень серьезного долгого и дорогостоящего лечения [5].
Эти данные позволяет неонатологам, невропатологам и педиатрам более точно оценивать динамику постгипоксических изменений головного мозга у новорожденных и детей первых трех лет жизни, компенсаторные возможности и адаптационные резервы детского организма.
Нейросонография — «спасательный круг» неонатологов
По статистике, роды во многих случаях идут с отклонениями от естественного сценария. При таком развитии событий нужно проконтролировать состояние главного органа центральной нервной системы ребёнка — головного мозга. Сделать это можно с помощью эффективной процедуры — нейросонографии (НСГ). О том, что она собой представляет, как проводится и какие результаты даёт, вы узнаете из этой статьи.

Суть процедуры
Нейросонографию называют ультразвуковым исследованием мозга. В ходе этой процедуры врач применяет ультразвук, позволяющий изучить состояние:
Датчик генерирует ультразвуковые волны. Они легко проникают сквозь органы и ткани младенца, не причиняя им ни малейшего вреда, и по-разному отражаются ими. Датчик улавливает отражённые волны, а затем на основе этого отклика программное обеспечение сканера строит изображение. Изучая его, врач делает выводы о состоянии мозговых и других тканей новорождённого и формулирует диагноз.
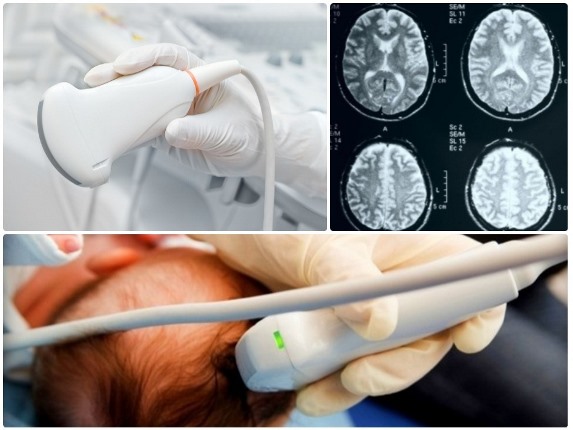
Кости черепа младенца подвижны, что облегчает его прохождение через родовые пути. После родов на головке остаются незакрытые роднички, и именно они позволяют просканировать головной мозг ультразвуком в ходе нейросонографии. В этом случае процедура называется чрезродничковой, и она применима только к новорождённым. Также существует транскраниальная НСГ, выполняемая через черепные кости, доступная взрослым пациентам.
Нейросонография пришла на смену небезопасной магнитно-резонансной томографии (МРТ) и стала настоящим «спасательным кругом» неонатологов.
ВАЖНО! Минздрав России включил НСГ в перечень комплексных обследований, выполняемых в рамках первого скрининга новорождённых в возрасте 1 месяц.
Полная безопасность
Ультразвуковые волны, лежащие в основе нейросонографии, не оказывают никакого влияния на органы и ткани. Вот почему НСГ совершенно безопасна для младенцев и не вызывает у них ни малейших болезненных ощущений.
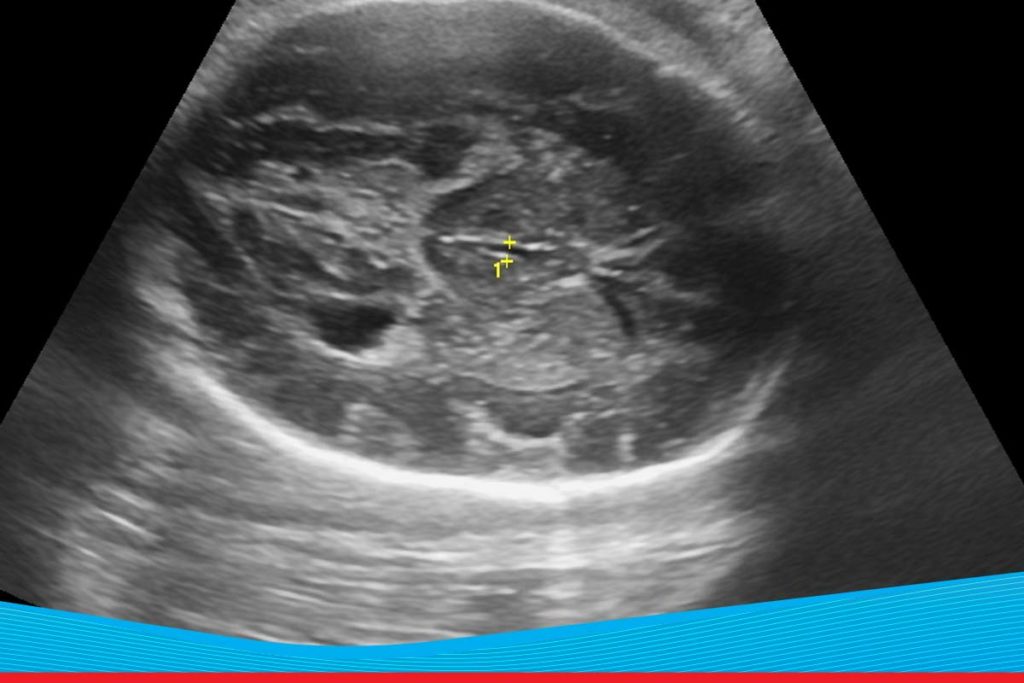
Новорожденные при выполнении нейросонографии часто плачут, что иногда вызывает опасения у мам и побуждает их оставлять на форумах негативные отзывы о процедуре. Для беспокойства нет оснований — плач связан только с присутствием постороннего человека (врача), который настораживает и пугает младенца. Чтобы ребёнок был спокойнее, рекомендуем накормить его перед процедурой.
Техника проведения
Нейросонографияне требует никаких подготовительных мероприятий. Единственное исключение — упомянутое выше кормление.
Врач наносит на участок головы, через который будет проводиться процедура, безопасный для кожи гель. Он исключает появление воздуха между датчиком и головой, улучшает прохождение ультразвуковых волн и повышает точность исследования.

В течение непродолжительного времени (от 7 до 20 минут) врач двигает датчик по голове младенца, проводя исследование в разных срезах. Программное обеспечение сканера анализирует отражённые ультразвуковые волны и создаёт на экране монитора изображение. Врач изучает контуры головного мозга, выполняет необходимые измерения и фиксирует получаемые данные в медицинском протоколе. Собранные сведения позволяют ему сделать вывод об отсутствии патологий или поставить тот или иной диагноз, назначить лечение.
Ни в коем случае не нужно пытаться проанализировать результаты НСГ самостоятельно. Их расшифровка требует глубоких специальных познаний и должна выполняться только врачом. Пожалуй, единственная запись, которую может верно интерпретировать мама или папа малыша — «Патологий не обнаружено».
В каких случаях выполняется НСГ?
Чаще всего нейросонографию назначают младенцам. Есть ряд показаний к выполнению этой процедуры. В их числе:
Есть симптомы, которые должны насторожить и побудить к проведению НСГ даже при отсутствии перечисленных выше показаний. Процедура рекомендована, если:
Если по тем или иным причинам исследование в этом возрасте не проводилось, стоит выполнить его в 3 месяца. Это правило носит рекомендательный характер, окончательное решение принимают родители, однако пропускать срок и отказываться от процедуры не следует — в более старшем возрасте, когда родничок закроется, НСГ станет гораздо менее информативной.
Показатели, указывающие на норму
В первую очередь врач, выполняющий нейросонографию, оценивает форму и размеры полушарий головного мозга. Нормальной считается их симметричность.
В пространстве, расположенном между левым и правым полушарием мозга, не должно быть жидкости.
Борозды и извилины, покрывающие кору мозга, должны быть чётко выраженными.
В мозговых оболочках недопустимы патологические изменения.
Желудочки мозга — полости, содержащие спинномозговую жидкость — должны иметь чёткие границы и не быть расширенными, в них не должно находиться посторонних включений.
Мозговой водопровод на эхограмме в норме практически не различим.
Чётко видны ножки мозга, представляющие собой гипоэхогенные образования.
Хорошо различима пульсирующая базилярная артерия.
Размеры структур мозга должны лежать в определённых диапазонах:
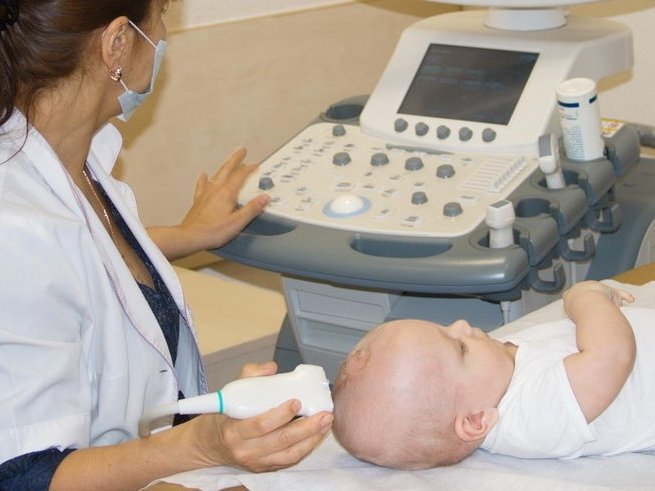
Это — далеко не полный перечень признаков нормальной анатомии головного мозга новорожденного. Врачам известен целый комплекс таких показателей. Кроме того, специалист, выполняющий НСГ, принимает во внимание вес, рост и другие характеристики ребёнка, констатируя нормальность анатомии или ставя диагноз. Именно поэтому родителям не нужно пытаться самостоятельно истолковать результаты ультразвукового исследования — это работа для профессионалов.
Патологии
Значительную долю всех нарушений, диагностируемых при нейросонографии, занимают расстройства гемодинамики (кровообращения). Врач может выявить геморрагическое или ишемическое поражение, которое станет поводом к немедленному медицинскому вмешательству.
Настораживающий признак — патологическое изменение геометрии мозговых структур. Считаются отклонением от нормы асимметрия полушарий головного мозга, сглаженность извилин, неоднородность и асимметричность желудочков, выход размеров мозговых структур из определённых диапазонов.
Является патологией наличие жидкости в области, расположенной между полушариями.
В некоторых случаях при нейросонографии обнаруживаются опухоли, размягчения вещества и кисты.

Так же, как в случае с показателями нормы, выше были перечислены далеко не все признаки патологических отклонений. Их полный комплекс известен врачам, и именно они должны анализировать результаты НСГ. Одни патологии становятся поводом к назначению дополнительных исследований, другие — к немедленному лечению, третьи — к регулярному наблюдению за состоянием здоровья малыша.
Прислушайтесь к мнению врачей и специалистов Минздрава России и не пренебрегайте нейросонографией. Эта безопасная процедура, выполненная своевременно, позволит убедиться в отсутствии патологий, а при их наличии — оперативно принять меры и вернуть ребёнку здоровье.
Что такое паренхима мозга у новорожденных
Нейросонографическое исследование является высокоинформативным скрининговым методом для прижизненной морфологической диагностики поражений головного мозга у новорожденных [1, 2, 4]. Наибольшая диагностическая ценность нейросонографии проявляется в диагностике врожденных пороков ЦНС, внутренней гидроцефалии, перивентрикулярных кровоизлияний, перивентрикулярной лейкомаляции в стадии образования кист [3, 5].
Цель исследования
Изучение информативности нейросонографических и патоморфологических исследований в диагностике менингоэнцефалитов у новорожденных с врожденными пороками развития нервной системы.
Материалы и методы исследования
Проводилось динамическое наблюдение за группой новорожденных (n = 30) с менингоэнцефалитами на фоне врожденных пороков развития нервной системы (далее – ВПР НС). ВПР НС составляют 16,4 % в структуре ВПР. Диагноз менингоэнцефалита, наличие ВПР НС подтверждены результатами динамическим клиническим наблюдением, результатами клинического исследования СМЖ, данными НСГ в динамике. Определены диагностические возможности НСГ и патоморфологического исследования в зависимости от этиологии менингоэнцефалита и характера порока.
Результаты исследования и их обсуждение
Для острого периода менингоэнцефалита у детей с врожденными пороками развития нервной системы (далее – ВПР НС) характерна высокая частота регистрации субарахноидальных уплотнений (84,5 %), локального отека затылочной области (78,2 %), начальной дилатации желудочковой системы мозга (72,7 %), кист и петрификатов (50,9 %), явлений вентрикулита (утолщение, уплотнение стенки желудочка, внутрижелудочковые спайки) (33,6 %). Кисты и петрификаты в 85,7 % случаев выявляются на первой неделе жизни; признаки вентрикулита появляются в среднем на 10,2 + 2,0 день жизни (в том числе в 59,5 % случаев с рождения), преимущественно у доношенных новорожденных с бактериальными и сочетанными менингоэнцефалитами. Признаки диффузного отека паренхимы регистрируются у 21,8 % больных, в 62,3 % случаев с рождения; атрофия паренхимы, перивентрикулярная лейкомаляция появляется в динамике, субэпендимальные и внутрижелудочковые кровоизлияния с рождения и в динамике на 4–7 неделях жизни.
Для больных со спинномозговой грыжей и постнатальным инфицированием мозговых оболочек характерно диффузное повышение эхогенности подкорковых структур, таламуса обоих полушарий, признаки компенсированной и субкомпенсированной гидроцефалии. В динамике развитие гнойно-фибринозного менингоэнцефалита, вентрикулита, гнойного воспаления оболочек спинного мозга сопровождается появлением в полости боковых желудочков множественных шварт, дающих крупноячеистый рисунок, истончением паренхимы полушарий, с диффузным повышением ее эхогенности. Сроки регистрации – 25–30-й день жизни.
Для больных со спинномозговыми грыжами и внутриутробным инфицированием мозговых оболочек характерно выявление в первые дни жизни умеренной или значительной дилатации желудочковой системы мозга, грубой тяжистости. Наблюдается диффузное повышение эхогенности паренхимы обоих полушарий, таламуса и ликвора, утолщение стенок желудочков до 0,6 см. В динамике на 3-й недели жизни в проекции задних рогов и в 3 желудочке визуализируются спайки, повышенная эхогенность и неоднородность ликвора, прогрессирует дилатация желудочковой системы мозга. На 4–5-й неделях жизни увеличивается количество спаек, которые становятся более мощными с мелкими кистовидными структурами.
Наличие врожденной гидроцефалии, осложненной развитием менингоэнцефалита, нейросонографически проявляется дилатацией желудочковой системы мозга, повышением эхогенности паренхимы, фрагментарным уплотнением стенок боковых желудочков, признаками незрелости. С рождения или в динамике регистрируется подчеркнутость борозд и извилин. В динамике характерны уплотнение стенок боковых желудочков, повышенная эхогенность и неоднородность ликвора с формированием спаечного процесса на уровне передних рогов и тел боковых желудочков. Нарастает дилатация желудочковой системы, толщина свободной жидкости в подоболочечном пространстве достигает до 10 мм в сагиттальной плоскости. Желудочковый индекс 50 %.
Нейросонографическая картина больных с менингоэнцефалитом на фоне гидранэнцефалии выявляет выраженную дилатацию всей желудочковой системы мозга, резкое истончение паренхимы мозга с сохранением срединных стволовых структур, наличием перивентрикулярных очаговых уплотнений, уплотнение и утолщение стенок боковых желудочков до 0,8 см, повышение эхогенности ликвора. В динамике регистрируется нарастание дилатации желудочковой системы на фоне менингоэнцефалита с истончением мозгового плаща, обструкцией ликворных путей.
Для менингоэнцефалита на фоне голопрозэнцефалии характерно равномерное диффузное повышение эхогенности паренхимы и ликвора, частичная визуализация межполушарной перегородки, высокоинтенсивные очаговые и линейные уплотнения в перивентрикулярных отделах, выраженная водянка с дилатацией обоих боковых желудочков с резким истончением мозгового плаща, стенки желудочков волнистые, утолщены. В динамике прогрессирует обструкция ликворных путей, дилатация желудочковой системы мозга, истончение мозгового плаща. Желудочковый индекс 100 %.
У больных с менингоэнцефалитами на фоне врожденных пороков развития сосудистой системы мозга (сосудистая мальформация, кавернозные гемангиомы) при проведении нейросонографического исследования выявляются множественные кистовидные структуры до 3–4 мм в диаметре по всей паренхиме мозга, субэпендимарно, в таламических отделах, начальная дилатация желудочковой системы мозга. В динамике появляются признаки отека паренхимы обоих полушарий, свежих субарахноидальных геморрагий по ходу Сильвиевых борозд, нарастают размеры желудочков, признаки внутричерепной гипертензии. Явления вентрикулита появляются на 1–2-й неделе жизни.
В остром периоде менингоэнцефалитов у детей с грубыми пороками развития нервной системы и оперативным вмешательством регистрируются субарахноидальные уплотнения, локальный отек, начальная дилатация желудочковой системы мозга, петрификаты и кисты. Во всех случаях кисты и петрификаты обнаруживаются с рождения. Характерна высокая частота развития вентрикулита, с появлением нейросонографических признаков на 1–3-й день жизни. Клинически вентрикулит у больных в послеоперационном периоде не диагностируется. Наблюдаются признаки диффузного повышения эхогенности паренхимы, атрофии паренхимы с рождения или в динамике.
Осложненное течение после операции по поводу наложения вентрикулоперитонеального шунта с развитием гнойного базального менингита и вентрикулита нейросонографически проявляется истончением паренхимы мозга, подчеркнутостью борозд и извилин в теменно-височной области, дислокацией ядер гипоталамуса, наличием гиперэхогенных структур в полости желудочков, связанных с сосудистым сплетением. Патологоанатомически выявляется спаечный арахноидит, окклюзионная водянка головного мозга с развитием альтеративно-продуктивного менингоэнцефалита, гнойного базального менингита, гнойно-геморрагического вентрикулита, массивного кровоизлияния в сосудистые сплетения боковых желудочков.
Исход менингоэнцефалита у новорожденных с ВПР НС зависит от характера ВПР, его влияния на осуществление жизненно важных функций организма, проведения оперативного вмешательства, развития послеоперационных осложнений. Для новорожденных с менингоэнцефалитами и ВПР НС характерно преимущественно острое течение заболевания с формированием неврологического дефицита (16,7 %), летальным исходом (83,3 %). Сроки наступления летального исхода колеблются от 2 до 63 дней жизни. В более ранние сроки летальный исход наступает у больных в послеоперационном периоде (1–15 день после оперативного вмешательства), в более поздние сроки (35–63 день жизни) у больных с менингоэнцефалитом на фоне спинномозговой грыжи. Формирование неврологического дефицита происходит у больных с врожденной прогрессирующей гидроцефалией с формированием окклюзии (задержка психомоторного развития, тетрапарез, парез мимической мускулатуры).
В группе пациентов с менингоэнцефалитами и ВПР НС в ЦНС преобладают изменения, характерные для бактериального (36,8 %) и сочетанного (28,4 %) поражения.
Воспалительный процесс в ЦНС и внутренних органах при цитомегаловирусных менингоэнцефалитах на фоне ВПР НС (врожденная гидроцефалия) развивается чаще у доношенных новорожденных. Патоморфологически выявляется преимущественно субэпендимарный энцефалит и серозный менингоэнцефалит, у больных с хроническим течением цитомегаловирусного менингоэнцефалита выраженный перивентрикулярный и субэпендимарный глиоз, спайки в твердой мозговой оболочке.
Поражение ЦНС сочетается с поражением печени у 59,1 % больных, преимущественно в виде межуточного гепатита (54 %); поражением легких интерстициального характера (87 %), поражением сердца (41 %) и почек (68,2 %) межуточного характера. Сочетанное поражение ЦНС и ЖКТ регистрируется у 50 % больных (серозный, десквамативный, атрофический энтероколит).
Септический процесс у детей с цитомегаловирусными менингоэнцефалитами и ВПР НС в большинстве случаев протекает с осложнениями, связанными с текущим воспалительным процессом в ЦНС. Наиболее частым осложнением является развитие генерализованного геморрагического синдрома (кровоизлияния во внутренние органы, надпочечники, ткань головного мозга) (59,1 %). Геморрагический синдром характерен для доношенных новорожденных (76,5 %). Регистрируются субарахноидальные кровоизлияния, кровоизлияния в дупликатуры твердой мозговой оболочки, субдуральные гематомы с локализацией в средней и задней черепных ямках. Как результат перенесенного гипоксического поражения головного мозга отмечаются очаги размягчения в затылочных, височных долях головного мозга до стадии формирования глиального рубца.
Характер вовлечения в патологический процесс ЦНС у больных с бактериальными менингоэнцефалитами на фоне ВПР НС определяется этиологией менингоэнцефалита. У больных со стафилококковым (St. epidermidis) менингоэнцефалитом на фоне сосудистой мальформации головного мозга патологоанатомически регистрируется серозный менингоэнцефалит. У больных с менингоэнцефалитом, вызванным синегнойной палочкой, на фоне множественных кавернозных гемангиом головного мозга, врожденной гидроцефалии выявляется серозный менингоэнцефалит, на фоне спинномозговой грыжи серозно-гнойный менингоэнцефалит, гнойный менингоэнцефалит, гнойно-фибринозный менингоэнцефалит.
По частоте вовлечения в патологический процесс наряду с ЦНС органы и системы распределяются следующим образом: поражение легких (87,5 %), поражение сердца (90,6 %), поражение почек (68,8 %), поражение печени (68,8 %), поражение ЖКТ (46,9 %). Преобладает пневмонический процесс гнойного, деструктивного, абсцедирующего характера (68,4 %), обусловленный преимущественно грамотрицательной флорой. Вовлечение сердца в патологический процесс проявляется миокардитом (межуточный, серозный). Перикардит регистрируется преимущественно у доношенных новорожденных (31,3 %). Преимущественный характер поражения почек – межуточный, гнойно-некротический (93,75 %). Поражение ЖКТ чаще проявляется эрозивно-десквамативным и эрозивно-язвенным энтероколитом (50 %).
Осложнения, связанные с воспалительным процессом в ЦНС, в других органах и системах наблюдаются у большинства больных. Ведущими осложнениями воспалительного процесса синегнойной этиологии на фоне ВПР НС являются: гнойный вентрикулит, гнойное воспаление оболочек спинного мозга у всех больных с менингоэнцефалитом на фоне спинномозговой грыжи. Реже выявляется геморрагический синдром (кровоизлияния в мягкие мозговые оболочки) (50,4 %), преимущественно у недоношенных новорожденных.
У больных со стафилококковым менингоэнцефалитом на фоне ВПР НС характерно развитие лейкомаляции с преимущественной локализацией очагов в перивентрикулярной области. Наблюдается развитие отека и набухания головного мозга, в том числе с вклинением в большое затылочное отверстие, в 46,9 % случаев. Вовлечение в патологический процесс ЦНС у больных с сочетанными менингоэнцефалитами на фоне ВПР НС носит преимущественно гнойный, гнойно-некротический (75,6 %) характер.
Менингоэнцефалит у пациентов со спинномозговой грыжей, вызванный ассоциацией возбудителей (Escherichia spp., Ps. aerug.), соответствует патоморфологической картине гнойного менингоэнцефалита. Менингоэнцефалит у больных с врожденной гидроцефалией является следствием внутриутробного инфицирования токсоплазмой и постнатального инфицирования грамотрицательной флорой. Патоморфологическое исследование выявляет альтернативно-продуктивный менингоэнцефалит с развитием гнойного базального менингита, гнойного вентрикулита. У больных с врожденной гидроцефалией возможно постнатальное инфицирование ассоциацией возбудителей с участием S. epid., Candida albicans, Salm. typhi murium, Ps. aerug. В этих случаях патоморфологически находят серозный и гнойно-некротический менингоэнцефалит, гнойный вентрикулит. Для больных с пороками развития сосудистой системы головного мозга характерно развитие бактериально-грибкового (S. epid., Candida albicans) абсцедирующего менингоэнцефалита, вирусно-бактериального (CMV, Salm. typhi murium) гнойного менингоэнцефалита.
Осложнения, связанные с воспалительным процессом в ЦНС, в других органах и системах наблюдаются у всех больных со спинномозговой грыжей, врожденной гидроцефалией, пороками развития сосудистой системы. Ведущими осложнениями являются: отек и набухание головного мозга, в том числе с вклинением в большое затылочное отверстие (83,9 %), геморрагический синдром (41,9 %), вентрикулит (41 %).
Кровоизлияния во внутренние органы наблюдаются только у доношенных новорожденных, появление кровоизлияний в надпочечники, в мозг и мозговые оболочки не зависит от гестационного возраста. Развитие гнойно-геморрагического вентрикулита боковых желудочков, массивное кровоизлияние в сосудистые сплетения боковых желудочков с прорывом их в полости патогенетически связано с осложненным течением послеоперационного периода после наложения вентрикулоперитонеального шунта больному с окклюзионной гидроцефалией. Перивентрикулярный и субэпендимарный глиоз регистрируется только у глубоконедоношенных новорожденных. Развитие лейкомаляции не характерно для больных с сочетанными менингоэнцефалитами и ВПР НС.
По частоте вовлечения в патологический процесс наряду с ЦНС органы и системы распределяются следующим образом: поражение легких (100 %), поражение сердца (77,4 %), поражение почек (77,4 %), поражение печени (90,3 %), поражение ЖКТ (64,5 %). Преобладает пневмонический процесс гнойного, деструктивного, абсцедирующего характера (77,4 %), обусловленного преимущественно ассоциациями с участием грамотрицательной флоры. Вовлечение сердца в патологический процесс проявляется у большинства больных миокардитом (межуточный, серозный) (96,4 %). Преимущественный характер поражения печени, почек – межуточный. Поражение ЖКТ чаще проявляется серозным энтероколитом (65 %).
Заключение
По результатам нейросонографических исследований установлены признаки менингоэнцефалита у больных с ВПР НС: вентрикулит, прогрессирующая дилатация желудочков с формированием окклюзионной гидроцефалии, атрофия паренхимы мозга, петрификаты, кисты, диффузная или перивентрикулярная гиперэхогенность, субарахноидальные кровоизлияния. Применение нейросонографического исследования увеличивает возможность диагностики явлений вентрикулита. Патоморфологически у новорожденных с менингоэнцефалитом и ВПР НС регистрируются субэпендимарный энцефалит, серозный, гнойный, гнойно-некротический менингоэнцефалит. Частота вовлечения мягких мозговых оболочек в патологический процесс достигает 75,8%.
Рецензенты:
Рычкова О.А., д.м.н., заведующая кафедрой детских болезней лечебного факультета с курсом иммунологии и аллергологии, ГБОУ ВПО «Тюменская государственная медицинская академия» Минздрава России, г. Тюмень;
Мельникова И.Ю., д.м.н., профессор, заведующая кафедрой педиатрии и детской кардиологии, ГБОУ ВПО СЗГМУ им. И.И. Мечникова Минздава России.





