Научная электронная библиотека
Наумова Е. А., Шварц Ю. Г., Семенова О. Н.,
Пирамида доказательности
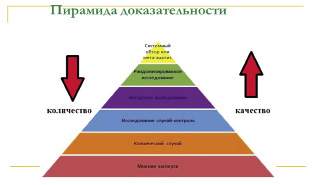
Если различные типы исследований расположить в порядке значимости, для врача и принятия им конкретных клинических решений, то получится условная пирамида, изображенная на рис. 16.
Рис. 16. Пирамида доказательности
Как вы видите, на самой нижней ступени стоят многочисленные мнения экспертов. Возникает вопрос почему? Неужели авторитетные специалисты в своей области не могут дать точный ответ, что и когда необходимо делать практическому врачу? К сожалению, нет. Ни один самый опытный и талантливый клиницист не может иметь достаточного прямого опыта, чтобы свободно ориентироваться во всем многообразии клинических ситуаций. Во-первых, конкретный врач видит лишь определенный или «отобранный» контингент больных, что не позволяет ему распространять свои знания на всех больных, существующих в мире. Но самое главное, ни один врач не видит результаты лечения (особенно отдаленные) всех больных, которых он/она лечит. Ни один врач не может точно знать, сколько и какие из его пациентов жили «долго и счастливо», а у кого развивались осложнения, в том числе и смертельные. Да, есть пациенты, которых один врач в реальной практике может наблюдать достаточно долго, но еще раз подчеркнем, при этом будет много больных, дальнейшая судьба которых ему не известна. Именно поэтому врач не может делать вывод об эффективности какого-либо вида терапии (т. е. ее влияния на выживаемость пациентов), только на основании своей деятельности и своего опыта. Это всегда будет искаженный результат. И именно поэтому на вершине данной пирамиды – рандомизированные исследования, как золотой стандарт изучения влияния вмешательств на конечные точки, и их статистический анализ – мета-анализ.
Что такое пирамида доказательности
Транспаранты и лозунги “За доказательность!” – это хорошо, но сначала нужно понять предмет дискуссии. Для этого необходимо рассказать о методологии простым языком.
Это концепция принятия решений в здравоохранении на всех уровнях: и в организации, и у постели больного. В её основе лежит простое правило – в каждой клинической ситуации решение должно приниматься на основании фактов. И этот факт – не из энциклопедии и инстаграма, а результат синтеза данных лучших рандомизированных исследований. Если нет рандомизированных, то из лучших существующих – сравнительных, наблюдательных и так далее (смотрите иерархию, пирамиду “доказательной медицины”).
Рандомизированное контролируемое исследование (РКИ) – это золотой стандарт медицинского эксперимента. Почему? В РКИ имеется группа исследования и группа контроля, при этом пациенты случайным образом распределяются по группам. Процесс такого распределения называется рандомизацией.
Рандомизация позволяет избежать ситуации, когда одна группа имеет преимущество перед другой. РКИ позволяет минимизировать предвзятость при распределении пациентов по группам. Поэтому и является золотым стандартом исследования. Наличие правильной рандомизации – один из главных признаков качественного исследования.
Даже рандомизированные исследования бывают разного “сорта”. Например, не все рандомизированные исследования двойные слепые, бывают и тройные слепые, бывают и открытые.
Но даже заявленное в названии заслепление не гарантирует качества. Например, неадекватное двойное ослепление, как и его отсутствие в открытых исследованиях, приводят к изменению результата в “нужную” сторону. Такое изменение результата называется “смещением” (англ. – bias). Смещение – это ошибка, возможно и преднамеренная, которая может повлиять на результат исследования.
Многие считают, что качество исследования определяет количество участников. Нет. Качество исследования определяет количество смещений. Чем больше смещений, тем ниже качество. Это и оценивается в систематическом обзоре.
Это формат научной работы, когда анализируются все имеющиеся данные по конкретному клиническому вопросу. Затем, если находятся качественные исследования, происходит их статистический синтез – мета-анализ.
Мета-анализ дает ответ на вопрос – эффективно вмешательство или нет по имеющимся данным. Обычно для этого используются следующие величины – относительный риск и отношение шансов.
Нет, это в первую очередь про качество. Исследователю нужно сделать качественную научную работу, чтобы специалист по доказательной медицине мог включить её в систематический обзор. Если качественных исследований больше одного, можно выполнить мета-анализ.
Информация о том, какого именно качества должны быть работы предварительно описывается в клиническом протоколе. Этот протокол регламентирует проведение систематического обзора, от него нельзя отступать. В протоколе прописано всё: как отбирать исследования, как считать результат, какие смещения учитываются, а какие – нет.
Нет, типов смещений больше. Есть несколько основных показателей качества по Cochrane Handbook:
Генерация распределения – пациенты должны распределиться в группы случайным образом. Для этого должны использоваться адекватные методы, на сегодняшний день это генератор случайных чисел. Хотя подходит и метод подбрасывания монетки, но это – долго и нудно. Особенно для крупных исследований – найдите сумасшедшего, который подбросит монетку 3000 раз.
Сокрытие распределения (“allocation concealment”) – это когда человек, проводящий рандомизацию, не знает, в какую группу распределяется пациент. Скрыть распределение можно даже в открытых исследованиях. Важно, чтобы “распределитель” не сообщил врачам и пациентам о том, кого к какой группе причислили.
Ослепление участников и персонала – важное условие непредвзятости. Ни пациенты, ни врачи не должны знать, чем одни лечат других. Хотя кто-то думает, что такое должно работать и в обычной практике (ROFL).
Ослепление тех, кто оценивает конечные точки (“Blinding of outcome assessment”). Конечная точка – это параметр, по которому оценивают пользу или вред лекарства/вмешательства. Соответственно, важно ослепить “оценщиков” – вы знаете, автооценщики в государственной и частной структуре по-разному оценят вред, нанесенный автомобилю. Тут тоже самое. Поэтому важно быть хладнокровным и беспристрастно оценивать результат, вслепую, как Фемида (нет, лучше).
Выборочная отчетность о результатах (“selective outcome reporting”). Приведем пример этого понятия. Допустим, для оценки нежелательных явлений антидепрессанта описывалась тошнота, рвота и головная боль, но не оценивалась смертность от всех причин. Смертность – важный параметр безопасности, его отсутствие в публикации может говорить о смещении.
Неполные данные о результатах (“incomplete outcome data”). Это чуть сложнее и также требует примера. Если участники с худшими клиническими исходами с большей вероятностью выбывают из-за побочных эффектов, и это происходит в основном в экспериментальной группе, тогда оценка эффекта будет смещена в пользу экспериментального вмешательства.
Другие смещения включают в себя наличие конфликта интересов, потёртость (да, бывают и такие) и т.д. Выбор оцениваемых смещений лежит на авторской группе исследования. Вышеописанные – основные.
Если в исследовании нет ни одного смещения, его качество считают высоким. Если есть точно хотя бы одно – низким. Неудивительно, что доказательств “высокого качества” мало. Но это лишь означает, что надо нормально делать. Тогда и будет нормально!
Влияет. Количество участников позволяет снизить погрешность расчётов при оценке эффекта. Также количество участников позволяет более точно выявить частоту развития нежелательных явлений при применении лекарства/вмешательства.
Идеальная ситуация, когда к качеству приложено количество. Качество + количество = лучший результат. К увеличению количеств участников в исследованиях призывал и Питер Гётше, сооснователь Кокрейн, сообщества, которое разработало современную методику проведения систематических обзоров и сотрудничает с ВОЗ.
Но если смещений много и число пациентов велико – результат может не соответствовать реальности. Смещения могут выявляться на всех уровнях исследования – от организации и до интерпретации результатов. Некачественные исследования могут спонсироваться заинтересованной стороной, и автор исследования в таком случае имеет конфликт интересов. Даже автор систематического обзора.
Это ситуация, когда автор замечен в коммерческих отношениях с компанией или органом, которым нужно получить конкретный результат. Например, доказать эффективность и безопасность своего вмешательства или неэффективность конкурента.
Конфликт интересов тщательно отслеживается в ходе анализа данных при написании систематических обзоров. Хотя есть примеры, когда в систематическом обзоре почти все исследования (34/36) спонсировались фармацевтической промышленностью. А с другой стороны – как иначе? Добывать средства на независимые исследования очень тяжело, даже в Европе и Америке.
Никому. Нужно тщательно проверять качество. Посмотрите ещё раз на пирамиду доказательств – доверие будет относиться к такому параметру, как “мнение”. Самый низ. Только проверка качества и анализ имеющейся информации.
Проводят исследования врачи, главные исследователи должны иметь пятилетний опыт, а медучреждение – соответствующую аккредитацию. Как правило, это представители академической среды – врачи с учеными степенями, работающие на кафедрах. Исполнителей находят компании, занимающиеся организацией клинических исследований. Это могут быть и организации при фармкомпаниях, и независимые от производителей компании, как Worldwide Clinical Trials. Также исследование может быть проведено отдельной группой врачей-исследователей, которые выиграли на это грант. Проведение исследований регламентируется государственным стандартом Р ИСО 14155-2014.
Конечно, если пациент спросит, ответ простой – переложите ответственность, если не знаете. В этом должны разбираться те, кто составляет клинические рекомендации. Вы можете сослаться на них, если не знаете ответа на конкретный вопрос. Вопрос другой, найдётся ли ответ там… Но это совсем другая история и отдельная тема для обсуждения.
Чтобы ответить на вопрос, можно ли считать отечественную медицину доказательной, надо понимать, что здравоохранение – это не производство РКИ. Доказательные данные – результат эксперимента. Как их применять решают авторы клинических рекомендаций. Вы можете найти там и систематические обзоры Кокрейн, и работы других коллективов.
Конечно, не по каждому клиническому вопросу есть РКИ. Но как мы уже говорили, существует иерархия доказательств – она включает в себя уровни доказательности и силу рекомендаций. Чем лучше качество, чем выше сила рекомендации, тем больше уверенности в принимаемом решении.
Клинические рекомендации можно и нужно постоянно улучшать и обновлять. Как именно – решать профессионалам. Этой осенью впервые в российское практике эксперты Кокрейн оценивали российские клинические рекомендации и выделили “проблемные”, по их мнению, пункты.
Резюмируя вышеизложенное.
В общем и целом доказательная медицина – уникальный инструмент для принятия решений. Обычно её противопоставляют гомеопатии и это уже совсем не интересно и не смешно – гомеопатия занимает меньше 1% рынка. Гомеопатия – это просто песчинка хайпа, а народ продолжает его разводить, и разводить, и разводить… (и так 10^19 раз).
Если мы пытаемся бороться доказательствами с гомеопатией, то китайцы решили сделать традиционную медицину… доказательной. Они активно проводят эксперименты с народными методами с прицелом на высокое качество. Стратегия довольно интересная и политически, и экономически обоснованная. Пожелаем успеха исследователям Поднебесной!
Согласитесь, следует использовать доказательную медицину для чего-то действительно важного, а не просто тренироваться в стрельбе из Тополя-М по барбарийским уткам.
Материал подготовил Глеб Краснов
Как сообщалось ранее, в России порядка 20% населения пробовала лечиться гомеопатическими препаратами, многие из них – и другими средствами, отрицаемыми официальной медициной. Большая часть считает свой опыт положительным. Но можно ли считать все лечебные методы равноправными? Ещё сто лет назад об этом можно было подискутировать, но с середины XX века медицина стала наукой. Врач-психотерапевт Николай Колосунин объяснил, как и почему это произошло. Подробнее читайте: «Никакая другая медицина, кроме “доказательной”, сегодня не может называться этим словом».
Что такое пирамида доказательности
ФГБОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России
ФГАОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России; ФГБУ «Центральная клиническая больница с поликлиникой» Управления делами Президента Российской Федерации
Что такое доказательная медицина?
Журнал: Доказательная гастроэнтерология. 2021;10(1): 38-48
Эттингер А.П., Жарова М.Е. Что такое доказательная медицина?. Доказательная гастроэнтерология. 2021;10(1):38-48.
Oettinger AP, Zharova ME. What is evidence-based medicine?. Russian Journal of Evidence-Based Gastroenterology. 2021;10(1):38-48.
https://doi.org/10.17116/dokgastro20211001138
ФГБОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России
Эта публикация открывает собой систематический цикл об основах доказательной медицины, который планируется регулярно публиковать в нашем журнале. Мы надеемся, что он вместе с последующими циклами публикаций на сходные актуальные темы окажет практическую помощь коллегам. Цикл статей мы начинаем с истории становления и развития доказательной медицины, разъяснения основных терминов и понятий, таких как пирамида доказательности, система GRADE и система PICO(T).
ФГБОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России
ФГАОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России; ФГБУ «Центральная клиническая больница с поликлиникой» Управления делами Президента Российской Федерации
Даты принятия в печать:
Обращение к читателю. Зачем нужна доказательная медицина?
Длительный опыт работы в диссертационных советах, в редакционных коллегиях отечественных и зарубежных медицинских изданий, систематическое участие в международных съездах и конференциях позволяют утверждать, что на сегодняшний день у отечественных коллег существуют значительные резервы для понимания и использования принципов и положений, составляющих понятие доказательная медицина. На наш взгляд, главная причина в том, что отстает, в первую очередь, подготовка профессионального сообщества всех уровней к изучению, освоению и, в конечном итоге, восприятие принципов доказательной медицины в качестве полезного набора рабочих инструментов и их свободного использования в повседневной практике.
Причины появления интереса к доказательности в медицине, особенно в нашей стране, кроются в появлении новых требований и в смещении ориентиров оценки деятельности практически любого работника медицинской отрасли. Медицина была и остается научной областью деятельности. Из деклараций это переходит в повседневную жизнь. Отсюда появление повышенного интереса к публикационной активности и связанной с этим понятием потребности изменить собственный подход к планированию и выполнению в первую очередь регулярной исследовательской работы, включая диссертационные работы, клинические исследования и все, что можно отнести к научной деятельности в любом разделе медицины, причем во всех звеньях лечебно-профилактической работы.
Почему в общем виде этим следует интересоваться и почему нужно популяризировать доказательную медицину? Практика руководства отраслью, внезапное появление требований к исполнителям без подготовки мнения профессионального сообщества приводит к неправильным реакциям и замедлению внедрения новшества, поскольку врачи не видят очевидных выгод для себя и расценивают новшества как очередную нагрузку, которая не помогает им, а отвлекает от выполнения основных и понятных обязанностей. Активное или пассивное сопротивление контрпродуктивно. Оценка самого явления как очередной бюрократической причуды только замедляет прогресс. А описанная реакция закономерна в основном по одной простой и давно известной причине — появление новшества, даже самого полезного, никто не готовит. Сначала появляется распоряжение, затем чаще всего командно-нажимным способом заставляют выполнять его и наказывают за несвоевременное и ненадлежащее исполнение.
Публикаций, посвященных доказательной медицине немало, однако ощущается дефицит именно практически направленных руководств и установок, представлено незначительное количество докладов.
Данная публикация открывает собой систематический цикл, который планируется регулярно публиковать в нашем журнале. Мы надеемся, что вместе с последующими циклами публикаций на сходные актуальные темы он окажет практическую помощь коллегам.
История доказательной медицины, основные вехи
В мировой статистике клинических исследований, по данным Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США (Food and Drug Administration, FDA), наша страна занимает устойчивое второе место по абсолютному количеству участников (6875) и по процентному отношению к мировым цифрам участников клинических исследований (5,22%) [1]. Такая статистика, с одной стороны, радует, а с другой стороны, выдвигает требование к повышению общего уровня овладения предметом не только в относительно немногочисленных передовых крупных учреждениях, но и в целом по стране. В принципе упорядочение любой медицинской, особенно врачебной, деятельности имеет в основе доказательность, начиная с доказывания самому себе правильности выбора диагностических, лечебных или профилактических мероприятий в каждодневной практической работе с конкретными пациентами. Это не открытие, пытливость и стремление к прогрессу отличали врачебное сословие со дня его появления. Особенность современного момента состоит в невиданном ранее повышении темпов жизни вообще и сокращении сроков принятия решений в частности, нарастании потоков информации, повсеместном диктате финансов и финансирующих и в спорном по целесообразности, но императивном внесении приемов производственного и торгового менеджмента в отрасль. Все это по современным определениям — вызовы. И противостоять им можно только одним продуктивным способом — осваивая новые технологии, в первую очередь те, которые помогают врачу эффективно, а значит с пользой для пациента и без постоянного стресса и ущерба для себя радостно и с энтузиазмом работать. Освоение принципов доказательной медицины не является панацеей от всех проблем, но опыт отечественных и зарубежных коллег, которые их используют, говорит о том, что это весьма полезный и необходимый навык, реально повышающий квалификацию и самооценку любого коллеги. Хотя в основе самого понятия и совершенствования лежал и лежит исключительно практический замысел.
Терминология — основа успешного освоения любой новой информации, а в случае доказательной медицины это особенно важно. Единая или единообразная, по крайней мере, терминология — необходимый элемент. Наличие значительного, то есть больше двух, количества терминов, обозначающих одно и то же (субъект или явление) приводит к негативному эффекту — практик просто отвергает саму систему, их использующую. Для того чтобы разобраться, что же представляет собой доказательная медицина, следует дать этому термину определение.
Доказательная медицина — это точное и осмысленное использование лучших результатов клинических исследований для принятия решений в оказании помощи конкретному пациенту [2].
Истоки доказательной медицины можно найти и в древней Греции, и в Библии: Книга Давида, Глава 1:1-16. Когда дети Израиля были пленниками в Вавилоне, они должны были есть вавилонскую пищу. Дети Израиля спросили, могут ли они вместо этого придерживаться вегетарианской диеты. Сравнение детей Израиля с вавилонской молодежью показало, что вегетарианская диета была более здоровой [3].
Первое опубликованное контролируемое исследование проведено в 1747 г. Джеймсом Линдом (James Lind) (рис. 1). Будучи корабельным врачом, Дж. Линд столкнулся с распространенным заболеванием среди мореплавателей того времени — цингой. Разделив моряков на шесть групп по 2 человека, он назначил им разное лечение. Первая группа получала кварту сидра ежедневно, другая — двадцать пять капель купороса, третья — шесть ложек уксуса в день, четвертая — половину пинты морской воды, пятая — два апельсина и лимон, шестая — пряную пасту или напиток из ячменной воды. Лечение пятой группы закончилось через шесть дней, когда кончились фрукты, но к этому времени моряки почти полностью выздоровели [3].
Рис. 1. Основные вехи развития доказательной медицины.
Еще один из основоположников экспериментального метода в медицине — Пьер-Шарль Александр Луи (Pierre-Charles Alexandre Louis) (1787—1872), — французский врач, сравнивший эффективность различных видов кровопускания. В его исследовании присутствовали группы сравнения и даже элементы количественного анализа. Подобных исследований было значительно больше, но публикационная активность в те времена была весьма низкой, и об этих исследованиях знало очень небольшое количество людей.
В России в этот период также проводились клинические исследования, например, в 1829—1830 гг. в Санкт-Петербурге М.Е. Дином, который, выявляя лечебную эффективность гомеопатических средств, применял плацебо и слепой метод. В результате доказана несостоятельность гомеопатической концепции и такой вид лечения даже был запрещен в России [3].
Сам термин «доказательная медицина» или evidence-based medicine (EBM) в научных публикациях впервые появился в 1992 г. Гордон Гайят (Gordon Guyatt) использовал этот термин в своей статье для описания нового подхода к обучению медицинской практике, чуть ранее в 1990 г. он упоминал его в своих лекциях в Университете Макмастера (McMaster University, Торонто, Канада) [4].
Однако сама концепция медицины, основанная не на экспертном мнении, а на доказательствах, появилась еще в 1960 г. Все больше врачей и ученых обращали внимание медицинского сообщества на недостатки распространенного в то время способа принятия клинических решений, что подтверждалось, например, «талидомидной трагедией», получившей огромную огласку в средствах массовой информации. В США под влиянием этого трагического события сенатор Эстес Кефовер в 1959 г. начал проводить в Конгрессе слушания об опасениях по поводу практик фармацевтической промышленности, таких как предполагаемая высокая стоимость и неопределенная эффективность многих лекарств, продвигаемых производителями. Только в 1962 г. внесены поправки в закон, по которому все заявки на новые лекарственные препараты должны были продемонстрировать «существенные доказательства» эффективности лекарственного средства, и это помимо демонстрации безопасности, что ознаменовало начало процесса утверждения Управления по санитарному надзору за качеством пищевых продуктов и медикаментов (Food and Drug Administration, FDA) в его современной форме [5].
В начале 60-х годов XX века Сюзанна Флетчер (Suzanne Fletcher) и Роберт Флетчер (Robert Fletcher) активно поддерживали концепцию принятия клинических решений на основе доказательств. Результатом их работы стал учебник «Клиническая эпидемиология: основы» (Clinical Epidemiology: The Essentials), опубликованный в 1982 г. и описывающий научные основы клинической помощи [6].
Элван Файнштейн (Alvan Feinstein), эпидемиолог, математик и ревматолог в серии публикаций в журнале Annals of Internal Medicine (1967 г.) уделил большое внимание роли клинических рассуждений и выявленных предубеждений (bias), а также ввел термин клиническая эпидемиология. Свои принципы он подтвердил на практике. Работая в Нью-Йорке ревматологом, Э. Файнштейн доказал, что установление диагноза ревматическая лихорадка и отличия доброкачественных шумов от патологических основаны больше на клиническом авторитете, а не научных критериях. Позже Э. Файнштейн создал классификацию болезни, что помогло более эффективно лечить пациентов [6].
В 1967 г. под руководством декана университета Джона Эванса (John Evans) и профессора Фрейзера Мастарда (Fraser Mustard) клиническая эпидемиология стала официальным курсом обучения в медицинской школе Университета Макмастера. Возглавил новый курс 32-летний Дэвид Сакетт (David Sackett), который позже многими будет признан одним из основоположников доказательной медицины. На курсе преподавались способы внедрения эпидемиологических и биометрических методов для изучения диагностического и терапевтического процесса с целью улучшения состояния здоровья пациента. В 1981 г., после нескольких лет работы курса клинической эпидемиологии, Д. Сакетт и его коллеги решили поделиться своими разработками и опубликовали серию статей в журнале Canadian Medical Association Journal о «критической оценке» («critical appraisal») — правилах чтения научной литературы [7]. В 1985 г. авторы начали работу над «библией» доказательной медицины — книгой «Клиническая эпидемиология: научная основа для клинической медицины» (Clinical Epidemiology: a Basic Science for Clinical Medicine) [8].
Позже директором курса стал уже известный нам Гордон Гайятт, который вместе со своими коллегами продолжил работу, начатую его предшественниками. Гайятт и его коллеги начали сотрудничать с американскими учеными, сформировав международную рабочую группу по доказательной медицине в 1992 г. В период с 1993 по 2000 г. рабочая группа из Университета Макмастера опубликовала в JAMA методы для широкой аудитории врачей в серии из 25 статей, которые позже были объединены в «Руководство по использованию медицинской литературы» («Users’ Guides to the Medical Literature») [9].
Рассказ о зарождении доказательной медицины будет неполным без упоминания Арчибальда Лемана Кокрана (Archibald Leman Cochrane) — шотланского врача и эпидемиолога. На протяжении всей своей карьеры он боролся с субъективностью (bias) в медицине и являлся ярым сторонником проведения рандомизированных контролируемых исследований (РКИ). Ярким примером его идеологии является тот факт, что даже находясь в тюрьме во время Второй мировой войны, А.Л. Кокрейн провел свое первое испытание на других военнопленных, сравнивая влияние дрожжевого экстракта на гиповитаминоз. Его сострадание к испытуемым, которые были его товарищами и сокамерниками, повлияло на его будущую работу. Позже А.Л. Кокрейн организовал крупное исследование, пытаясь определить влияние туберкулеза и пыли на развитие прогрессирующего легочного фиброза — исследование Rhondda Fach (1948 г.). Некоторые из наиболее ценных уроков, которые он извлек из исследования Rhondda Fach, включали ценность эпидемиологических исследований и угрозу предвзятости (bias) исследования. Позже Арчибальд Кокрейн организовал первое рандомизированное исследование роли аспирина в профилактике сердечно-сосудистых заболеваний. В 1972 г. он выполнил один из первых систематических обзоров. На основании своего опыта в 1972 г. А.Л. Кокрейн опубликовал книгу «Действенность и эффективность: случайные размышления о медицинской службе» («Effectiveness and Efficiency: Random Reflections on Health Services»), в которой обосновывал целесообразность использования РКИ для улучшения качества медицинской помощи. Эта книга также является одной из важнейших для становления доказательной медицины. Дело Арчи Кокрейна продолжили Том Чалмерс, Ян Чалмерс и Мюррей Энкин, организовавшие в 1992 г. «Кокрановское сотрудничество» (Cochrane Collaboration) в Оксфорде при поддержке Национальной службы здравоохранения Великобритании (NHS) [6, 10].
Том Чалмерс расширил работу А.Л. Кокрейна. Он утверждал, что РКИ являются основой иерархии доказательств, кульминацией которой становятся объединенные данные нескольких испытаний. Он добавил, что при обобщении доказательств необходимо учитывать предвзятость публикации, то есть тот факт, что исследования с положительными результатами с большей вероятностью будут опубликованы, чем исследования с отрицательными результатами. Ему приписывают введение метаанализа. Акушер Ян Чалмерс, работая в лагерях палестинских беженцев в 60-х годах XX века, на собственном опыте убедился в опасности подчинения медицинским догмам и в том, что поиск достоверной информации имеет жизненно важное значение. Ян Чалмерс объединился с акушером Мюрреем Энкиным для создания обширной базы данных опубликованных, неопубликованных, текущих и запланированных исследований и метаанализов [6].
Объединив усилия, трое ученых по аналогии Оксфордской базы данных перинатальных исследований в 1993 г. создали сообщество, целью которого является формирование систематических обзоров эффективности различных медицинских вмешательств, важных и полезных для принятия врачебных решений. Назвали сообщество в честь одного из отцов доказательной медицины — Арчибальда Кокрейна, а эмблемой стало схематическое изображение результатов одного из первых систематических обзоров об эффективности короткого курса кортикостероидов, который назначали беременным с высоким риском преждевременных родов; тогда удалось доказать, что таким образом риск смерти новорожденных можно снизить на 30—50% [10].
Процесс совершенствования всех элементов системы доказательной медицины ведется непрерывно, особенно интенсивно с конца 90-х годов прошлого века и по сей день в разных странах мира. Лидирующие позиции в развитии доказательной медицины занял созданный в Университете Оксфорда Центр доказательной медицины (Centre for Evidence-Based Medicine, CEBM). CEBM является частью Департамента первичной медицинской помощи в отделении Оксфордского университета в Наффилде, позиционирует себя как некоммерческая организация, занимающаяся практикой, обучением и распространением высококачественной доказательной медицины для улучшения здравоохранения в повседневной клинической практике. Исследовательский отдел Центра издает руководства по доказательной медицине. В настоящее время изданы два руководства — в 2009 и 2011 г. Это и выдвинуло этот центр на первые позиции в мире по разработке проблем доказательной медицины [11].
Основные термины доказательной медицины
Для лучшего понимания доказательной медицины необходимо разбираться в основных терминах, которые разъяснены ниже.
Зависимая и независимая переменная
Математические инструменты, используемые для количественного контроля любого научного эксперимента, называются зависимыми и независимыми переменными. Для приближения к рассматриваемым проблемам целесообразно адаптировать точные, но общие определения к рассматриваемым типам исследований.
Зависимые переменные — это получаемые в завершенном исследовании результаты.
Независимые переменные — это те новые условия и параметры в количественном выражении, которые вносятся в ходе экспериментального исследования (изменение доз, способов операции, параметров обследования и т.д.).
В общем виде в экспериментальном исследовании для более точного определения величины зависимой переменной, то есть для максимального приближения результатов исследования к истинному положению вещей, исследователи стремятся применять оптимальные сочетания независимых переменных, то есть строить исследование рационально и адекватно поставленным целям.
Независимые переменные — это переменные, значениями которых можно управлять, а зависимые переменные — это переменные, которые можно только измерять или регистрировать.
Зависимая переменная, или переменная ответа, зависит от независимой переменной. Любое изменение в независимой переменной влияет на зависимую переменную. В действительности зависимые переменные — это те значения, которые фактически измеряются исследователем без предположений и сомнений. И это как бы данность.
Разберем на примере, чем же отличаются зависимая и независимая переменные. В эксперименте исследователь изучает влияние дозы препарата А на уровень ферментов печени, в данном случае концентрация препарата А — это независимая переменная, а уровень ферментов печени — зависимая. Или, например, мы хотим узнать, какая из операций, А или Б, имеет меньше осложнений в виде послеоперационного кровотечения, в данном случае тип операции — независимая переменная, а частота развития осложнений — зависимая.
В большинстве научных исследований делается попытка показать связь между двумя переменными — зависимой и независимой, то есть как одна переменная (независимая переменная) влияет на другую (зависимую переменную). Если исследователь может утверждать, что независимая переменная вызывает зависимую переменную, то он сделал самое сильное утверждение в исследовании:
Когда есть большая вероятность того, что другие переменные могут повлиять на результат, исследование имеет низкую внутреннюю достоверность. Хорошие исследования всегда разрабатываются таким образом, чтобы минимизировать вероятность того, что любые переменные, кроме независимой переменной, влияли на зависимую переменную.
Независимая переменная — все то, что применено нами в процессе работы с пациентом или тест-системой. Зависимые переменные — это те результаты, которые получены в ходе работы. Все результаты медицинских и прикладных медико-биологических исследований конкретны.
Экспериментальное и обсервационное исследование
Достаточно давно в науке, и не только биомедицинской, осуществлено разделение на экспериментальные и обсервационные исследования. Их основное отличие состоит в том, что в экспериментальных исследованиях исследователь контролирует большинство переменных, то есть вмешивается в ход исследования. В обсервационном исследовании исследователь только наблюдает и не изменяет ни одну из переменных (табл. 1, 2).
Таблица 1. Сравнение экспериментального и обсервационного исследований
Рандомизированное контролируемое исследование.
Экспериментальное исследование с использованием лабораторных животных