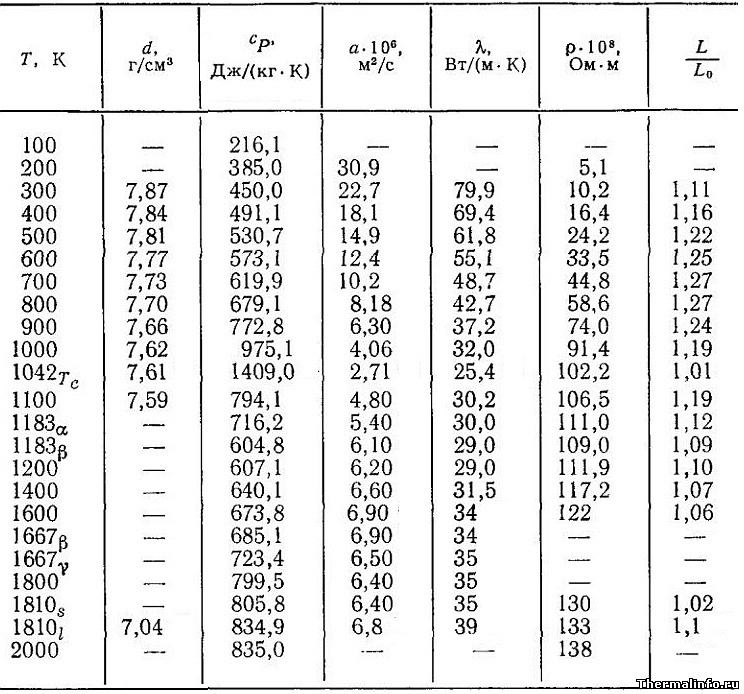
Плотность железа Fe, удельная теплоемкость, теплопроводность и другие его свойства

Свойства железа существенно зависят от температуры: при нагревании этого металла его плотность, теплопроводность и температуропроводность уменьшаются, а значение удельной теплоемкости железа растет.
Плотность железа равна 7870 кг/м 3 при комнатной температуре. При нагревании железа его плотность снижается. Поскольку железо является основным элементом в составе стали, то плотность железа определяет и значение плотности стали. Зависимость плотности железа от температуры слабая — при его нагревании плотность металла снижается и принимает минимальное значение 7040 кг/м 3 при температуре плавления, равной 1810 К или 1537°С.
Удельная теплоемкость железа, по данным таблицы, имеет значение 450 Дж/(кг·град) при температуре 27°С. В зависимости от структуры удельная теплоемкость твердого железа при увеличении температуры изменяется по-разному. По значениям в таблице видны характерный максимум теплоемкости железа вблизи Tc и скачки при структурных переходах и при плавлении.
Теплопроводность железа при комнатной температуре равна 80 Вт/(м·град). С ростом температуры теплопроводность железа снижается — она имеет отрицательный температурный коэффициент в области температуры 100-1042 К, а затем начинает слабо расти. Минимальное значение теплопроводности железа составляет 25,4 Вт/(м·град) вблизи точки Кюри. При β-γ переходе наблюдается слабое изменение теплопроводности, которое также имеет место и при γ-δ переходе.
Теплопроводность железа резко падает по мере увеличения количества примесей, особенно кремния и серы. Наивысшей теплопроводностью обладает очень чистое электролитическое железо — его теплопроводность при 27°С равна 95 Вт/(м·град).
Зависимость коэффициента теплопроводности железа от температуры также определяется степенью чистоты этого металла. Чем железо чище, тем выше его теплопроводность и тем больше по абсолютной величине она снижается с повышением температуры.
Плотность железа
Плотность железа и другие его физические свойства
При температуре ниже 910 o С устойчива структура с объемно-центрированной кристаллической решеткой (a-железо), она обладает ферромагнетизмом. При температуре 769 o С доменная структура разрушается, ферромагнитные свойства исчезают, и железо становится парамагнетиком (b-железо). Этот фазовый переход сопровождается лишь небольшим расширением кристаллической решетки и резким увеличением теплоемкости; существенных изменений кристаллической структуры не происходит. Дальнейшее нагревание до 910 o С приводит к возникновению более плотной модификации (g-железо) с кубической гранецентрированной решеткой.
Рис. 1. Железо. Внешний вид.
Основные константы железа приведены в таблице ниже.
Таблица 1. Физические свойства и плотность железа.
Температура плавления, o С
Температура кипения, o С
Температура Кюри, o С
Тип кристаллической решетки
Распространенность железа в природе
По содержанию в земной коре железо стоит на 4-м месте (4,1%), уступая лишь кислорода, кремнию и алюминию. В земной коре оно главным образом представлено гематитом Fe2O3 (красный железняк), магнетитом Fe3O4 (магнитный железняк), лимонитом Fe2O3×nH2O (бурый железняк), ильменитом FeTiO3 и серосодержащим минералом пиритом FeS2 (железный колчедан). В целом известно более 300 железосодержащих минералов. Значительное количество железа входит в состав различных силикатов и алюмосиликатов, составляющих горные породы.
В свободном виде на Земле встречается железо метеоритного происхождения, часто в виде сплава с никелем. Известно и самородное железо в виде чешуек или мелких листочков, вкрапленных в базальты. Лишь изредка оно образует отдельные куски.
Краткая характеристика химических свойств и плотность железа
При комнатной температуре в компактном виде железо не взаимодействует ни с кислородом, ни с водой, однако во влажном воздухе медленно ржавеет, покрываясь коричневой коркой гидратированного оксида Fe2O3×nH2O – ржавчины. Реакция с перегретым водяным паром приводит к образованию железной окалины Fe3O4, которая при более высокой температуре восстанавливается водородом до оксида FeO.
Железо легко растворяется в разбавленных кислотах: соляной, бромоводородной и иодоводородной:
Очень разбавленную (2-3%) азотную кислоту железо медленно восстанавливает до нитрата аммония.
Холодные концентрированные растворы кислот-окислителей: серной и азотной, а также хромовая смесь пассивируют металл.
Железо устойчиво к действию даже расплавленных щелочей, однако при кипячении порошка металла с концентрированным раствором щелочи в инертной атмосфере образуются синие растворы, из которых кристаллизуются тетрагидроксоферраты (II):
При нагревании железо активно не взаимодействует со многими неметаллами. С хлором оно дает хлорид FeCl3, с серой – сульфид FeS. Взаимодействие железа с бромом для получения трибромидаFeBr3 проводят при температуре 200 o С.
Примеры решения задач
вычислите, сколько теплоты выделится при сжигании 560 г железа.
Согласно уравнению реакции, горению подвергли 3 моль железа. Молярная масса железа равна 56 г/моль. Тогда, теоретическая масса железа будет равна:
m(Fe)th = 3 × 56 = 168 г.
Обозначим, реальное количество теплоты, выделяющееся в ходе описанной выше реакции как «х». Составим пропорцию:
168 г Fe – 1116 кДж теплоты;
569 г Fe – x кДж теплоты.
х = (1116 × 569) / 168 = 3780.
Следовательно, при сжигании 560 г железа выделяется 3780 кДж теплоты.
Fe + S = FeS + 97,2 кДж
Вычислите, какое количество теплоты выделится, если в результате реакции образуется 44 г сульфида железа (II). Напишите в ответе, является ли эта реакция экзо- или эндотермической.
Fe + S = FeS + 97,2 кДж.
Согласно уравнению реакции, образуется 1 моль сульфида железа (II). Молярная масса сульфида железа (II) равна 88 г/моль. Тогда, теоретическая масса сульфида железа (II) будет равна:
m(FeS)th = 1 × 88 = 88 г.
Обозначим, реальное количество теплоты, выделяющееся в ходе описанной выше реакции как «х». Составим пропорцию:
88 г FeS – 97,2 кДж теплоты;
44 г FeS – x кДж теплоты.
х = (97,2 × 44) / 88 = 48,6.
Следовательно, при сжигании железа в атмосфере серы с образованием сульфида железа (II) выделяется 48,6 кДж теплоты.
Копирование материалов с сайта возможно только с разрешения
администрации портала и при наличие активной ссылки на источник.
Плотность железа
Плотность железа.
Плотность железа:
Плотность – скалярная физическая величина, определяемая как отношение массы тела к занимаемому этим телом объёму.
Для обозначения плотности обычно используется греческая буква ρ.
Плотность железа (ρ) составляет:
Необходимо иметь в виду, что плотность металлов может изменяться в зависимости от условий окружающей среды (температуры и давления). Точное значение плотности металлов в зависимости от условий окружающей среды (температуры и давления) необходимо смотреть в справочниках.
Примечание: © Фото https://www.pexels.com, https://pixabay.com

Мировая экономика
Справочники
Востребованные технологии
Поиск технологий
О чём данный сайт?
Настоящий сайт посвящен авторским научным разработкам в области экономики и научной идее осуществления Второй индустриализации России.
Он включает в себя:
– экономику Второй индустриализации России,
– теорию, методологию и инструментарий инновационного развития – осуществления Второй индустриализации России,
– организационный механизм осуществления Второй индустриализации России,
– справочник прорывных технологий.
Мы не продаем товары, технологии и пр. производителей и изобретателей! Необходимо обращаться к ним напрямую!
Мы проводим переговоры с производителями и изобретателями отечественных прорывных технологий и даем рекомендации по их использованию.
О Второй индустриализации
Осуществление Второй индустриализации России базируется на качественно новой научной основе (теории, методологии и инструментарии), разработанной авторами сайта.
Конечным результатом Второй индустриализации России является повышение благосостояния каждого члена общества: рядового человека, предприятия и государства.
Вторая индустриализация России есть совокупность научно-технических и иных инновационных идей, проектов и разработок, имеющих возможность быть широко реализованными в практике хозяйственной деятельности в короткие сроки (3-5 лет), которые обеспечат качественно новое прогрессивное развитие общества в предстоящие 50-75 лет.
Та из стран, которая первой осуществит этот комплексный прорыв – Россия, станет лидером в мировом сообществе и останется недосягаемой для других стран на века.
Показатель плотности железа и другие параметры металла.
Плотность железа является параметром технической характеристики металла. Его значение зависит от влияния ряда факторов, определяющих свойства материала и его сплавов.
Характеристика химических свойств железа
Химический элемент является самым распространенным в земной коре. В чистом виде он обладает серебристо-белым цветом, склонностью к намагничиванию, ковкостью. Самородное железо образует зернистые, чешуйчатые, ленточные агломераты.
Мелкие зерна химически чистого элемента находятся в метаморфических и осадочных горных породах, россыпях, железистых рудах. Сплошные массы рудного материала сосредоточены в базальтах. Железо образует самородки весом до нескольких тонн.
Существуют такие разновидности рудного сырья:
Железо является составной частью метеоритов и подразделяется на камасит и тэнит. Они образуют тесные срастания с никелем и по свойствам близки к теллурическому виду. При содержании в составе природного сплава никеля выше 30% соединение не реагирует на магнит.
Железо обладает высокой химической активностью, склонно к коррозии при высокой влажности и температуре. В дисперсном состоянии самовозгорается и пламенеет в чистом кислороде.
Обычно железом называют его сплавы, в которых содержатся примеси других химических элементов. Они сохраняют пластичность и мягкость чистого железа.
На практике для производства изделий применяются сплавы с содержанием углерода (чугун, сталь). Устойчивость к воздействию внешней среды соединение приобретает при добавлении легирующих компонентов (хрома, марганца, никеля).
Плотность материалов
Группа металлов характеризуется физико-техническими параметрами и свойствами, позволяющими узнать их удельный вес. В производстве металлопроката этот показатель рассчитывается с целью определения соответствия сплавов для производства изделий.
История производства сплавов с изменением их плотности
Как инструментальный материал железо использовалось еще во времена Шумера и Древнего Египта. Археологические артефакты (украшения, кинжал) были изготовлены из метеоритного сплава, содержащего никель и железо.
Небесное происхождение рудного материала отражено в латинском и греческом языках, где его название обозначает «звездный» («сидер»).
Способ получения стали из черного шлиха описан Аристотелем.
В качестве сырья использовались пески, содержащие магнетит. Изготовленная сталь отличалась превосходными качествами благодаря содержанию в ней титана.
С развитием цивилизаций в мире увеличивались потребности в объеме сырья. Промышленные масштабы переработки руды требовали новых технологий выплавки.
Первым шагом металлургического производства было получение сырья путем восстановления его из окиси. В результате процесса выгорания руды в специально оборудованной печи оставался комок пористого металла, который подвергался обработке путем плавления.
В результате многократного сложения вдвое заготовки с последующей ковкой удалось получить отличную сталь, называемую дамасской.
Но в жидком состоянии химический элемент впервые был получен несколько веков назад. Этот факт обусловил возможность насыщать углеродом расплавленный материал с целью придавать ему новые свойства.
Путем непрерывных экспериментов, поисков новых технологий извлечения ценного компонента из руды, формировался новый состав материала, используемого в современном производстве металлопроката, предметов быта и техники.
В основу разработок было положено улучшение технических параметров материала, изменение его плотности и температуры плавления.
Физические характеристики, состав и особенности металла железа
Железо – первый по значимости и распространенности конструкционный материал. Известен он с глубокой древности, а свойства его таковы, что когда железо научились выплавлять в значимом количестве, металл вытеснил все остальные сплавы. Наступил век железа и, судя по области его применения, время это закончится нескоро. Данная статья расскажет вам, какова удельная плотность железа, какая у него температура плавления в чистом виде.
Состав и структура железа
Железо – типичный металл, причем химически активный. Вещество вступает в реакцию при нормальной температуре, а нагрев или повышение влажности значительно увеличивают его реакционноспособность. Железо корродирует на воздухе, горит в атмосфере чистого кислорода, а в виде мелкой пыли способно воспламениться и на воздухе.
Чистому железу присуща ковкость, однако в таком виде металл встречается очень редко. На деле под железом подразумевают сплав с небольшими долями примесей – до 0,8%, которому присущи мягкость и ковкость чистого вещества. Значение для народного хозяйства имеет сплавы с углеродом – сталь, чугун, нержавеющая сталь.
Железу присущ полиморфизм: выделяют целых 4 модификации, отличающиеся структурой и параметрами решетки:
Температура фазовых переходов заметно изменяется при легировании тем же углеродом. Собственно, сама способность железа образовать столько модификаций служит основой обработки стали в разных температурных режимах. Без таких переходов металл не получил бы столь широкого распространения.
Теперь настал черед свойств металла железа.
О структуре железа рассказывает этот видеосюжет:
Свойства и характеристики металла
Железо – достаточно легкий, умеренно тугоплавкий металл, серебристо-серого цвета. Легко реагирует с разбавленными кислотами и поэтому считается элементом средней активности. На воздухе – сухом, металл постепенно покрывается пленкой оксида, которая препятствует дальнейшей реакции.
Но при самой небольшой влажности вместо пленки появляется ржавчина – рыхлая и неоднородная по составу. Ржавчина дальнейшей коррозии железа не препятствует. Однако физические свойства металла, а, главное, его сплавов с углеродом таковы, что, несмотря на низкую коррозийную стойкость, использование железа более чем оправдано.
Далее вы узнаете, чему равна плотность железа (в кг на м3) в сравнении, например, с медью или алюминием.
Масса и плотность

С повышением температуры плотность железа закономерно падает.
А теперь давайте узнаем, какова температура плавления железа по Цельсию, сравнивая ее, например, с медью или чугуном.
Температурный диапазон
Металл относится к умеренно тугоплавким, что означает сравнительно невысокую температуру изменения агрегатного состояния: