Выделение чистых культур микроорганизмов



Чистой культурой называют такую культуру, которая содержит микроорганизмы одного вида. Выделение чистых культур бактерий – обязательный этап бактериологического исследования в лабораторной диагностике инфекционных болезней, в изучении микробной загрязненности различных объектов окружающей среды, и, в целом, при любой работе с микроорганизмами. Исследуемый материал (гной, мокрота, фекалии, кровь и другой материал от больных; вода, почва, воздух, пищевые продукты, трупы животных и человека, переносчики) обычно содержит ассоциации микробов.
Выделение чистой культуры позволяет изучить морфологические, культуральные, биохимические, антигенные и другие признаки, по совокупности которых определяется видовая и типовая принадлежность возбудителя, то есть производится его идентификация.
Для выделения чистых культур микроорганизмов используют методы, которые можно разделить на несколько групп.
1. Метод Пастера – последовательное разведение исследуемого материала в жидкой питательной среде до концентрации одной клетки в объеме (имеет историческое значение).
2. Метод Коха («пластинчатые разводки») – последовательное разведение исследуемого материала в расплавленном агаре (температура 48-50 0 С), с последующим разливом в чашки Петри, где агар застывает. Высевы делают, как правило, из трех-четырех последних разведений, где бактерий становится мало и, в дальнейшем, при росте на чашках Петри появляются изолированные колонии, образующиеся из одной исходной материнской клетки. Из изолированных колоний в глубине агара получают чистую культуру бактерий пересевом на свежие среды.
3. Метод Шукевича – применяется для получения чистой культуры протея и других микроорганизмов обладающих «ползущим» ростом. Посев исследуемого материала производят в конденсационную воду у основания скошенного агара. Подвижные микробы (протей) способны подниматься вверх по скошенному агару, неподвижные формы остаются расти внизу на месте посева. Пересевая верхние края культуры можно получить чистую культуру.
4. Метод Дригальского – широко применяется в бактериологической практике, при этом исследуемый материал разводят в пробирке стерильным физиологическим раствором или бульоном. Одну каплю материала вносят в первую чашку и стерильным стеклянным шпателем распределяют по поверхности среды. Затем этим же шпателем (не прожигая его в пламени горелки) делают такой же посев во второй и третьей чашках. С каждым посевом бактерий на шпателе остается все меньше и меньше и, при посеве на третью чашку, бактерии будут распределяться по поверхности питательной среды отдельно друг от друга. Через 1-7 сут выдерживания чашек в термостате (в зависимости от скорости роста микроорганизмов) на третьей чашке каждая бактерия дает клон клеток, образуя изолированную колонию, которую пересевают на скошенный агар с целью накопления чистой культуры.
5. Метод Вейнберга. Особые трудности возникают при выделении чистых культур облигатных анаэробов. Если контакт с молекулярным кислородом не вызывает сразу же гибели клеток, то посев производят по методу Дригальского, но после этого чашки сразу помещают в анаэростат. Однако чаще пользуются методом разведения. Сущность его заключается в том, что разведения исследуемого материала проводят в расплавленной и охлажденной до 45-50 0 С агаризированной питательной среде. Делают 6-10 последовательных разведений, затем среду в пробирках быстро охлаждают и заливают поверхность слоем смеси парафина и вазелинового масла, чтобы помешать проникновению воздуха в толщу питательной среды. Иногда питательную среду после посева и перемешивания переносят в стерильные трубки Бурри или капиллярные пипетки Пастера, концы которых запаивают. При удачном разведении в пробирках, трубках Бурри, пипетках Пастера вырастают изолированные колонии анаэробов. Чтобы изолированные колонии хорошо были видны, используют осветленные питательные среды. Для извлечения изолированных колоний анаэробов, пробирку слегка нагревают, вращая ее над пламенем, при этом агар, прилегающий к стенкам, плавится и содержимое пробирки в виде агарового столбика выскальзывает в стерильную чашку Петри. Столбик агара разрезают стерильным пинцетом и извлекают колонии петлей. Извлеченные колонии помещают в жидкую среду, благоприятную для развития выделяемых микроорганизмов (например, среду Китта-Тароцци). Агаризированную среду из трубки Бурри выдувают, пропуская газ через ватную пробку.

6. Метод Хангейта – когда хотят получить изолированные колонии бактерий с особенно высокой чувствительностью к кислороду (строгие аэробы) используют метод вращающихся пробирок Хангейта. Для этого расплавленную агаризированную среду засевают бактериями при постоянном токе через пробирку инертного газа, освобожденного от примеси кислорода. Затем пробирку закрывают резиновой пробкой и помещают горизонтально в зажим, вращающий пробирку, среда при этом равномерно распределяется по стенкам пробирки и застывает тонким слоем. Применение тонкого слоя в пробирке, заполненной газовой смесью, позволяет получить изолированные колонии, хорошо видимые невооруженным глазом.
7. Выделение отдельных клеток с помощью микроманипулятора. Микроманипулятор – прибор, позволяющий с помощью специальной микропипетки или микропетли извлекать одну клетку из суспензии. Эту операцию контролируют под микроскопом. На предметном столике микроскопа устанавливают влажную камеру, в которую помещают препарат «висячая капля». В держателях операционных штативов закрепляют микропипетки (микропетли), перемещение которых в поле зрения микроскопа осуществляется с микронной точностью благодаря системе винтов и рычагов. Исследователь, глядя в микроскоп, извлекает отдельные клетки микропипетками и переносит их в пробирки со стерильной жидкой средой для получения клона клеток.
БАКТЕРИОЛОГИЧЕСКИЙ ПОСЕВ (БАКАНАЛИЗ) В ГИНЕКОЛОГИИ И УРОЛОГИИ
Содержание Бакпосев как ценный диагностический инструментЧто показывают мазки и посевыЧем отличаются мужские и женские мазкиПочему необходим баканализОборудование для подготовки и проведения анализа Бакпосев как ценный диагностический инструмент Диагностика при наличии неспецифических симптомов требует особо чувствительных и точных методов. В гинекологии и урологии доктора часто сталкиваются с проявлениями болезни, которые можно трактовать по-разному. Например, это: боль при мочеиспускании или после него;отечность и краснота половых органов, высыпания;воспалительные заболевания мочеполовой системы (уретрит, простатит, везикулит и т.д.);подозрение на любые инфекции (гонорея, микоплазмоз, хламидиоз, трихомониаз и т.д.);бесплодие;профилактическое обследование;выявление инфекции у партнера. Качественный и количественный состав микрофлоры слизистых оболочек является ценным диагностическим материалом. Поэтому значение бактериологического посева в постановке диагноза и мониторинге лечения очень высоко. Что показывают мазки и посевы Посевы и мазки отделяемого разных органов используют гинекологи, урологи, отоларингологи, дерматологи, офтальмологи, хирурги, маммологи. Что касается гинекологии и урологи, то здесь микробиологические исследования незаменимы. У женщин исследуется влагалище и шейка матки, у мужчин — мочеиспускательный (уретральный) канал. Основные виды исследований — общий мазок на флору и обнаружение инфекций. Микроскопия мазка на флору показывает: количество лейкоцитов;наличие бактерий;присутствие внутриклеточных паразитов;наличие и простейших, грибов. В силу анатомических отличий взятие материала для мазка и посева происходит по-разному у мужчин и женщин. Чем отличаются мужские и женские мазки В гинекологии при взятии мазков применяется цитощетка. Это простое приспособление позволяет сделать соскоб нужной глубины со стенок влагалища. Используя гинекологическое зеркало, врач получает пробы с разных участков влагалища. Для взятия мазков у мужчин применяется зонд урогенитальный типа А. Он вводится в мочеиспускательный канал на глубину нескольких сантиметров. Полученный материал помещается на предметное стекло. Теперь его можно исследовать под микроскопом. Окрашенные мазки дают более полную информацию. Например, чтобы дифференцировать флору на грампложительную и грамотрицательную, понадобится набор для окраски мазков по Граму. Азур-Эозин по Романовскому позволяет тщательно прокрасить мазки и увидеть морфологию клеток. Эти и другие химические реактивы представлены в каталоге на сайте Апекслаб https://apexlab.ru/category/ Почему необходим баканализ При всей информативности, мазок не позволяет конкретно определить вид присутствующих бактерий. Например, виды коков (стафилококк, стрептококк) в поле зрения светового микроскопа выглядят одинаково. В норме на слизистых присутствуют сотни видов разных бактерий: лактобактерии;бифидобактерии;бактероиды;пропионибактерии;порфиромонады;превотеллы;пептострептококки;коринеформные бактерии. Для адекватной диагностики требуется выделение чистой культуры микроорганизма при помощи посева. Оборудование для подготовки и проведения анализа Современные методы позволяют определить виды патогенной флоры и их количество. Тампон-зонд с транспорной средой amies с углем позволит не только безопасно взять у пациента пробы, но и в целости доставить их в баклабораторию для посева. Наряду с суперсовременным методом ПЦР не утратили актуальности классические посевы на агаре. Для работы по методике используются: микробактериальная петля (нанесение пробы на питательную среду);пипетка Пастера (дозированный отбор жидкого материала);стеклянная палочка (вспомогательный инструмент при размешивании и взятии проб, окраски мазков). Интерпретация результатов в комплексе с клинической картиной помогает диагностировать дисбиотические нарушения состава микрофлоры, причины воспалительных процессов, появление атипичных микроорганизмов.
Апекслаб, ООО Лабораторное оборудование и материалы
Содержание
Бакпосев как ценный диагностический инструмент
Диагностика при наличии неспецифических симптомов требует особо чувствительных и точных методов. В гинекологии и урологии доктора часто сталкиваются с проявлениями болезни, которые можно трактовать по-разному. Например, это:
Качественный и количественный состав микрофлоры слизистых оболочек является ценным диагностическим материалом. Поэтому значение бактериологического посева в постановке диагноза и мониторинге лечения очень высоко.
Что показывают мазки и посевы
Посевы и мазки отделяемого разных органов используют гинекологи, урологи, отоларингологи, дерматологи, офтальмологи, хирурги, маммологи. Что касается гинекологии и урологи, то здесь микробиологические исследования незаменимы.
У женщин исследуется влагалище и шейка матки, у мужчин — мочеиспускательный (уретральный) канал. Основные виды исследований — общий мазок на флору и обнаружение инфекций.
Микроскопия мазка на флору показывает:
В силу анатомических отличий взятие материала для мазка и посева происходит по-разному у мужчин и женщин.
Чем отличаются мужские и женские мазки
В гинекологии при взятии мазков применяется цитощетка. Это простое приспособление позволяет сделать соскоб нужной глубины со стенок влагалища. Используя гинекологическое зеркало, врач получает пробы с разных участков влагалища.
Для взятия мазков у мужчин применяется зонд урогенитальный типа А. Он вводится в мочеиспускательный канал на глубину нескольких сантиметров.
Полученный материал помещается на предметное стекло. Теперь его можно исследовать под микроскопом. Окрашенные мазки дают более полную информацию. Например, чтобы дифференцировать флору на грампложительную и грамотрицательную, понадобится набор для окраски мазков по Граму. Азур-Эозин по Романовскому позволяет тщательно прокрасить мазки и увидеть морфологию клеток. Эти и другие химические реактивы представлены в каталоге на сайте Апекслаб https://apexlab.ru/category/
Почему необходим баканализ
При всей информативности, мазок не позволяет конкретно определить вид присутствующих бактерий. Например, виды коков (стафилококк, стрептококк) в поле зрения светового микроскопа выглядят одинаково. В норме на слизистых присутствуют сотни видов разных бактерий:
Для адекватной диагностики требуется выделение чистой культуры микроорганизма при помощи посева.
Оборудование для подготовки и проведения анализа
Современные методы позволяют определить виды патогенной флоры и их количество. Тампон-зонд с транспорной средой amies с углем позволит не только безопасно взять у пациента пробы, но и в целости доставить их в баклабораторию для посева.
Наряду с суперсовременным методом ПЦР не утратили актуальности классические посевы на агаре. Для работы по методике используются:
Интерпретация результатов в комплексе с клинической картиной помогает диагностировать дисбиотические нарушения состава микрофлоры, причины воспалительных процессов, появление атипичных микроорганизмов.
Выделение чистых культур бактерий (ЧК)



Iэтап — получение изолированных колоний бактерий из исследуемого материала. При выделении ЧК бактерий из испытуемого материала первоначально необходимо оценить концентрацию бактерий в материале. На I этапе выделения ЧК также осуществляют первоначальную идентификацию бактерий по морфологии и тинкториальным свойствам. Для решения этих задач из исследуемого материала
готовят фиксированный мазок, окрашивают по методу Грама (или другими методами в зависимости от цели исследования) и микроскопируют. Если количество бактерий в поле зрения велико, исследуемый материал разводят в пробирке со стерильным изотоническим раствором хлорида натрия. При малом количестве бактерий в препарате весь объем образца засевают на жидкие среды обогащения с целью увеличения концентрации бактерий. При необходимости выделения определенного вида бактерий посев осуществляют на элективные среды.
Для выделения ЧК бактерий из испытуемого материала необходимо сначала разобщить находящиеся в нем микробы разных видов. Обычно для этого посев материала производят на плотную питательную среду таким образом, чтобы получить изолированные колонии присутствующих в нем бактерий (см. выше). После посева чашку переворачивают дном кверху, подписывают и помещают в термостат при 37 °С на 18—24 ч.
Иногда применяют метод пластинчатых разводок, который заключается в перемешивании различных разведений исследуемого материала с расплавленным и остуженным питательным агаром в колбе или пробирке. После этого агар разливают в чашки Петри и инкубируют в термостате.
Разделение бактерий с использованием физических и химических факторов осуществляют следующим образом. Для выделения спорообразующих бактерий уничтожают неспорообразую-щие, прогревая исследуемый материал при 80 «С в течение 20 мин или подвергают кратковременному кипячению. Споры бактерий при этом сохраняются и при посеве прогретого материала на питательную среду прорастают. Если материал содержал только один вид спорообразующих бактерий, таким образом можно получить ЧК. Если материал содержал споры разных бактерий, дальнейшее выделение осуществляют стандартными методами.
При выделении ЧК психрофильных бактерий используют инкубацию при низких температурах, задерживающих рост сопутствующей микрофлоры. Так, например, для выделения ЧК возбудителя чумы
В ряде случаев ЧК бактерий можно получить путем подавления размножения части микробов в исследуемом материале воздействием на них факторами, к которым выделяемый вид устойчив. С этой целью используют антимикробные препараты, химические вещества и бактериофаги. В питательную среду вносят соответствующее вещество или фаг в строго определенной концентрации, препятствующей размножению сопутствующих бактерий, но не оказывающей выраженного ингибиру-ющего действия на исследуемый микроорганизм.
Кроме упомянутых, в бактериологической практике иногда применяют и другие методы. Например, для выделения чистой
 |
культуры бактерий рода Proteus (Proteus vulgaris) используют его способность к «ползучему» росту (метод Шукевича). При этом бактерии, засеянные в основание скошенного агара, за время культивирования распространяются по всей поверхности агара.
II этап — накопление ЧК для ее дальнейшей идентификации. II этап начинают с оценки результатов первичного посева материала и изучения кулыпуралъных признаков выросших бактерий — особенностей их роста на питательных средах.
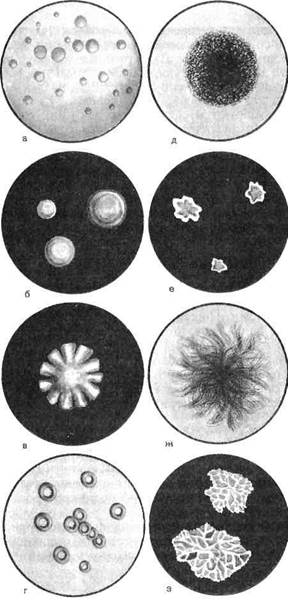
Морфология микробных колоний является наиболее информативным культуральным признаком. Колонии различаются по величине, форме, цвету, консистенции, контуру края, структуре и характеру поверхности (рис. 3.1.1). По величине колонии могут быть крупные (диаметр более 4—5 мм), средние (2—4 мм) и малые (1—2 мм), по форме — круглые, розеткооб-разные, листовидные и т.д. Цвет колонии зависит от выработки определенного пигмента — белого, желтого, красного и др. Колонии непигментирующих бактерий бесцветны. По консистенции различаются сухие, влажные, сочные или слизистые колонии. Поверхность колонии бывает гладкой, морщинистой, исчерченной, плоской, выпуклой, вдавленной. Край колонии может быть ровным, волнистым, бахромчатым. Колонии могут иметь аморфную, зернистую, волокнистую внутреннюю структуру.

При получении микробного газона характер роста бактерий может быть сухим, влажным, «ползучим», складчатым, пигментированным. В жидкой питательной среде одни бактерии дают диффузное помутнение, другие характеризуются придонным или пристеночным ростом; некоторые культуры образуют пленки на поверхности среды, другие — осадок на дне пробирки, что преимущественно определяется потребностью в кислороде.
Для оценки результатов первичного посева исследуемого материала чашки с посевами просматривают и изучают морфологию выросших колоний. Для определения морфологии бактерий и их тинкториальных свойств из материала колоний разных типов готовят мазки, окрашивают по методу Грама и микроскопируют. Необходимо помнить, что родственные бактерии могут отличаться по морфологии колоний и наоборот. Материал из изолированной колонии каждого типа пересевают в отдельные пробирки со скошенным агаром или какой-либо другой питательной средой. Для этого часть колонии снимают петлей, не задевая соседние колонии, и засевают штрихом на скошенную поверхность агара в пробирку. Для выделения и накопления чистой культуры выбирают колонии только тех бактерий, которые присутствовали в исследуемом материале. Появление колоний других бактерий может быть результатом контаминации (загрязнения) посева посторонними микробами
Рис.3.1.1. Типы бактериальных колоний, а — круглые с ровными краями; б — круглые, выпуклые, блестящие, слизистой консистенции; в — с неровными краями; г — круглые с валиком по периферии; Д — зернистые; е — плоские листовидные; ж — ветвистые; з — складчатые.


Особенности культивирования анаэробных бактерий.Все манипуляции со строгими анаэробами должны осуществляться в бескислородных условиях. Для этого используют герметичные настольные камеры с регулируемым газовым составом среды. Посевы производят на специальные обогатительные (элективные) среды для анаэробов (тиогликолевую, Китта—Тароцци). Посевы инкубируют в специальных С02-инкубаторах или в анаэростатах (металлических или пластмассовых контейнерах, герметично закрывающихся крышкой, снабженной патрубками для заполнения газовой смесью нужного состава), которые помещают в обычный термостат. Для инкубации небольших по объему посевов (1—2 чашки Петри) применяют пластиковые пакеты, содержащие химические генераторы газовой смеси, которые обеспечивают полное удаление кислорода из воздушной среды в течение нескольких минут.
8.1. Техника посева и выделения чистых культур микроорганизмов
Доставляемый в лабораторию материал подвергают бактериологическому исследованию в тот же день. Техника посева зависит от характера засеваемого материала, консистенции питательной среды и цели исследования.
Для проведения посевов необходимы: подлежащий исследованию материал, питательные среды, бактериологическая петля, шпатели (стеклянные, металлические), пастеровские и градуированные пипетки, металлические кюветы или поднос для переноса засеянных чашек и металлические коробки для переноса пробирок, ведро или бачок с крышками для сброса отработанного инфицированного материала, спиртовая или газовая горелка.
Жидкий материал для посева берут петлей или пипеткой. При взятии петлей жидкость должна образовать в кольце петли тонкую прозрачную пленку – «зеркало». Пипетками пользуются в том случае, когда материал засевают в большом или точно отмеряемом объеме.
Способ взятия плотного материала определяется его консистенцией. При посевах чаще всего пользуются бактериологической петлей.
Все манипуляции, связанные с посевом и выделением микробных культур, производят над пламенем горелки. Бактериальную петлю перед взятием материала прокаливают в пламени горелки, затем ее остужают так, чтобы при соприкосновении с жидкой средой она не вызывала кипения жидкости, а прикосновение к агару не сопровождалось его плавлением. Для остуживания петли лучше всего погружать ее в конденсационную жидкость пробирки со стерильной питательной средой или прикасаться к крышке чашки Петри со стерильной средой. Нельзя остужать петлю прикосновением к поверхности питательной среды, даже свободной от микробного роста, так как на ней могут находиться колонии, не видимые простым глазом.
После окончания посева петлю прожигают повторно для уничтожения находящейся в ней микробной культуры или инфицированного микроорганизмами материала.
Пипетки и шпатели, использованные для посевов, опускают в дезинфицирующий раствор.
После посева на чашках Петри со стороны дна, на пробирках – в верхней трети надписывают название засеянного материала или ставят номер анализа и дату посевов.
8.1.1. Техника посевов на плотные и жидкие питательные среды
При посеве на скошенный агар петлю с находящимся на ней пересеваемым материалом вводят в пробирку до дна, опускают плашмя на поверхность питательной среды и скользящими движениями наносят штрихи снизу вверх от одной стенки пробирки к другой (рис. 8.1).
При обилии в засеваемом материале микробов они растут в виде пленки, покрывающей всю поверхность питательной среды. Такой характер микробного роста получил название сплошного или газонного. Посев газоном производят, когда нужно получить большие количества микробной культуры одного вида.
Чашки инкубируют при температуре 37 °С в течение 18– 24 ч, после чего подсчитывают количество колоний, выросших в разных секторах, и определяют количество бактерий в 1,0 мл по приведенной табл. 8.1 (этот метод принят для определения степени бактериурии).
Таблица 8.1. Определение количества бактерий в 1 мл методом секторных посевов*
Количество колоний в секторах
Количество бактерий в 1 мл
*Приказ № 535 от 22 апреля 1985 г. «Об унификации микробиологических (бактериологических) методов исследования, применяемых в клинико-диагностических лабораториях лечебно-профилактических учреждений» (Москва, 1985).
8.1.2. Методы выделения чистых культур
Чистой культурой принято называть совокупность однородных микроорганизмов, относящихся к одному виду, полученных из массы одной колонии, клетки которой идентичны по морфологическим, тинкториальным, культуральным, метаболическим и генетическим признакам, так как по существующим представлениям микробная колония является популяцией бактериальных клеток, возникшей в результате размножения единственной материнской клетки. Микробная колония являются аналогом клона.
Чистые культуры микроорганизмов одного вида, выделенные из различных источников, могут отличаться друг от друга незначительным отклонением морфологических, культуральных или биохимических признаков, не выходя за пределы своего вида или подвида. Такие культуры называют штаммами. Вместо ранее именованных типов в зависимости от характера изменившегося признака их обозначают морфоварами (отличные по морфологическим признакам), сероварами (имеющие антигенные отличия), биоварами (отличающиеся биологическими свойствами).
Чистая культура необходима для изучения морфологических, культуральных, биохимических и антигенных свойств, по совокупности которых определяется видовая принадлежность исследуемого микроорганизма.
Для выделения чистых культур микробов из материалов, содержащих обильную смешанную микрофлору, предложено много различных методов. Наибольшее распространение получил метод механического разъединения микроорганизмов, находящихся в исследуемом материале, с целью получения изолированных колоний на поверхности или в глубине питательной среды. Очень широко применяются селективные питательные среды, стимулирующие развитие тех микроорганизмов, чистую культуру которых предполагается выделить. Некоторые виды микробов обладают высокой чувствительностью к воздействию определенных факторов внешней среды. Индивидуальная устойчивость микробов к тому или иному фактору была использована для разработки методов выделения чистых культур путем умерщвления сопутствующей микрофлоры. Этим способом производится выделение споровых форм микробов, устойчивых к действию высокой температуры, микобактерий туберкулеза, безразличных к действию концентрированных растворов минеральных кислот, в отличие от остальных микробов, содержащихся в мокроте.
При выделении чистой культуры патогенных микробов из патологического материала, загрязненного посторонней микрофлорой, прибегают иногда к заражению лабораторных животных, восприимчивых к тому виду микроба, который предполагается выделить из исследуемого материала. Биологический метод выделения чистой культуры применяется при исследовании мокроты на содержание в ней пневмококков, микобактерий туберкулеза.
Получение чистой культуры методом рассева в глубине среды (по Коху). Три пробирки, содержащие по 15 мл мясопептонного агара, ставят в водяную баню для расплавления агара. Расплавленную среду остужают до температуры 43–45 °С. В пробирку вносят одну бактериологическую петлю исследуемого материала. Для лучшего перемешивания материала со средой засеянную пробирку вращают несколько раз, зажав между ладонями. После этого одну петлю (прокаленную и остуженную) содержимого 1-й пробирки переносят во 2-ю и таким же образом из 2-й в 3-ю. Приготовленные разведения микробов выливают из пробирок в стерильные чашки Петри, обозначенные номерами, соответствующими номерам пробирок.
После застудневания среды с исследуемым материалом чашки помещают в термостат. Количество колоний в чашках с питательной средой уменьшается по мере разведения материала.
Выделение чистой культуры по способу Дригальского. Расплавленную питательную среду разливают в три чашки Петри. Застывшую среду обязательно подсушивают, так как влажная поверхность ее способствует образованию сливного роста. В первую чашку вносят одну каплю исследуемого материала и стерильным шпателем втирают его в поверхность питательной среды. Далее, не прожигая шпателя и не набирая нового материала, шпатель переносят во 2-ю, а затем и 3-ю чашки, втирая в поверхность питательных сред оставшийся на нем материал.
Метод рассева по поверхности, предложенный Дригальским, является наиболее употребительным для получения чистой культуры микробов. Вместо шпателя можно пользоваться петлей. Материал на питательной среде распределяют параллельными штрихами по всей чашке в одном направлении. Затем, повернув чашку на 90°, проводят штрихи в направлении, перпендикулярном первым штрихам. При таком способе посева материал, находящийся в петле, расходуется постепенно, и по линиям штрихов, нанесенных в конце посева, вырастают изолированные колонии микробов.
Выращивание и выделение чистых культур анаэробов. Для выращивания анаэробов необходимо создать определенные условия, сущность которых заключается в удалении молекулярного кислорода из питательной среды и пространства, окружающего эти культуры. Другим обязательным условием, обеспечивающим выделение анаэробов из исследуемого материала, является внесение большого количества посевного материала в питательную среду.
Единственным отличием питательных сред, применяемых для выращивания анаэробов, служит пониженное содержание в них свободного кислорода. Самым простым способом удаления растворенного кислорода является кипячение. Непосредственно перед посевом материала пробирки с питательными Средами кипятят на водяной бане в течение 10–20 мин. При кипячении из среды вытесняется воздух и, следовательно, удаляется кислород. Свежепрокипяченную питательную среду быстро охлаждают, погружая в лед или подставляя под струю холодной воды, чтобы не дать ей насытиться кислородом воздуха, и используют для посева. Для уменьшения диффузии кислорода из воздуха питательные среды заливают сверху стерильным вазелиновым или парафиновым маслом (толщина слоя 1–1,5 см). Засев среды производят пипеткой сквозь масло в наклонном положении пробирки.
В качестве редуцирующих веществ используют глюкозу, аскорбиновую кислоту, цистеин, гликокол, глутатион. Активно связываются с кислородом животные ткани паренхиматозных органов. На этом свойстве животных клеток основано приготовление питательной среды Китта – Тароцци (рецепт 161), широко применяемой для выращивания анаэробов. В жидкие питательные среды помещают иногда пористые вещества: вату, пемзу, которые адсорбируют на своей поверхности пузырьки воздуха.
Для создания бескислородных условий используют физические, химические и биологические факторы.
Физические способы культивирования анаэробов:
Чтобы предупредить застывание питательной среды в момент насасывания ее в пипетки, пока их кончик не обломлен, пипетки погружают на 3–5 мин в стерильную воду с температурой 45–50 °С. После заполнения вытянутый конец трубки запаивают и помещают в стеклянный цилиндр с ватой на дне. Через 2–3 сут в столбике агара вырастают ясно видимые колонии микробов-анаэробов. Выросшие колонии легко изолировать. Для этого капилляр надрезают напильником выше уровня намеченной колонии, надламывают, а колонию микроба, находящуюся в агаре, извлекают петлей и пересевают в свежую питательную среду;
Химические методы выращивания анаэробов (метод Аристовского). Материал, исследуемый на наличие анаэробов, засевают на среду в чашки Петри и помещают их в эксикатор, на дно которого кладут химический поглотитель кислорода: гидросульфит натрия или пирогаллол. В расширенную часть сосуда устанавливают на подставке чашки с посевами. Прибор закрывают крышкой и помещают в термостат при температуре 37 *С на 24–48 ч.
Биологический метод выращивания анаэробов (по Фортнеру). В чашку Петри наливают толстым слоем 5 % кровяной агар с 1–2 % глюкозы. Посередине чашки в питательной среде вырезают стерильным скальпелем канавку шириной 1–1,5 см, которая делит питательную среду на две половины. Одну из них засевают культурой анаэробов или исследуемым на их наличие материалом, другую половину – культурой аэробов: чудесной палочкой (Serratia marcescens) или кишечной палочкой (Escherichia coli). Перед посевом чашки подсушивают в термостате, чтобы аэробы вместе с капельками влаги не могли попасть на другую сторону чашки. Засеянные чашки закрывают, а свободное пространство между дном и крышкой заклеивают лейкопластырем, чтобы предупредить поступление в чашку кислорода извне. В термостате чашки устанавливают вверх дном. Быстро растущие аэробы, поглощая находящийся в чашке кислород, создают тем самым благоприятные условия для роста анаэробов.
Анаэростат для культивирования анаэробов. Анаэростат – прибор для выращивания микробов в анаэробных условиях – представляет собой толстостенную металлическую или пластиковую камеру с герметически привинчивающейся крышкой, на которой имеются вакуумметр и два крана для присоединения к вакуум-насосу. Вместо кислорода в нем используются газовые смеси.