Магний в суточной моче
Это выявление количества магния в моче, собранной за сутки.
Магний в моче, соли магния в моче.
Синонимы английские
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Магний является четвертым по распространенности минералом в организме человека и жизненно важен для его функционирования. Это один из главных внутриклеточных катионов. Являясь кофактором многих ферментных систем, он задействован в реакциях энергетического обмена с участием аденозинтрифосфата (АТФ). Около 70 % магния – у человека в костях, оставшаяся часть главным образом содержится внутри клеток тканей и органов и включена в непрерывные метаболические процессы. 70 % от нее находится в свободном виде, в то время как 30 % связано с белками (в основном с альбуминами), а также с цитратами, фосфатами и другими веществами. Хотя только 1 % магния содержится в крови, в поддержании этого количества на постоянном уровне задействованы многие системы человеческого тела.
Регуляция магния происходит благодаря процессам в почках, в основном в восходящей части петли Генле. В частности, концентрация сывороточного магния зависит от того, сколько его выделилось через почки с мочой. Излишки поступившего с пищей минерала могут в небольшом количестве выходить со стулом.
Нарушения клубочковой фильтрации ведут к задержке магния и, как следствие, к повышению его концентрации в сыворотке. Гипермагниемия может возникать при острой и хронической почечной недостаточности, из-за избыточного поступления магния при лечении, а также при высвобождении магния из костей. Это опасно замедлением атриовентрикулярной проводимости.
При избытке магния могут возникать сбои в работе сердца, нарушение дыхания, депрессия.
Множеством исследований была доказана взаимосвязь между недостатком магния и изменениями в обмене кальция, калия, фосфора, ведущими к трудно поддающимся лечению желудочковым аритмиям, повышенной чувствительности к дигоксину, спазмам коронарных артерий. К тому же параллельно могут возникать симптомы нервно-мышечных и нейропсихиатрических нарушений.
Для чего используется этот анализ?
Когда назначается исследование?
Что означают результаты?
Референсные значения: 3 — 5 ммоль/сут.
Причины пониженного уровня магния в суточной моче
Причины повышенного уровня магния в суточной моче
Что может влиять на результат?
Причины ложнозавышенного результата
Причины ложнозаниженного результата
Кто назначает исследование?
Терапевт, уролог, нефролог, эндокринолог, гастроэнтеролог, диетолог, гинеколог.
Подписка на новости
Оставьте ваш E-mail и получайте новости, а также эксклюзивные предложения от лаборатории KDLmed
Оценка влияния степени экскреции фосфатов и магния на частоту формирования мочевых камней различного химического состава
М.Ю. Просянников, Н.В. Анохин, С.А. Голованов,О.В. Константинова, А.В. Сивков, О.И. Аполихин
Сведения об авторах:
ВВЕДЕНИЕ
Мочекаменная болезнь (МКБ) – важная не только медицинская, но и социальная проблема. Заболеваемость МКБ неуклонно растет практически во всех регионах мира, в том числе и в Российской Федерации 1, увеличивается количество госпитализаций в урологические стационары больных с диагнозом МКБ, растет число оперативных вмешательств по поводу уролитиаза.
Изучение метаболизма веществ, принимающих участие в процессах литогенеза и влияющих на камнеобразование, имеет первостепенное значение для назначения грамотной и адекватной метафилактики МКБ.
Наряду с диагностикой метаболизма основных камнеобразующих веществ – кальция, мочевой кислотой, оксалатов, оценка концентрации магния и фосфора в сыворотке крови и суточной моче имеет большое значение для разработки оптимальных подходов к метафилактике МКБ [3].
Магний – один из немногих элементов, способных ингибировать процессы камнеобразования в мочевых путях [3]. Доказано, что назначение препаратов магния при рецидивирующем уролитиазе уменьшает риск повторного камнеобразования: магний снижает средний размер агрегатов кальций оксалата и кальций фосфата [4, 5]. Магний способен ингибировать процессы литогенеза даже при кислых показателях pH мочи [6]. Назначение препаратов магния совместно с цитратными смесями увеличивает эффективность литолитической терапии [7], снижает уровень экскреции оксалатов в моче у пациентов с кальций-оксалатным уролитиазом [8]. Препараты магния способны снижать абсорбцию оксалатов в кишечнике у пациентов, страдающих уролитиазом [9].
В отличие от магния фосфор относиться к элементам-промотерам литогенеза. Опубликованы работы, где утверждается, что при избыточной потере фосфора с мочой, связанная с этим гиперфосфатурия является важным фактором камнеобразования кальциевых конкрементов [10]. В центральном регионе РФ фосфатные конкременты встречаются в 25% случаев, среди которых наиболее часто встречаются карбонатапатит, брушит и струвит [11].
Учитывая все вышесказанное, необходима комплексная диагностика метаболизма пациента. Важно оценить концентрацию как магния, так и фосфора в крови и суточной моче больного. При обнаружении гиперфосфатурии и гипомагниурии следует оценить необходимость и рассмотреть возможность коррекции данных нарушений у пациентов с МКБ.
Целью нашей работы стало изучение метаболизма магния и фосфора в организме пациентов, страдающих уролитиазом, определение реперных точек – значений признака, выход за рамки которого увеличивает риски возникновения той или иной формы уролитиаза.
МАТЕРИАЛЫ И МЕТОДЫ
На базе НИИ урологии и интервенционной радиологии имени Н.А. Лопаткина – филиала «НМИЦ радиологии» Минздрава России были проанализированы данные обследования 708 пациентов (303 мужчин и 405 женщин) с диагнозом МКБ. в возрасте от 17 до 78 лет, которые проходили обследование и лечение в период с 2010 г. по 2017 г.
Исследование биохимических показателей крови и показателей суточной экскреции мочи проводили на автоанализаторе ADVIA 1200 (Bayer-Siemens) по стандартным методикам с помощью диагностических наборов реагентов фирмы Siemens (Германия). Образцы крови и мочи брали у пациентов до выполнения плановых хирургических вмешательств (дистанционной литотрипсии, перкутанной нефролитолапаксии и других). В исследование отбирались пациенты, не имевшие признаков воспаления почечной паренхимы.
Минеральный состав мочевых конкрементов или их фрагментов, полученных после оперативных вмешательств или отошедших самостоятельно, определяли методом инфракрасной спектроскопии на ИК-Фурье спектрометре Nicolet iS10 (Thermo Scientific, США) с использованием библиотеки спектров мочевых камней известного состава. Отнесение камней смешанного состава к тому или иному типу мочевых камней (оксалатные, мочекислые, фосфатные (из карбонатапатита или струвита) проводилось по главному преобладающему минеральному компоненту (более 50% всей минеральной основы). Такой подход к классификации типов мочевых конкрементов является наиболее распространенным 3.
Исследование биохимических показателей крови и показателей суточной экскреции мочи проводили на автоанализаторе ADVIA 1200 (Bayer-Siemens) по стандартным методикам с помощью диагностических наборов реагентов фирмы Siemens (Германия).
В сыворотке крови пациентов определяли концентрацию общего кальция, натрия, калия, фосфора, магния, хлора, мочевой кислоты, креатинина, мочевины в сыворотке крови. В образцах суточной мочи определяли показатели экскреции общего кальция, натрия, калия, фосфора, магния, хлора, мочевой кислоты, креатинина, мочевины.
Для изучения встречаемости камней различного химического состава при различных уровнях магниурии выполнялось ранжирование магниурии на 10 интервалов: от 0,2 до 12,9 ммоль/сут (табл. 1).
Таблица 1. Распределение степени магниурии на диапазоны
Table 1. Distribution of the degree of magniuria by ranges
| № диапазона Range No. | Уровень экскреции магния с мочой (ммоль/сут) Level of magnesium excretion in urine (mmol/day) |
|---|---|
| Mg1 | 0,20 – 1,49 |
| Mg2 | 1,5 – 2,1 |
| Mg3 | 2,13 – 2,5 |
| Mg4 | 2,6 – 3,2 |
| Mg5 | 3,25 – 3,5 |
| Mg6 | 3,6 – 4,0 |
| Mg7 | 4,1 – 4,5 |
| Mg8 | 4,6 – 5,3 |
| Mg9 | 5,4 – 6,4 |
| Mg10 | 6,5 – 12,9 |
Для изучения встречаемости камней различного химического состава при различных уровнях фосфатурии выполнялось ранжирование фосфатурии на 10 интервалов: от 1,15 до 65,4 ммоль/сут (табл. 2).
Таблица 2. Распределение степени фосфатурии на диапазоны
Table 2. Distribution of the degree of phosphaturia by ranges
| № диапазона Range No. | Уровень экскреции фосфатов с мочой (ммоль/сут) Level of phosphate excretion in urine (mmol/day) |
|---|---|
| P1 | 1,15 – 13,2 |
| P2 | 13,3 – 16,3 |
| P3 | 16,4 – 18,4 |
| P4 | 18,5 – 21,0 |
| P5 | 21,2 – 24,4 |
| P6 | 24,5 – 26,9 |
| P7 | 27,0 – 30,2 |
| P8 | 30,4 – 34,2 |
| P9 | 34,4 – 40,2 |
| P10 | 40,4 – 65,4 |
Статистический анализ проводили с использованием статистического критерия Хи-квадрат Пирсона, что позволило определить достоверность различия между частотами выявления камней различного химического состава при различной степени фосфатурии и магниурии.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Фосфатурия Анализ полученных результатов показал, что влияние фосфатурии на вероятность образования мочевых камней различно и варьирует в зависимости от типа мочевого камня и степени фосфатурии.
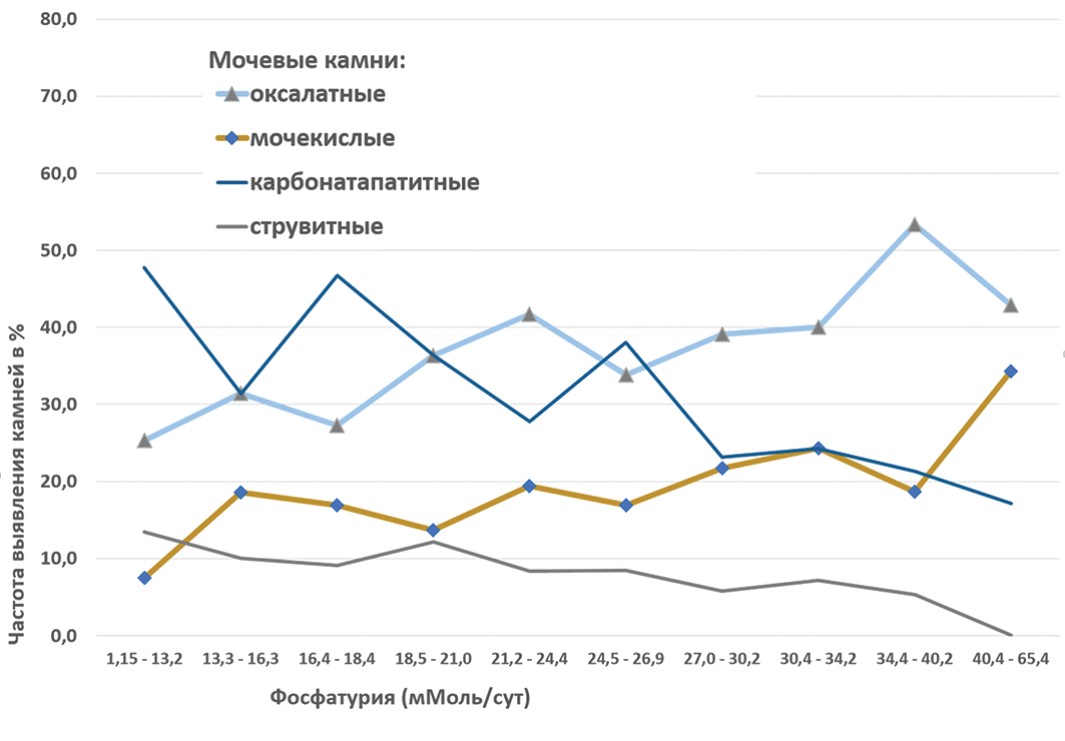
Частота формирования кальций-оксалатных конкрементов возрастает прямо пропорционально степени фосфатурии: если при показателях экскреции фосфора с мочой 1,15-13,2 (P1) частота встречаемости кальцийоксалатных камней равна 25,4%, то в интервале фосфатурии 34,4-40,2 (P9) кальций-оксалатные конкременты наблюдаются в 53,3% случаев (рис. 1).
Рис. 1. Частота мочевых камней различного химического состава (в % от общего количества конкрементов) в зависимости от степени фосфатурии
Fig. 1. Frequency of urinary stones of various chemical composition (in% of the total number of calculi) depending on the degree of phosphaturia
Таким образом, отмечается увеличение частоты встречаемости доли кальций-оксалатных камней при возрастании степени фосфатурии (P1-P10) на 17,5% (р=0,031).
Необходимо отметить, что согласно данным последних исследований приблизительно в 80% случаев в состав кальций-оксалатных конкрементов входит кальций-фосфат, который определяется чаще всего в центре камня [12]. Также проведенные исследования показали, что кристаллы апатита и брушита in vitro инициируют кристаллизацию кальций-оксалата из метастабильного раствора, что также стимулирует литогенез 15. Наличие кристаллов кальций-фосфата может играть огромную роль в формировании кальций-оксалатных конкрементов, фактически, кальций-фосфат является ядром для формирования кальций-оксалатных камней.
Согласно современной теории камнеобразовании, наличие бляшки Рэндалла является одним из необходимых условий формирования кальциевых конкрементов (кальций-оксалатных и кальций-фосфатных) [16]. Бляшка Рэндалла, в свою очередь, всегда состоит из солей кальций-фосфата, что объясняет тот факт, что в состав кальций-оксалатного камня в 80% случаев входят кристаллы кальций-фосфата [2, 17].
Результаты научных работ показали, что показатели реабсорбции фосфора в почечных канальцах у пациентов, страдающих МКБ, ниже, чем у здоровых лиц, что также косвенно указывает на ведущую роль нарушения метаболизма фосфора в патогенезе МКБ [18, 19]. Реабсорбция фосфора в почечных канальцах регулируется влиянием многочисленных белков и гормонов. Одной из основных причин гиперфосфатурии могут быть дефекты в строении белков-транспортеров, что проявляется в виде дисфункции проксимальных почечных канальцев [19]. Нарушение реабсорбции фосфора в почечных канальцах в свою очередь приводит к снижению уровня фосфора в сыворотке крови. В то же время доказано, что гиперфосфатурия увеличивает риск формирования кальций-оксалатных камней только в том случае, если сочетается с гиперкальциурией. В большинстве случаев гиперкальциурия при наличии сопутствующей гиперфосфатурии вызвана высоким уровнем кальцитриола (активный метаболит витамина D3) в сыворотке крови в ответ на гипофосфатемию. Таким образом, по современным представлениям о патогенезе МКБ одной из причин камнеобразования у пациентов с идиопатическим кальций-оксалатным уролитиазом является наличие генетически детерминированного дефекта почечных канальцев, которые в свою очередь приводит к гипофосфатемии, гиперфосфатурии и гиперкальциурии [19].
Частота встречаемости кальций-фосфатных (карбонатапатитных) конкрементов имела стойкую тенденцию к снижению в интервалах P1-P10. Если в первом интервале P1 (1,15 – 13,2 ммоль/сутки) карбонатапатитные конкременты были обнаружены в 47,8% случаев наблюдений (р=0,00012), то в десятом интервале P10 (40,4 – 65,4 ммоль/сутки) только в 17,1% (рис. 1). Разница частоты встречаемости кальций-фосфатных (карбонатапатитных) конкрементов в интервалах фосфатурии P1-P10 была равна 30,7% (р=0,00012).
Известно, что формирование кальций-фосфатных (карбонатапатитных) камней происходит только при наличии бляшек Рэндалла, то есть процессы литогенеза кальций-фосфатных конкрементов во многом похожи на процессы, протекающие при кальций-оксалатном уролитиазе [16]. Тем не менее по данным проведенного исследования частота встречаемости кальций-оксалатных и кальций-фосфатных камней при одинаковой степени фосфатурии различна. По всей видимости, на частоту формирования кальций-фосфатных конкрементов помимо уровня фосфатурии влияют иные процессы, в то время как литогенез кальций-оксалатных конкрементов напрямую связан со степенью фосфатурии.
Частота встречаемости мочекислых конкрементов напрямую зависит от степени выраженности фосфатурии. При увеличении уровня фосфатурии отмечается стабильный рост частоты выявления мочекислых камней (рис.1). Так, при степени фосфатурии равной 1,15 – 13,2 ммоль/сут мочекислые конкременты выявлялись в 7,5% случаев. При степени фосфатурии 40,4 – 65,4 ммоль/сут мочекислые камни были обнаружены в 34,3%. Разница частоты встречаемости мочекислых конкрементов была равна 26,8% (р=0,0001).
Проведенное исследование также показало, что с возрастанием степени фосфатурии (P1-P10) снижается частота формирования струвитных камней с 13,4% в интервале фосфатурии P1 1,15 – 13,2 ммоль/сут до 0 в интервале фосфатурии P10 равной 40,4 – 65,4 ммоль/сут (рис. 1).
Таким образом, проведенное исследование показало, что при возрастании степени фосфатурии увеличивается частота выявления кальций-оксалатных и мочекислых конкрементов. При этом частота обнаружения кальций-фосфатных (карбонатапатитных) и струвитных камней стабильно снижалась при повышении уровня фосфатурии.
Фосфатурия – недостаточно изученное метаболическое литогенное нарушение. С одной стороны, фосфор входит в состав 30-35% мочевых камней (кальцийфосфатные, струвитные), с другой стороны, согласно рекомендациям, как Европейской, так и Американской ассоциаций урологов нет необходимости следить за степенью фосфатурии у пациентов с МКБ. Считаем, что на настоящий момент влияние фосфора на литогенез изучено не полностью, необходимо проведение дополнительных научных исследований, которые помогут приоткрыть завесу тайны над влиянием фосфора на патогенез МКБ.
Магниурия
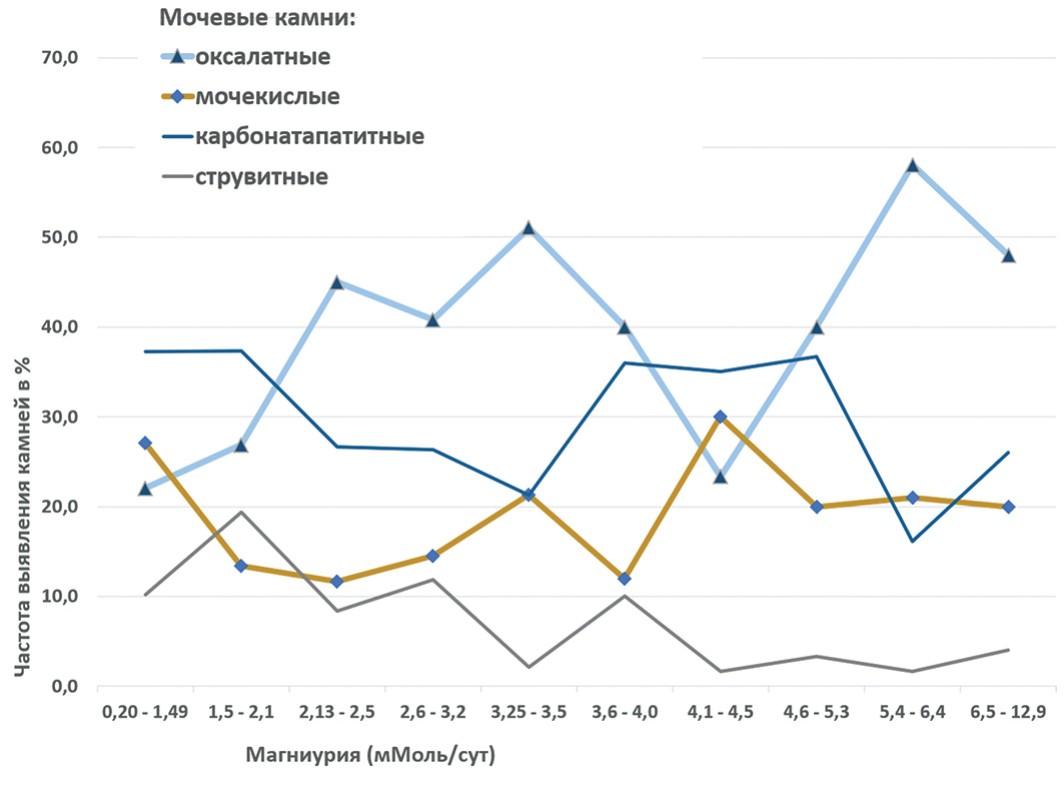
Анализ частоты встречаемости кальций-оксалатных конкрементов при различных степенях магниурии показал, что в интервалах магниурии Mg1 (0,20- 1,49 ммоль/сут) – Mg5 (3,25-3,5 ммоль/сут) отмечается стойкая тенденция к росту частоты выявления кальций-оксалатных камней с 22% до 51,1% (рост 29,1% (р=0,008)). При этом в интервалах магниурии Mg5 (3,25-3,5 ммоль/сут) – Mg7 (4,1-4,5 ммоль/сут) выявлено снижение доли кальций-оксалатных камней с 51,1% до 23,3%, а при магниурии Mg7 (4,1-4,5 ммоль/сут) – Mg9 (5,4- 6,4 ммоль/сут) отмечается повторный рост частоты встречаемости кальций-оксалатных конкрементов до 58,1% (рост 34,8 % (р=0,00009)), (рис. 2).
Рис. 2. Встречаемость мочевых камней (в % от общего количества конкрементов) в зависимости от степени магниурии
Fig. 2. The incidence of urinary stones (in% of the total number of calculi) depending on the degree of magnesiumuria
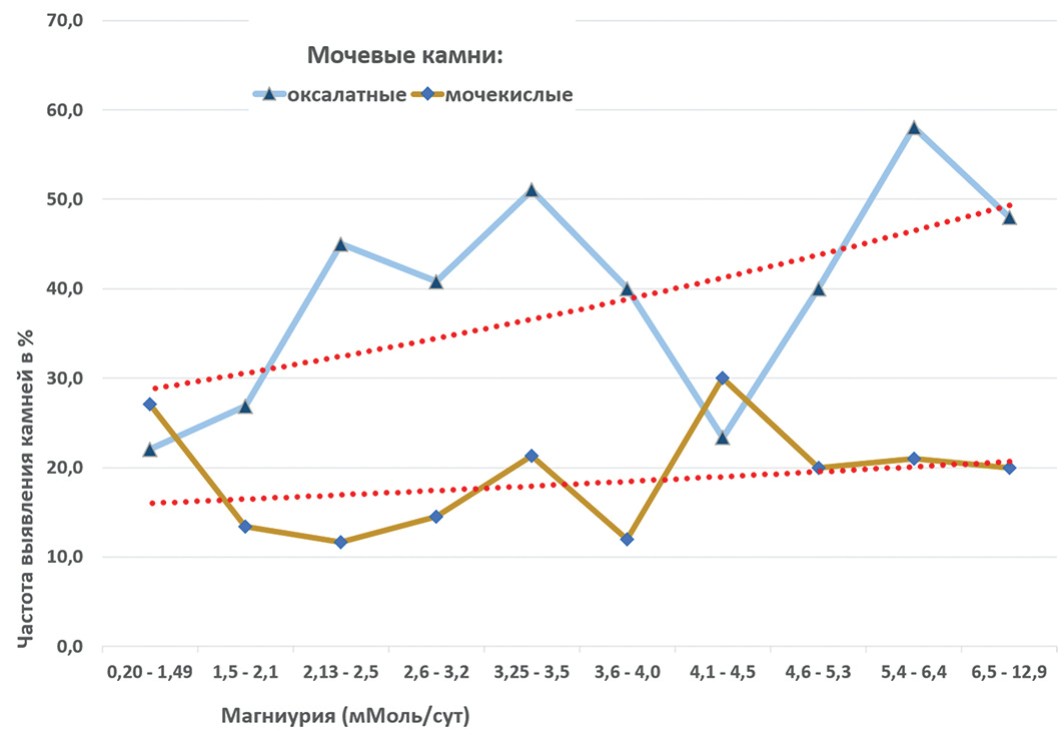
При построении экспоненциальной линии тренда отмечается увеличение доли встречаемости кальцийоксалатных конкрементов при росте степени магниурии (снижение доли карбонатапатитных конкрементов на 11,3% (р>0,05) (рис. 3).
В научном сообществе принято считать, что магний является ингибитором камнеобразования [20, 21]. Результаты проведенных научных исследований, в том числе и отечественных, показали, что регулярный прием препаратов магния снижает образование кальцификатов в почечной ткани и препятствует развитию уролитиаза. Так А.А. Спасов и соавт. в опыте на крысах доказали, что применение магния в комбинации с витамином B6 препятствует образованию мочевых камней на фоне введения в рацион питания экспериментальных животных камнеобразующих веществ – натрий оксалата и целекоксиба [22].
Рис. 3. Частота встречаемости мочекислых и кальций-оксалатных мочевых камней с учетом степени магниурии. На рисунке представлена экспоненциальная линия тренда (пунктирная линия).
Fig. 3. Frequency of occurrence of uric acid and calcium oxalate urinary stones, taking into account the degree of magnesiumuria. The figure shows an exponential trend line (dashed line)
S.R. Khan и соавт. в эксперименте получили данные, что применение препаратов магния стимулирует увеличение рН мочи, увеличивает уровень экскреции цитрата с мочой, при этом снижая уровень суточной экскреции оксалатов с мочой [23]. Опубликованы работы, в которых также доказано, что препараты магния снижают абсорбцию экзогенных оксалатов в кишечнике, связываясь с ними 24.
Тем не менее, не все исследователи убеждены в наличии ингибиторной активности у магния при МКБ. Так при исследовании группы пациентов с рецидивирующим кальций-оксалатным уролитиазом не было обнаружено снижения экскреции магния с мочой [26]. Также при обследовании 2147 пациентов с МКБ гипомагниурия была выявлена только у 11% больных, тогда как у остальных 89% больных этот показатель находился в пределах нормальных значений [27]. Результаты другого исследования показали, что у пациентов с идиопатическим кальцийоксалатным уролитиазом повышенная экскреция магния ассоциировала с усиление экскреции кальция и натрия, что клинически проявлялось в виде более активной формы уролитиаза [28]. Похожие данные были получены и настоящем исследовании – при увеличении частоты встречаемости кальций-оксалатных камней увеличивалась и степень магниурии.
Необходимо подчеркнуть, что в научном сообществе обсуждается вопрос о связи дефицита магния в организме с активностью процессов оксидативного стресса [29]. Опубликованы данные подтверждающие, что дефицит магния сопровождается повышением уровня маркеров оксидативного стресса: продуктов окислительной модификации липидов, белков и ДНК. Более того, утверждается, что именно дефицит магния приводит к процессам, протекающим при оксидативном стрессе, за счет активации ренин-ангиотензиновой системы [30].
Представленные данные тесно переплетаются с современными представлениями о патогенезе МКБ. Согласно одной из теорий литогенеза именно процессы оксидативного стресса лежат в основе формирования бляшек Рэндалла, образование которых в свою очередь является одним из необходимых условий для камнеобразования [31].
Считаем, что роль магния в патогенезе кальцийоксалатного уролитиаза изучена недостаточно. Опубликовано большое количество работ с противоречивыми выводами о влиянии магния на литогенез при МКБ. Необходимо продолжить проводимые исследования для изучения метаболизма магния в организме.
При анализе частоты встречаемости мочекислых мочевых камней в зависимости от степени магниурии статистически достоверной связи отмечено не было. Достоверное различие изменения уровня частоты встречаемости мочекислых конкрементов было выявлено только между интервалами Mg6 (3,6 – 4,0 ммоль/сутки) – Mg7 (4,1 – 4,5 ммоль/сутки) и составило 16,7% (рис. 2, р=0,023).
Исследование частоты встречаемости карбонатапатитных конкрементов в зависимости от степени магниурии показало, что рост доли карбонатапатитных камней наблюдался в интервалах магниурии Mg5 (3,25 – 3,5 ммоль/сутки) – Mg6 (3,6 – 4,0 ммоль/сутки) и составил 14,7% (рис.2, р=0,03).
При этом в интервале Mg1 (0,20 – 1,49 ммоль/сутки) – Mg5 (3,25 – 3,5 ммоль/сутки) было зафиксировано снижение частоты встречаемости карбонатапатитных камней на 16% с 37,3% до 21,3%. В интервале Mg8 (4,6 – 5,3 ммоль/сутки) – Mg9 (5,4 – 6,4 ммоль/сутки) снижение доли карбонатапатитных конкрементов составило 20,6% (р
Роль препаратов магния в ведении пациентов терапевтического профиля
Огромная роль магния (Mg ++ ) в обеспечении самого широкого спектра физиологических процессов в организме человека несомненна [5, 30, 33]. Магний является незаменимым макроэлементом организма и занимает четвертое место после натрия, калия и кальц
Огромная роль магния (Mg ++ ) в обеспечении самого широкого спектра физиологических процессов в организме человека несомненна [5, 30, 33]. Магний является незаменимым макроэлементом организма и занимает четвертое место после натрия, калия и кальция по своей распространенности в организме человека. Однако до настоящего времени определение его уровня в плазме крови не стало нормой в условиях реальной клинической практики, так как считается, что он только косвенно и очень приблизительно отражает его содержание внутри клетки.
Роль магния для организма человека
В норме за сутки в организм должно поступать около 300 мг магния для женщин и 350 мг — для мужчин. Общее количество магния у человека составляет около 24 г, причем около 40% находится внутри клеток. Наибольшее количество магния находится в костной (около 60%) и мышечной (около 20%) тканях. Около 40% от общего количества содержится в клетках сердца, головного мозга, почек, 20–30% от этого количества может быть достаточно быстро мобилизовано в условиях его повышенного потребления. Около 60% сывороточного магния находится в ионизированном виде, остальная часть связана с протеинами, фосфатами, цитратами. В плазме крови и эритроцитах находится менее 1% от общего количества магния. На сердце приходится около 20% всего магния, содержащегося в организме человека, что говорит о его большом значении для нормальной сердечной деятельности.
Потребность в магнии существенно возрастает при физических нагрузках, стрессе, в условиях жаркого климата, в период беременности и лактации, при посещении бани, злоупотреблении алкоголем, несбалансированных ограничительных диетах и синдроме хронической усталости [5, 17]. В этих ситуациях потребность повышается в среднем на 150 мг в сутки. Основными источниками поступления магния в организм являются бобовые и злаковые, шпинат, салаты, руккола, брокколи, ревень. Особенно богаты магнием орехи и шоколад, но существенное увеличение потребления данных продуктов может привести к прибавке в весе в связи с их высокой калорийностью. Кроме этого, необходимо помнить, что усваивается не более 30–40% магния, поступающего с пищей. При этом для его хорошей усвояемости также требуется поступление в организм в достаточном количестве кофакторов: молочной, аспарагиновой, оротовой кислот и, что особенно важно, витамина В6 [33]. В развитии алиментарного дефицита магния важную роль играют такие факторы, как его низкое содержание в пище, воде, а также избыточное потребления кальция, натрия, белка или жира с пищей, что существенно снижает поступление магния в организм из-за образования его невсасывающихся комплексов. Частота гипомагниемии у людей достаточна высокая и составляет от 10 до 40% [5, 19]. Для обозначения нарушений обмена магния используют два термина. Под «магниевым дефицитом» понимают снижение общего содержания магния в организме. Под «гипомагниемией» подразумевают снижение концентрации магния в сыворотке (в норме 0,8–1,2 ммоль/л). Умеренной недостаточности магния в организме соответствует его уровень в сыворотке крови 0,5–0,7 ммоль/л, выраженной (угрожающей жизни) — ниже 0,5 ммоль/л. Также выделяют первичный (генетически обусловленный) и вторичный (алиментарный, физиологический и т. д.) дефицит магния.
Частота выявления гипомагниемии зависит от особенностей исследуемой популяции, критериев диагностики и использованных методов диагностики. Обнаружение нормальных показателей магния в сыворотке крови не исключает его общего дефицита и гипокалиегистии, так как при возникновении дефицита магния он может высвобождаться из костей, предотвращая снижение его сывороточной концентрации. Поэтому клиническая ценность определения концентрации Mg ++ в сыворотке крови, в том числе и в ее форменных элементах, имеет клиническое значение только при наличии гипомагниемии.
Гомеостаз Mg ++ также очень сильно зависит от возраста (пожилые люди склонны к гипокалиемии, а у молодых среднесуточная потребность на 150 мг больше) и состояния кишечной абсорбции (например, уровень магния резко снижен при синдроме мальабсорбции и диарее) [33], которая в основном происходит в двенадцатиперстной кишке и проксимальном отделе тощей кишки. Снижают всасывание магния железо, кальций, фосфор, щавелевая кислота, фитаты и танин, содержащиеся в крепко заваренном чае. До 30% магния, получаемого с пищей, выводится через почки. Экскреция магния значительно возрастает при повышении уровня катехоламинов и глюкокортикостероидов. В условиях дефицита магния его выведение через почки существенно снижается. Также существенные потери магния могут иметь место при усиленном потоотделении. Основные причины дефицита магния представлены в табл. 1.
В настоящее время магний считается одним из основных регуляторов обменных процессов и его физиологические эффекты в организме человека хорошо изучены. Магний оказывает влияние на:
Известно, что магний является естественным антагонистом кальция, что обусловливает наличие у него миотропного, спазмолитического и дезагрегационного эффектов и участие в обеспечении нормальных электрофизиологических процессов клеток за счет влияния на трансмембранный потенциал [1].
В последнее время установлена важная роль магния в развитии эндотелиальной дисфункции. Было показано, что назначение препаратов магния способно через 6 мес существенно улучшить (почти в 3,5 раза больше по сравнению с плацебо) эндотелийзависимую дилятацию плечевой артерии. При этом также была выявлена прямая линейная корреляция — зависимость между степенью эндотелийзависимой вазодилятации и концентрацией внутриклеточного магния [22]. Одним из возможных механизмов, объясняющих благоприятное влияние магния на эндотелиальную функцию, может быть его антиатерогенный потенциал.
Дефицит магния может проявляться самой различной симптоматикой:
Также дефицит магния негативно сказывается на течении беременности, провоцируя преждевременные роды и повышая сократимость матки.
Состояние обмена магния при патологических состояниях
Артериальная гипертензия. Считается, что ионы магния подавляют активность ренин-ангиотензин-альдостероновой системы, поэтому на фоне гипомагниемии часто имеет место выраженная вазоконстрикция [2, 7, 16, 22].
Экспериментальные данные указывают на важную роль ионов магния в регуляции сосудистого тонуса. При снижении уровня внеклеточного магния увеличивается поступление кальция внутрь клетки, что вызывает вазоконстрикцию. При парентеральном введении магния наблюдается выраженная вазодилятация, сопоставимая с эффектом антагонистов кальция. Коррекция поступления в организм магния с помощью пищевых добавок позволяет добиться нормализации уровня АД при мягкой артериальной гипертонии у пожилых [9], в том числе и в условиях двойного слепого плацебо-контролируемого исследования [26].
В настоящее время явно недостаточно клинических данных для окончательного вывода о возможности использования магния с гипотензивной целью. У больных артериальной гипертензией, особенно при наличии гипертонической энцефалопатии, длительный прием магния в суточной дозе 15 ммоль сопровождался снижением АД в среднем на 12/8 мм рт. ст. В 29 ретроспективных исследованиях была выявлена связь между уровнем АД и потреблением магния. В то же время данные клинических исследований не подтвердили факт снижения АД при увеличении потребления магния. Только в одном из них, выполненном в Японии, увеличение потребления магния до 20 ммоль в день через 8 недель сопровождалось снижением АД на 2,5 мм рт. ст. и 3,7 мм рт. ст. по результатам суточного мониторирования артериального давления (СМАД).
Вместе с тем дополнительный прием магния можно рекомендовать больным с артериальной гипертензией, у которых имеется высокий риск гипомагниемии (например, при терапии тиазидными диуретиками [32]).
Ишемическая болезнь сердца (ИБС). По данным эпидемиологических исследований дефицит магния в питьевой воде повышает риск развития сердечно-сосудистых заболеваний (особенно ИБС) и внезапной смерти. Известно, что миокард больных, умерших от сердечно-сосудистой патологии, содержит почти в 2 раза меньше магния, чем у пациентов, скончавшихся от других причин.
Показано, что дефицит магния ассоциируется с повышением уровня атерогенных липидов [14, 20, 32]. Более того, по данным исследования ARIC (The Atherosclerosis Risk in Communities), частота развития ИБС выше у тех лиц, у которых выявляется более низкий уровень магния в крови. Причем эта закономерность сохраняется после стандартизации пациентов по их демографическим характеристикам, уровню холестерина, фибриногена и других факторов риска.
В Финляндии в результате реализации правительственной программы по профилактике магниевого дефицита у населения страны в течение последних 15 лет удалось снизить частоту инфарктов миокарда в популяции почти в 2 раза.
Анализ обобщенных данных 7 рандомизированных исследований у 1301 больного острым инфарктом миокарда выявил благоприятное влияние магния на больничную летальность [4, 8, 21, 24].
В многоцентровом исследовании LIMIT–II (Second Leicester Intravenous Magnesium Intervention Trial) (2316 пациентов) было выявлено снижение риска смерти на 24%, риска развития сердечной недостаточности на 25% (в группе больных острым инфарктом миокарда, которые в течение первых 28 дней получали дополнительно к стандартной терапии инфузии сульфата магния). Однако в более позднем исследовании (58 050 пациентов) при лечении сульфатом магния и изосорбидом мононитрата в сравнении с каптоприлом не было выявлено снижения летальности в группе больных, получавших магний, хотя на фоне терапии препаратами магния, несмотря на отсутствие снижения летальности у больных с гипомагниемией, существенно реже встречались аритмии, судороги в мышцах, чувство тревоги и другие проявления его дефицита.
Хроническая сердечная недостаточность. Дефицит магния был обнаружен при сердечной недостаточности, развившейся на фоне артериальной гипертензии и ИБС [25]. Причем тяжесть хронической сердечной недостаточности прямо коррелировала со степенью дефицита магния: это связывают с тем, что на фоне гипомагниемии существенно уменьшается диурез [12]. Кроме этого показано, что на фоне дефицита магния гораздо чаще развиваются нарушения ритма и проводимости при терапии сердечными гликозидами [29].
Нарушения сердечного ритма. Исследование Framinghem Heart Study продемонстрировало, что длительная гипомагниемия коррелирует с высокой частотой возникновения желудочковых экстрасистол, тахикардии, фибрилляции желудочков. В исследовании PROMISE Study была выявлена большая частота желудочковой экстрасистолии и высокая летальность в группе пациентов с гипомагниемией в сравнении с группами, в которых отмечалась нормо- и гипермагниемия.
Препараты магния давно используются как антиаритмические средства, сочетающие свойства антиаритмиков I (мембраностабилизирующие) и IV классов (антагонисты кальция). Магний предотвращает потерю калия клеткой и уменьшает вариабельность длительности интервала QT, которая является прогностически неблагоприятным фактором развития фатальных аритмий. Кроме того, магний способен ингибировать симпатические влияния на сердце [23, 33].
В качестве антиаритмика соли магния наиболее эффективны (препарат выбора) при пируэт-желудочковой аритмии (torsades de pointes), благодаря способности угнетать развитие следовых деполяризаций и укорачивать длительность интервала QT [11, 35]. Магний также используется как при врожденном синдроме удлиненного интервала QT, так и при его удлинении вследствие применения антиаритмиков I класса.
Препараты магния широко используются при лечении аритмий на фоне дигиталисной интоксикации благодаря способности восстанавливать функцию калий-натриевой помпы [8].
Результаты рандомизированного многоцентрового плацебо-контролируемого двойного слепого исследования MAGICA позволили рассматривать препараты магния и калия как общепринятый европейский стандарт при лечении аритмий у пациентов на фоне приема сердечных гликозидов, диуретиков, антиаритмиков. Антиаритмический эффект препаратов магния проявляется спустя 3 недели от начала лечения и позволяет снизить число желудочковых экстрасистол на 12% и общее число экстрасистол на 60–70%.
Пролапс митрального клапана. По данным эпидемиологических исследований у пациентов с пролапсом митрального клапана дефицит магния выявляется почти в 2/3 случаев [6, 13]. Прием препаратов магния данной категорией пациентов позволяет уменьшить проявления вегетативного дисбаланса: уменьшить симпатические влияния вегетативной нервной системы и усилить парасимпатическую активность. При этом наблюдается увеличение интервалов RMSSD днем и снижение в ночные часы.
Сахарный диабет. Гипомагниемия часто встречается при сахарном диабете 2-го типа [15]. Также считается, что дефицит магния повышает риск развития нарушения толерантности к глюкозе [4], так как ионы магния улучшают инсулинозависимую утилизацию глюкозы.
Алкогольная интоксикация. При злоупотреблении алкоголем дефицит магния играет важную роль в развитии психосоматического симптомокомплекса, миопатий, нейропатий, аритмий и абстинентного синдрома и аритмий [17].
Предменструальный синдром. Рассматривается как вариант стресса, сопровождающийся дефицитом магния и склонностью к спазму гладких мышц.
Таким образом, препараты магния играют важную роль в ведении пациентов с сердечно-сосудистой патологией прежде всего благодаря их способности благоприятно влиять на имеющиеся факторы риска и снижать риск сердечно-сосудистых заболеваний на уровне популяции.
В настоящее время существует несколько препаратов, содержащих магний для заместительной терапии (табл. 2). Выбор препаратов магния для коррекции его дефицита лежит между неорганическими и органическими солями магния. Первое поколение магнийсодержащих препаратов в своем составе имело неорганические соли, из которых магния усваивалось не более 5%. Кроме того, пациенты их плохо переносили из-за частого развития диареи, так как магний стимулирует перистальтику кишечника. Второе поколение магнийсодержащих препаратов значительно лучше усваивается и не провоцирует развитие диспепсии и диареи.
Поливитаминные комплексы с минералами не могут рассматриваться как источник магния для заместительной терапии, так как обычно содержат несколько микроэлементов, мешающих усвоению друг друга (например, всасывание магния снижается в присутствии кальция), поэтому эффективность поливитаминов с минералами значительно ниже, чем у специальных препаратов, содержащих магний.
При дефиците магния требуется его дополнительное введение из расчета 10–30 мг на килограмм массы тела в сутки на протяжении не менее 2 месяцев, что обусловлено медленным насыщением тканевых депо. Естественно, что обеспечить такое повышенное поступление магния только за счет изменения пищевого рациона нереально.
Одним из наиболее эффективных препаратов является Магнерот, который помимо магния содержит оротовую кислоту, которая способствует росту клеток, участвует в процессе обмена веществ. Поэтому Магнерот считается препаратом выбора в комплексном лечении и профилактике инфаркта миокарда, хронической сердечной недостаточности, аритмий сердца, вызванных дефицитом магния, спастических состояний, атеросклероза, гиперлипидемий. Противотревожное действие Магнерота существенно расширяет спектр его клинического применения. Имеющаяся клиническая доказательная база позволяет комбинировать его с антидепрессантами, противосудорожными и снотворными средствами при комплексной терапии депрессий, судорожных состояний и инсомнических расстройств.
Литература
С. В. Недогода, доктор медицинских наук, профессор
ВолГМУ, Волгоград