Проведение операций на поджелудочной железе в Израиле
Лечение рака поджелудочной железы хирургическим путем
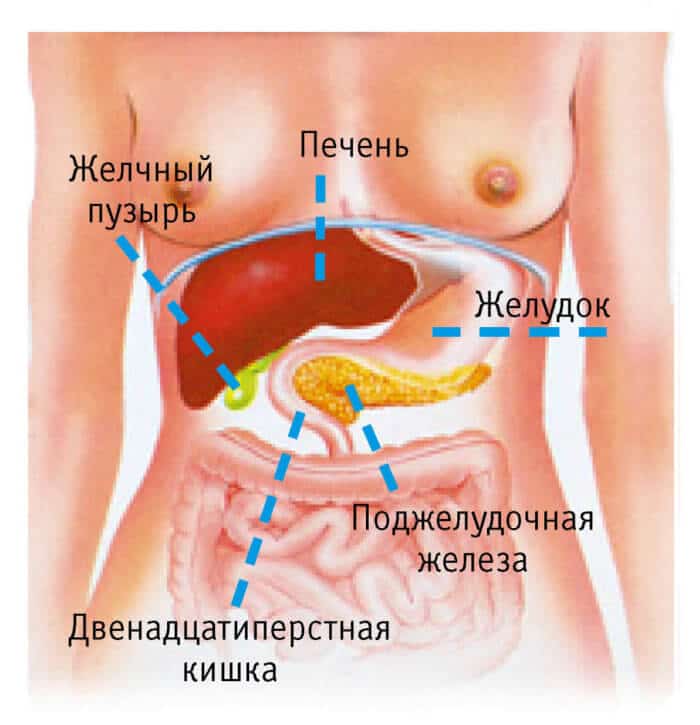
Поджелудочная железа – небольшой орган, который расположен под желудком в глубине живота позади двенадцатиперстной кишки. Условно ее разделяют на следующие части:
Поджелудочная железа выделяет важные для жизни человека биологические вещества: гормоны инсулин, глюкагон, которые регулируют уровень сахара в крови, энзимы – так называемые «соки поджелудочной железы» (амилаза, липаза), участвующие в расщеплении пищевых жиров.
Сам орган имеет маленькие размеры, но играет важную роль. Соки поджелудочной железы выделяют из пищи жизненно важные элементы, необходимые для поддержания жизнедеятельности человека. Стоит отметить, что синтезировать их в лаборатории до сих пор не удалось.
К сожалению, рак поджелудочной железы часто диагностируется поздно, так как имеет неясные и довольно гуманные симптомы: боли, зуд кожи и снижение веса. Так как заболевание выявляется на поздних стадиях, оно считается очень опасным.
Рак поджелудочной железы – основное показание к операции на поджелудочной железе и частичной резекции органа. Также причиной к проведению операции является обнаружение предракового состояния. В случае хронического воспаления и цисты применяется медикаментозное лечение.
Поскольку рак поджелудочной железы выявляется поздно, только 10% случаев являются операбельными. На слишком поздних стадиях невозможно провести частичную резекцию органа. Тем не менее, в настоящее время частичная резекция поджелудочной железы – единственное средство борьбы с раком данного органа.
Шансы на выздоровление после операции на поджелудочной железе
Рак поджелудочной железы – самый опасный вид рака. Даже наличие небольших размеров опухоли, что позволяет провести операцию по удалению, не являются гарантией выздоровления пациента.
Широкомасштабные исследования в данной области показали, что проведение операции в крупном медицинском центре (например, медицинский центр Тель-Авивский), где работают опытные специалисты, постоянно выполняющие подобные операции, в три раза увеличивает шансы на выздоровление. Имеется в виду как выживание в первые дни после операции, так и общее выздоровление (процент пациентов, которые продолжают жить спустя пять лет после обнаружения заболевания).
Особенности операции на поджелудочной железе
Частичная резекция поджелудочной железы – одна из самых крупных и сложных операций в области хирургии брюшной полости. Длится несколько часов, после чего следует медленное восстановление несколько недель.
Существует две техники проведения операции:
В Израиле операция Уиппла включает несколько этапов. Первый подразумевает диагностическую лапароскопию. Ее цель – узнать состояние органа и определить, можно ли проводить запланированную резекцию. Если опухоль неоперабельная, на этом этапе операция заканчивается. Если хирург решит, что стоит продолжать операцию, переходят ко второму этапу – резекция головки органа.
То, что было резецировано во время операции, подвергается гистологическому анализу в лаборатории. Это позволяет определить оптимальное лечение на основе состояния здоровья пациента.
Завершение операции на поджелудочной железе – подсоединение тела поджелудочной железы, желудка, оставшихся желчных протоков к тощей кишке (jejunum, средний отдел тонкой кишки), которая находится между двенадцатиперстной и подвздошной кишкой (ileum, нижний отдел тонкой кишки). Таким образом врач практически заново выстраивает пищеварительную систему больного.
Анестезия и длительность операции на поджелудочной железе
При проведении операции по частичной резекции поджелудочной железы используется общий наркоз. Продолжительность операции составляет примерно 5-6 часов.
Шансы на выздоровление
Резекция головки, хвоста – довольно опасная операция. Согласно исследованиям, лечение в крупном медицинском центре (таком, как Тель-Авивский медицинский центр), где работают опытные врачи, уменьшает риски.
Чтобы свести к минимуму вероятность осложнений, стоит сообщить хирургу, анестезиологу все данные анамнеза. Это позволит подобрать оптимальное лечение, полностью соответствующее состоянию больного.
После операции на поджелудочной железе
По окончанию операции пациент переводится на два часа в послеоперационную палату. Там он отходит от наркоза, после чего поступает в отделение интенсивной терапии, где около суток находится под строгим наблюдением врачей. Затем пациента переводят в отделение хирургии, где ему будут помогать сидеть в кровати, кресле. По возможности рекомендуется ходить, двигаться.
Как правило, проведение операции нуждается в госпитализации в течение 1-2 недели.
После выписки
После операции Уиппла и связанных с ней изменений в организме, многие пациенты теряют вес. В большинстве случаях требуется около 1,5 месяца, чтобы пищеварительная система приспособилась к новому строению, возобновила нормальное функционирование. Поэтому принимать пищу стоит небольшими порциями и перекусывать между трапезами. Можно обратиться к клиническому диетологу за консультацией.
После резекции поджелудочной железы, особенно в случаях, когда селезенка также была вырезана, проводится прививка для предотвращения инфекций. Некоторым пациентам необходимо принимать инсулин, энзимы, что поможет пополнить их недостаток в организме.
Если температура тела свыше 38 градусов, стоит обратиться в отделение, посоветоваться с дежурным врачом. При необходимости нужно обратиться в приемный покой для проведения дальнейшего обследования.
Рак поджелудочной железы
Поджелудочная железа представляет собой орган брюшной полости, расположенный за желудком, размерами 15-22 см. Она состоит из головки, тела и хвоста. В составе поджелудочной железы выделяют два типа клеток. Одни отвечают за продукцию ферментов, участвующих в пищеварении (экзокринная часть). Вторые выделяют в кровь важные гормоны, регулирующие обмен веществ, такие как инсулин и глюкагон (эндокринная часть).
.jpg)
Опухоли из клеток, производящих гормоны классическим раком не являются. Это отдельная группа заболеваний, которые входят в широкое понятие “нейроэндокринные опухоли”.
Причины развития рака поджелудочной железы мало изучены. Известно, что такие факторы как курение табака, злоупотребление алкоголем, низкая физическая активность, ожирение, хронический панкреатит и контакт с тяжелыми металлами могут повышать риск развития опухоли.
Также рак поджелудочной железы чаще развивается у лиц с отягощенной генетикой. Особенно подвержены развитию опухоли пациенты с наследственными опухолевыми синдромами, такими как синдром Линча и наследственный рак молочной железы.
Рак поджелудочной железы обычно встречается у лиц старше 45 лет. Случаи заболевания у более молодых лиц являются редкостью, но также встречаются в клинической практике.
СИМПТОМЫ.
На ранних стадиях болезнь часто может протекать бессимптомно. На более поздних могут появиться жалобы на боль в животе, тошноту, рвоту и потерю веса.
Часто первым проявлением болезни становится желтуха. Ее развитие связано со сдавлением опухолью желчных протоков. Более редким проявлением дебюта заболевания может быть впервые выявленный диабет. Как правило, это проявляется повышенной жаждой, частым и обильным мочеиспусканием, сухостью во рту.
ДИАГНОСТИКА.
При подозрении на опухоль поджелудочной железы доктор помимо общего осмотра может назначить дополнительные обследования:
УЗИ брюшной полости – позволяет оценить наличие и примерные размеры опухоли в животе.
Компьютерная томография (КТ) / Магнитно-резонансная томография (МРТ) – позволяют с высокой точностью оценить наличие, размер и расположение опухоли и возможных метастазов. КТ и МРТ являются золотым стандартом обследования в онкологии.
Магнитно-резонансная холангиопанкреатография (МРХПГ) – метод позволяющий изучить желчные протоки. Важный метод при диагностике желтух, исключения воспалительных изменений желчного дерева.
Эндоскопическаяультрасонография (ЭУС) – способ визуализации желудка и начальных отделов тонкой кишки с помощью гибкого зонда (эндоскопа) с видеокамерой и УЗИ-датчиком.В некоторых случаях позволяет сделать вывод о стадии опухоли.
Эндоскопическая ретроградная холангиопанкреатография (ЭРХПГ) – метод позволяющий оценить состояние желчных протоков и протока поджелудочной железы. Может понадобиться при решении вопроса о стентировании протоков.
Диагностическая лапароскопия – хирургическая операция в ходе которой видеоаппаратура погружается в брюшной полость для непосредственной оценки опухоли и/или метастазов, либо с целью биопсии (забора опухолевого материала).
Исследование крови на уровень онкомаркеров. Основные маркеры, которые по научным данным связаны с раком поджелудочной железы – Са19.9, РЭА. Сa 19.9 имеет наибольшее значение и часто используется хирургами для контроля успешности операции и в качестве косвенного маркера рецидива болезни. При этом, онкомаркеры не подходят для ранней диагностики и скрининга рака поджелудочной железы.
Биопсия – обязательный компонент диагностики перед началом лечения. В ходе прокола кожи под контролем УЗИ или КТ, либо в процессе диагностической операции, происходит получение кусочка опухоли. Этот кусочек подвергается гистологическому (ГИ) и иммуногистохимическому (ИГХ) исследованию, после чего диагноз “рак” подтверждается или опровергается. При исследовании может быть выявлена нейроэндокринная опухоль или другой процесс, например, лимфома, что глобально меняет тактику лечения пациента.
Начать специфическое лечение до результатов биопсии невозможно!
После подтверждения диагноза необходимо пройти процедуру стадирования (установления стадии), если она не была выполнена заранее. Рекомендуемая процедура включает в себя выполнение КТ трех зон (грудная клетка, брюшная полость и малый таз), либо КТ грудной клетки и МРТ брюшной полости и малого таза. Эти исследования помогают оценить распространенность опухолевого процесса, что влияет на выбор тактики лечения.
ЛЕЧЕНИЕ.
При ранних стадия (I-III) рака поджелудочной железы основным методом лечения является хирургическая операция. Существует несколько ее типов:
Данные вмешательства могут проводиться в рамках открытого доступа (большой разрез) или малоинвазивной (лапароскопической) хирургии (малые разрезы).
Во всех случаях, когда речь идет об операции хирург должен оценить возможность радикально удалить опухоль. Чаще всего ему может мешать вовлечение в рост опухоли крупных сосудов. Все опухоли могут быть разделены на 3 группы:
После операции пациентов могут беспокоить такие проблемы как потеря веса, диарея, другие нарушения пищеварения. В связи с тем, что при удалении части железы снижается количество ферментов. Пациенты, как правило, должны принимать ферменты в виде лекарства. Для определения дозы ферментных препаратов используется анализ на определение эластазы кала.
Помимо хирургического лечения при ранних стадиях всем пациентам показана химиотерапия (cм.ниже). Чаще всего она проводится после операции с целью профилактики рецидива (возврата заболевания в будущем).
Иногда химиотерапия проводится до операции с целью уменьшить объем опухоли (при погранично-резектабельном раке) и повлиять на невидимые глазом опухолевые клетки, которые могут стать источником рецидива (при резектабельном и погранично-резектабельном раке). Суммарный срок курса химиотерапии в среднем составляет 6 месяцев.
Если опухоль пациента неоперабельна, либо имеются отдаленные метастазы (печень, легкие, кости и т.д), то пациенту показана лекарственная терапия. Она направлена на увеличение продолжительности жизни и улучшение ее качества за счет уменьшения симптомов заболевания.
Основной метод лекарственного лечения – химиотерапия.
Химиотерапия предусматривает внутривенное введение в организм веществ, которые называются цитостатиками. Они нарушают процесс деления клеток, препятствуя росту опухоли.
Лечение проходит в виде циклов с введением препаратов 1 раз в 7, 14 или 21 день.
Могут использоваться как комбинированные режимы (несколько препаратов), так и монотерапия (1 препарат).
К наиболее распространенным схемам лечения при раке поджелудочной железы относятся:
2. Гемцитабин + nab-паклитаксел
6. 5-фторурацил или капецитабин
Выбор конкретной схемы зависит от индивидуальных особенностей пациента, его сохранности, сопутствующих заболеваний. Комбинированные режимы больше подходят пациентам с хорошим соматическим статусом, без значимых сопутствующих заболеваний или состояний. Монотерапия применяется у более ослабленных пациентов.
Для контроля эффективности химиотерапии каждые 2-3 цикла (6-8 недель) проводится обследование (КТ и/или МРТ). В ходе обследования оценивается динамика размеров опухоли и метастазов. При отрицательной динамике (рост опухоли) схема лечения может поменяться (смена линии).
*Химиотерапия может быть начата только у пациента в стабильном состоянии. Иногда может потребоваться коррекция симптомов на первом этапе и лишь потом переход к основному лечению. Например, пациенты с нарастающей желтухой часто требуют срочного дренирования протоков (установку специальной трубки для отведения желчи).
Иногда в лечении рака поджелудочной железы применяются и другие методы лечения, такие как таргетная терапия или иммунотерапия.
Врач может порекомендовать исследование опухолевого материала на предмет маркеров MSI/dMMR (микросателлитная нестабильность) или мутации BRCA ½ и NTRK. Эти тесты помогают определиться, будет ли опухоль чувствительна к лечению таргетными и иммунопрепаратами. Как правило, эти современные виды лечения назначаются при неэффективности классических режимов химиотерапии у пациентов, имеющих соответствующие генетические поломки (см.выше).
ЛУЧЕВАЯ ТЕРАПИЯ И РАК ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ.
Лучевая терапия имеет ограниченное применение у пациентов, страдающих раком поджелудочной железы. В некоторых случаях облучение может проводиться по следующим показаниям:
СОПРОВОДИТЕЛЬНАЯ ТЕРАПИЯ И ПАЛЛИАТИВНАЯ ПОМОЩЬ.
В ходе лечения рака поджелудочной железы пациенты могут столкнуться с рядом проблем, связанных как с самим заболеванием, так и побочными эффектами лечения.
Борьбой с осложнениями занимается мультидисциплинарная команда в составе химиотерапевта, хирурга, терапевта, нутрициолога (специалиста по питанию) и других врачей. Правильно подобранная сопроводительная терапия позволяет улучшить качество жизни пациентов даже в очень тяжелых ситуациях.
В СПб больнице РАН проводятся все виды современного лечения рака поджелудочной железы. Для осуществления лучевого метода лечения онкологи СПб больницы РАН направляют на лечение в специализированные центры.
Панкреатодуоденальная резекция
Акции
Оперативные вмешательства со скидкой 7%.
Онкоконсилиум может потребоваться как при лечении в «СМ-Клиника», так и пациентам других медицинских учреждений с целью получения альтернативного мнения.
«СМ-Клиника» предоставляет своим пациентам предоперационное обследование со скидкой до 72%!
Консультация врача-хирурга по поводу операции бесплатно!
Основные преимущества операции Уиппла
Показания
Противопоказания
Возможность проведения такой операции в «СМ-Клиника» определяется после полного обследования пациента и онкологического и терапевтического консилиума.
Подготовка и предоперационные исследования
Перед операцией ПДР пациент проходит расширенное предоперационное исследование. Оно включает ряд стандартных процедур:
Кроме этого, нужно сделать:
С результатами нужно пойти к терапевту и хирургу, посетить анестезиолога, потому что вмешательство проходит под общим наркозом.
Как проходит панкреатодуоденальная резекция?
Операция Уиппла проходит под общим наркозом и может выполняться двумя способами:
Иногда перед резекцией выполняется диагностическая лапароскопия, которая позволяет визуально оценить распространение рака за пределы поджелудочной железы. Если опухоль дала метастазы, хирург может решить не продолжать операцию.
Операция выполняется только в стационаре в условиях командной работы хирургов и онкологов. Одновременно в операционной бригаде работают 3-4 хирурга. Время выполнения операции зависит от сложности – от 3 часов.
Восстановление после панкреатодуоденэктомии
После вмешательства пациент от 3 суток проводит в отделении интенсивной терапии, а потом – от 14 суток в стационаре. Ему ставят капельницы, обеспечивают уход за дренажными трубками и швами.
В первый день после операции разрешено пить прозрачные жидкости небольшими глотками. Во второй день необходимо соблюдать нулевую лечебную диету. Начиная с третьего дня после операции можно вводить в рацион твердую пищу.
После операции рекомендована химиотерапия и облучение. Это повышает выживаемость на 10%.
Возможные осложнения
Записаться на прием онколога в «СМ‑Клиника» вы можете круглосуточно, позвонив по телефону в Санкт-Петербурге +7 (812) 435 55 55 или заполнив форму обратной связи
Сенько Владимир Владимирович ведущий хирург онколог, зам. главврача по хирургии, руководитель хирургического стационара стаж: 21 год
Осокин Антон Владимирович хирург, онколог, колопроктолог стаж: 17 лет
Гриневич Владимир Станиславович оперирующий онколог, маммолог, онкопроктолог стаж: 25 лет
Хохлов Сергей Викторович хирург, онколог, колопроктолог стаж: 23 года
Колосовский Ярослав Викторович хирург, онколог, маммолог, колопроктолог стаж: 15 лет
Арамян Давид Суренович хирург, колопроктолог, онколог, маммолог стаж: 11 лет
Бойко Александр Александрович оперирующий онколог стаж: 10 лет
Шишкин Андрей Андреевич оперирующий онколог стаж: 11 лет
Михайлов Алексей Геннадьевич оперирующий онколог, маммолог стаж: 20 лет
Протасов Дмитрий Андреевич оперирующий гинеколог стаж: 30 лет
| Прием (осмотр, консультация) врача-онколога первичный, лечебно-диагностический, амбулаторный | 1750 |
При подозрении на опухолевое заболевание или при наличии подтверждающих диагноз исследований вы можете обратиться к профильному онкологу нашего центра. Врачи специализируются на онкозаболеваниях мужской и женской репродуктивных систем, мочевыделительной и пищеварительной систем, болезнях крови и кожных покровов.
Панкреатодуоденальная резекция. Первые шаги в покорении вершины.
В историческом обзоре приводятся в хронологической последовательности этапы рождения и эволюции панкреатодуоденальной резекции. Описаны первые опыты проведения данного вмешательства корифеями хирургии XIX-XX веков.
Панкреатодуоденальная резекция. Первые шаги в покорении вершины.
Pancreatoduodenal resection. The first steps in conquest of the top.
Светлой памяти хирурга Геннадия Алексеевича Старченко посвящается.
Панкреатодуоденальная резекция в любых вариантах и условиях выполнения уже многие десятилетия остается для большинства хирургов объективно одним из самых технически сложных оперативных вмешательств, а субъективно – одной из сверкающих вершин хирургического мастерства. Вершины, манящей своей высотой и риском хирургов молодых и никогда не отпускающей своим притяжением хирургов зрелых, уже не раз покорявших ее.
Молодым докторам известно из книг и рассказов, а зрелые знают не понаслышке, что именно панкреатодуоденальная резекция в каждом из своих этапов содержит более чем значительное число потенциальных рисков, при неблагоприятном стечении обстоятельств трансформирующихся в весьма трагические последствия. Не многие из оперативных вмешательств требуют от хирурга одновременного опыта диссекции патологически измененных тканей при различных вариантах анатомии, навыков контроля массивных кровотечений, шва структур пищеварительной трубки и сосудистого шва при уверенном и прецизионном их исполнении.
Являясь во многом знаковым оперативным вмешательством, панкреатодуоденальная резекция обладает не менее одиозной историей. Историей, полной побед и поражений, возвышенного оптимизма и драматического неверия. Целая эпоха личностей и событий открывается нам при изучении рождения и эволюции этой хирургической операции. Эпоха, символами которой стали такие имена как F. Trendelenburg, A. Codivilla, W. Halsted, W. Kausch, A. Whipple.
ВЕКТОРЫ ДВИЖЕНИЯ
Принято считать, что современная история панкреатодуоденальной резекции берет свое начало со второй половины XIX века. В то самое время, когда хирурги зачастую являлись пионерами не только в сфере собственно оперативного искусства, но и в таких областях как физиология и патология.
В начале прошлого столетия весьма догматичным было представление о двенадцатиперстной кишке как о жизненно необходимом, так называемом эссенциальном органе. Данное суждение физиологов в сочетании с авторитетным мнением анатомов о технической невозможности удаления части или всей двенадцатиперстной кишки исключало, казалось бы, любые фантазии на тему хирургического удаления опухолей панкреатодуоденальной зоны. Тем не менее неординарность мышления и упорство хирургов, как это случалось не раз, смогли пробить брешь в стене схоластических представлений, и в 1907 году Desjardins и в 1908 году Sauve в анатомическом эксперименте убедительно доказали техническую возможность удаления двенадцатиперстной кишки и сопредельных структур. В свою очередь в качестве контраргумента представлениям физиологов об эссенциальности двенадцатиперстной кишки в 1918 году L. R. Dragstedt представил результаты экспериментов на собаках: оказывается после полного удаления двенадцатиперстной кишки подопытные животные, как это ни странно, остаются живы. Интересно, что после работы L. R. Dragstedt публикации последубыли посвящены различным аспектам удаления лишь части двенадцатиперстной кишки, вплоть до 1937 года, когда А. Brunschwig произвел тотальную дуоденэктомию, но уже не в эксперименте, а в качестве полноценной хирургической операции.
Принципиальным вопросом, стоявшим на повестке дня практически с самого рождения панкреатодуоденальной резекции, был вопрос о судьбе главного панкреатического протока. По аналогии с представлениями об эссенциальности двенадцатиперстной кишки существовало устойчивое мнение о невозможности существования организма без поступления в пищеварительную трубку панкреатического сока. Однако экспериментальными исследованиями конца XIX – начала ХХ века была продемонстрирована вполне удовлетворительная переносимость животными полной перевязки вирсунгова протока. Но, увы, результаты этих экспериментов оказали скорее негативное, чем позитивное действие на прогресс хирургической мысли: на два десятилетия прочно укрепилась идея о безальтернативной целесообразности необратимой окклюзии главного панкреатического протока. Более того, подавляющее большинство хирургов вплоть до 1940-х годов полагали, что попытки соединения просвета двенадцатиперстной или тонкой кишки с вирсунговым протоком заведомо обречены на неудачу вследствие активации панкреатических проферментов дуоденальным или кишечным соком с практически абсолютной неизбежностью несостоятельности такого анастомоза. Дополнительным фактором, ограничивающим возможность формирования панкреатикодуодено- (энтеро-) анастомоза было, по их мнению, отсутствие брюшинного покрова на задней стенке двенадцатиперстной кишки. Однако данные рассуждения, и сегодня представляющиеся нам вполне логичными, уже и в те далекие времена противоречили данным клинических наблюдений и экспериментов. А эти данные свидетельствовали о том, что лигирование вирсунгова протока в подавляющем большинстве случаев приводит к формированию наружнего панкреатического свища со всеми вытекающими из этого последствиями. Справедливости ради следует заметить, что уже в 1909 году независимо друг от друга R. Coffey и Hans Kehr высказали вполне логичную идею о возможности имплантации культи поджелудочной железы в просвет пересеченной тонкой кишки, что явилось своего рода пророчеством для будущих инвагинационных панкреатоэнтероанастомозов. Только в 1941 году V. Hunt, поборов предубеждения коллег, внедрил панкреатикоэнтеростомию в клиническую практику, резко уменьшив тем самым число наружных панкреатических свищей. К этому же времени относятся и экспериментальные работы, в ходе которых было показано, что панкреатикоэнтероанастомозы потенциально и фактически безопасны. При морфологических исследованиях зоны экспериментального панкреатикоэнтероанастомоза научной группой во главе с A. Whipple было установлено, что область сформированного всего двумя шелковыми швами (!) соустья менее чем за 24 часа полностью покрывается пролиферирующим эпителием панкреатического протока. Тем самым дискуссия о целесообразности лигирования или анастомозирования главного панкреатического протока была прекращена за явным преимуществом последнего.
Весьма непростой задачей, которую пришлось решать пионерам панкреатодуоденальной резекции был выбор оптимального способа обеспечения пассажа желчи в пищеварительную трубку. Первые варианты решения представляли собой самое простое с точки зрения оперативной хирургии решение – формирование холецистогастроанастомоза. Однако уже в первой серии операций, выполненных A. Whipple, один из пациентов умер при явлениях прогрессирующего холангита, холангиогенного сепсиса при стенозировании подобного анастомоза. Данный опыт послужил причиной отказа от формирования анастомозов билиарного тракта с желудком практически с самого начала внедрения панкреатодуоденальной резекции в клиническую практику. В дальнейшем предлагались многочисленные способы формирования билиодигестивных анастомозов, с большим или меньшим успехом препятствовавшие рефлюксу кишечного содержимого в желчные протоки, вплоть до признанной на сегодняшний день «золотым стандартом» гепатикоэнтеростомии на отключенной по Ру петле.
Еще одной проблемой, преследовавшей панкреатодуоденальную резекцию практически с самого начала, была проблема пептических язв гастроэнтероанастомоза. Данное осложнение в течение нескольких десятилетий являлось, увы, неизбежным спутником почти каждой третьей или четвертой панкреатодуоденальной резекции. Строго говоря пептические язвы не являются видоспецифическим осложнением для данного оперативного вмешательства. Однако, поскольку панкреатодуоденальная резекция имела исходно своей составной частью дистальную резекцию желудка, то очевидно, что первая операция неизбежно несет в себе потенциально возможные негативные последствия второй. При этом изначально к факторам развития пептических язв относили способ реконструкции пищеварительной трубки, последовательность анастомозов и даже место формирования анастомоза на культе желудка. Однако с течением времени стало очевидно, что основной причиной развития пептических язв гастроэнтероанастомоза служит так называемая экономная, а по сути – неадекватная по объему удаляемой дистальной части, резекция желудка. На справедливость данного положения весьма категорически указывал еще С.С. Юдин, подчеркивая, что только высокая (более 2/3) резекция желудка может служить наиболее надежным средством профилактики пептических язв гастро-энтероанастомоза.
Представив себе, хотя бы примерно, масштабы решаемых проблем, череду событий и лиц, исторически связанных с рождением и эволюцией панкреатодуоденальной резекции, мы понимаем, что достаточно сложно назвать «то самое» событие, открывшее, по сути, новую эпоху в абдоминальной хирургии. Однако каждый волен расставлять приоритеты сам, и нам остается лишь привести в хронологической последовательности объективные факты хирургической истории – ступени покорения вершины.
СОБЫТИЯ, ЛИЦА И ЭПОНИМЫ
Все случилось не вдруг и не вследствие некоего внезапного озарения или счастливой случайности. Напротив, даже незначительным поступательным движениям в хирургии поджелудочной железы предшествовали долгие годы, а порой и десятилетия поистине диалектического накопления критической массы анатомических, физиологических и экспериментальных исследований. Попытки же использования известного принципа «Sturm und Drang» в отношении поджелудочной железы неизбежно завершались драматическими неудачами, породившими в хирургическом сообществе нового времени весьма характерные максимы типа «Ешь, когда сможешь. Спи, когда сможешь. Но не оперируй поджелудочную железу» или «Господь поместил поджелудочную железу в глубине живота потому, что не желал встречи хирурга с ней».
Эпоха ренессанса, разрушитель средневековых схоластических догм, оставила свой след и в истории изучения поджелудочной железы. В 1642 году урожденный немец Johann Georg Wirsung, преподаваший в то время анатомию в Падуанском университете, вместе со своими ассистентами Thomas Bartolini и Moritz Hoffmann описал проток поджелудочной железы, впадающий в двенадцатиперстную кишку. Изначально исследователи были убеждены, что проток был создан Творцом исключительно для свободного истекания флегмы из селезенки в кишечник. Однако в поздних своих работах J. Wirsung уже определенно высказывался об экзокринной функции исследуемого органа, по сути характеризуя его именно как железу. Тем не менее, истинное значение открытия J. Wirsung было оценено лишь два века спустя, когда Albrecht Von Haller показал наличие соединения главного панкреатического протока и общего желчного протока при впадении в двенадцатиперстную кишку, Paul Langerhans опубликовал первое описание гистологической структуры поджелудочной железы, а великий Claude Bernard доказал основополагающее значение поджелудочной железы в процессе пищеварения. Именно тогда, в середине XIX века, в знак уважения к научным заслугам J. Wirsung голландец Johannes Van Horne и француз Jean Riolan впервые ввели термин «Wirsungianus – вирсунгов проток».
Начало клинических исследований в отношении патологии поджелудочной железы принято связывать с именем Giovanni-Battista Morgagni, описавшим в 1744 году опухоль головки поджелудочной железы как причину механической желтухи. Любопытно, что уже тогда ученый пришел к заключению, вполне актуальному и в наше время: к моменту появления желтухи опухоль достигает таких размеров и степени инвазии в окружающие структуры, что ее резекция не представляется возможной. Первое микроскопическое описание аденокарциномы поджелудочной железы в 1858 году представил американец Jacob M. Da Costa, а в 1889 году француз Louis Terrier описал феномен дилатации желчного пузыря у пациентов с опухолью головки поджелудочной железы. Практически одновременно, в 1890 году, швейцарец Ludwig Courvoisier пришел к заключению о том, что при наличии желтухи, обусловленной обструкцией общего желчного протока сокращенный желчный пузырь указывает на наличие холедохолитиаза, а дилатированный желчный пузырь – на опухолевую этиологию желтухи. С этого времени хорошо знакомое нам клиническое проявление опухолей билиопанкреатодуоденальной зоны носит название триады Курвуазье-Терье. Любопытно, что для опухолей именно головки поджелудочной железы французы Louis Bard и Audrien Pic несколько раньше, в 1888 году, совместно описали характерную клиническую картину, сейчас известную как синдром Бара-Пика, включающую диспепсию, признаки ферментной недостаточности, боли в правом верхнем квадранте живота, желтуху, ахолию, увеличенный желчный пузырь.
Однако, как было сказано нашим аргентинским коллегой Ernesto Rafael Guevara de la Serna, почти столетие спустя: «Если вы сможете найти путь без каких-либо препятствий, он, вероятно, никуда не ведет». Время неумолимо шло вперед и всплеск хирургической пассионарности второй половины XIX столетия, ассоциирующийся сегодня с такими именами как Th. Billroth, Th. Kocher, C. Roux, F. Trendelenburg, W. Halsted, склонил чашу весов от пессимистичной паллиативности к поиску радикального решения проблемы опухолей панкреатодуоденальной зоны. Штурм вершины начался. Собственно начало эпохи хирургической панкреатологии принято датировать 1882 годом, когда Friedrich Trendelenburg выполнил первую успешную дистальную резекцию поджелудочной железы. В ходе полуторачасовой операции была удалена массивная веретеноклеточная опухоль, инвазирующая хвост поджелудочной железы, единым блоком с дистальной частью органа. Удаление селезенки изначально запланировано не было, но повреждение ее паренхимы с последующим кровотечением потребовало выполнение спленэктомии. В 1886 году американский хирург Nicolas Senn в монографии «The Surgery of the Pancreas» отметил, что «наиболее благоприятные условия для резекции поджелудочной железы имеются при первичной локализации поражения в хвосте», подчеркнув уже очевидные для большинства хирургов того времени доступность выделения и резекции дистальных отделов органа, отсутствие необходимости панкреатической, билиарной и кишечной реконструкции, объективно меньший риск массивного кровотечения во время вмешательства.
В 1889 году Giuseppe Ruggi произвел первую энуклеацию опухоли головки поджелудочной железы. Пятью годами позднее другой итальянский хирург Domenico Biondi выполнил первую полноценную парциальную резекцию головки поджелудочной железы с оставлением двенадцатиперстной кишки интактной.
Заслуженный успех W. Halsted был воспринят хирургическим сообществом викторианской эпохи с заметным энтузиазмом, как закономерное начало очередного этапа в развитии хирургии поджелудочной железы. Можно себе представить смущение многочисленных читателей хирургических журналов зарождающегося нового века, узнавших из запоздавшего почти на десять лет отчета, о том, что всего пятью днями раньше операции W. Halsted итальянским хирургом Alessandro Codivilla было выполнено вмешательство, отражавшее принципиально иной подход к лечению опухолей панкреатодуоденальной зоны и впоследствии получившее название панкреатодуоденальной резекции. Как это нередко бывает, карты неторопливого исторического пасьянса были смешаны одним молодым и смелым экспромтом.
Тридцатисемилетний итальянский хирург Alessandro Codivilla, ученик G. Ruggi, обладавший к тому времени уже значительным опытом дистальных резекций желудка, 7 февраля 1898 года выполнил лапаротомию пациенту с нарушением желудочной эвакуации и подозрением на опухоль антрального отдела желудка seu опухоль головки поджелудочной железы. Интраоперационно была диагностирована «эпителиома головки поджелудочной железы», распространяющаяся на луковицу двенадцатиперстной кишки. Учитывая факт распространения опухоли на стенку двенадцатиперстной кишки, A. Codivilla воздержался от энуклеации и выполнил резекцию en bloc дистальной части желудка, проксимальной части двенадцатиперстной кишки с участком головки поджелудочной железы и терминальной части общего желчного протока. Реконструктивный этап операции включал в себя формирование холецисто-энтероанастомоза на отключенной по Ру петле и гастро-энтероанастомоза. Главный панкреатический проток был лигирован, культя поджелудочной железы закрыта отдельными швами. В послеоперационном периоде отмечалось формирование наружного панкреатического свища в операционную рану. Истечение панкреатического секрета в сочетании с перманентной диареей привели к прогрессирующему истощению пациента и летальному исходу на 21 сутки послеоперационного периода. К сожалению эта первая описанная в литературе панкреатодуоденальная резекция оказалась последней в хирургическом творчестве Alessandro Codivilla, сконцентрировавшем свое внимание в последующие годы сугубо на проблемах ортопедии.
Как ни странно на первый взгляд, но именно хирургии, в значительно большей степени, чем другим областям медицины, свойственен консерватизм. Несмотря на широкий резонанс, операции A. Codivilla и W. Halsted были расценены как нечто эксвизитное: утверждения Johann von Mikulicz—Radecki в отношении принципиальной неоперабельности опухолей панкреатодуоденальной зоны не подвергались сомнению. Однако первые годы наступившего двадцатого столетия принесли целую череду новых фактов, доказывавших возможность и необходимость выполнения панкреатодуоденальной резекции. В 1904 году предложенное Caesar Roux Y-образное выключение из пассажа сегмента тонкой кишки было использовано для формирования билиодигестивного анастомоза и продемонстрировало наилучший вариант профилактики восходящего холангита. Pierre Duval в 1906 году применил при парциальной резекции головки поджелудочной железы прием мобилизации двенадцатиперстной кишки, предложенный тремя годами ранее E. Th. Kocher. В 1907 году был опубликован отчет хирурга из Кенигсберга Oscar Ehrhardt об успешной парциальной панкреатдуоденэктомии, выполненной им «по необходимости». Во время релапаротомии у пациентки, ранее перенесшей гастро-энтеростомию по поводу нерезектабельного рака пилорического отдела желудка с прорастанием в головку поджелудочной железы O. Ehrhardt резецировал антральный и пилорический отделы желудка, луковицу и участок нисходящего отдела ДПК, а также часть головки поджелудочной железы. К сожалению, исход этой операции остался неизвестен.
В это же время Abel Desjardin опубликовал первое анатомическое обоснование формирования инвагинационного панкреато-энтероанастомоза как этапа одномоментной панкреатодуоденальной резекции. Свой вариант техники формирования панкреатико-энтероанастомоза, правда в качестве отсроченного этапа операции, предложил также в анатомическом эксперименте год спустя Louis Sauve, а в 1909 году Robert Coffey представил отчет о серии весьма демонстративных экспериментов на собаках, в ходе которых автор в качестве реконструктивного этапа панкреатодуоденальной резекции успешно использовал формирование инвагинационного панкреато-энтероанастомоза.
И, наконец, как результат 11-летнего периода анатомических, экспериментальных и клинических исследований в 1909 году уроженцем Восточной Пруссии Walther Carl Eduard Kausch, по иронии судьбы – зятем J. von Mikulicz—Radecki, была выполнена первая успешная гастропанкреатодуоденальная резекция. В свои сорок два года W. Kausch был уже известен в хирургическом сообществе более чем полусотней публикаций по проблемам абдоминальной хирургии, в том числе и монографией «Функциональные результаты операций на желудке».
Пациент был выписан через два месяца после операции и прожил еще семь месяцев, скончавшись в конечном итоге от прогрессирующего холангита. Нетрудно заметить насколько разительно операция W. Kausch отличалась как от вмешательства, выполненного A. Codivilla, так и от вмешательства W. Halsted и сходных с ним по объему операций W. Koerte, B. Riedel, A. Mayo—Robson, W. Mayo, В.Ц. Томашевича и В.И. Добротворского. Прежде всего, операция немецкого хирурга была запланированным вмешательством, сознательно разделенным на два этапа при полном осознании величины и факторов операционного риска. По сути W. Kausch был первым хирургом, доказавшим целесообразность билиарной декомпрессии в качестве подготовки перед радикальной операцией при опухолях периампулярной зоны. В законченном виде вмешательство W. Kausch представляло собой не только радикальное удаление опухоли, но и полноценную реконструкцию пищеварительной трубки с успешным решением вопроса «ахиллесовой пяты» панкреатодуоденальной резекции – анастомозирования панкреатического протока с кишечной трубкой. Данные обстоятельства позволяют считать именно W. Kausch автором первой успешной панкреатодуоденальной резекции, а его имя – эпонимическим названием этой операции. К сожалению, методике панкреатодуоденальной резекции не дано было получить дальнейшее развитие в руках самого автора: W. Kausch, сломленный чередой личных трагедий, был вынужден оставить хирургическую практику.
В истории покорения вершины вновь наступил период затишья, на этот раз – двадцатипятилетний. За это время в литературе лишь трижды встречалось упоминание об успешных радикальных операциях по поводу периампулярных опухолей. В 1914 году G. Hirschel впервые выполнил одномоментную панкреатодуоденальную резекцию, а в 1922 году O. Tenani повторил двухэтапный ее вариант. В 1913 году русский хирург Иван Иванович Греков произвел субтотальную панкреатэктомию с «оставлением полоски паренхимы железы шириной 1 см вдоль медиального края двенадцатиперстной кишки» по поводу местнораспространенного опухолевого процесса в теле и хвосте железы.
Несмотря на значительный прогресс в техническом аспекте выполнения панкреатодуоденальной резекции, объективные на то время трудности своевременной диагностики опухолей панкреатодуоденальной зоны и периоперационного ведения пациентов служили серьезными препятствиями даже для самых горячих оптимистов и приверженцев идеи радикальных операций. В 1911 г. американским хирургом Bertram M. Bernheim была предпринята первая попытка осмотра брюшной полости цистоскопом для диагностики опухолевого поражения гепатопанкреатодуоденальной зоны. Однако идея B. Bernheim слишком сильно опередила свое время. В большинстве случаев хирурги сталкивались с уже весьма распространенным опухолевым процессом и, не решаясь на рискованную резекцию в условиях весьма ограниченных ресурсов по выхаживанию пациентов, ограничивались либо сугубо эксплорацией, либо формированием билиодигестивных анастомозов. Лишь изредка в литературе появлялись сообщения об очередной трансдуоденальной резекции периампулярной опухоли, как правило – с малоутешительным результатом. Тема панкреатодуоденальной резекции была отложена ad meliora tempora.
Тем не менее, весьма значимыми вехами для последующих штурмов вершины явились в первые десятилетия ХХ века работы Ottorini Tenani и Lester R. Dragstedt. В 1918 году O. Tenani предложил принципиально новый вариант билиодигестивного анастомоза – соединение общего желчного (печеночного) протока с тонкой кишкой вместо применявшейся в то время повсеместно холецистоэнтеростомии. Было замечено, что формирование холедохо (гепатико)-энтероанастомоза в сочетании с выключением сегмента тонкой кишки по методу C. Roux резко уменьшило число случаев послеоперационного холангита. Кроме этого O. Tenani явился пионером пред- и интраоперационных гемотрансфузий и первым хирургом, доказавшим необходимость целенаправленной инфузионной и нутритивной подготовки пациентов к объемным оперативным вмешательствам. В свою очередь Lester R. Dragstedt в серии наглядных экспериментов по тотальной дуоденэктомии у собак, датируемых 1918 годом, доказал отсутствие неких эссенциальных свойств двенадцатиперстной кишки: никаких нарушений жизненно важных функций и необратимых расстройств пищеварения после полного удаления этой части пищеварительной трубки у животных не возникало. В 1929 году, после описания двумя годами ранее R. Wider морфологического субстрата и клинической симптоматики инсулин-продуцирующих опухолей, американский хирург Roscoe Graham выполнил первую энуклеацию инсулиномы, тем самым продемонстрировав принципиальную возможность диагностики опухолей поджелудочной железы еще до оперативного вмешательства.
Начало «лучших времен» для панкреатодуоденальной резекции в первой половине ХХ столетия неразрывно связывают с именем Allen Oldfather Whipple и с 1934 годом, когда эта операция уже навсегда вернулась в клинику. В 1935 году хирурги из Нью-Йорка – A. Whipple, W. Parsons и C. Mullins – опубликовали работу под названием «Лечение карциномы фатерова сосочка», в которой представили двухэтапную технику радикальной резекции периампулярных опухолей. A. Whipple, основавший в начале 1930-х междисциплинарную рабочую группу по изучению заболеваний гепатопанкреатобилиарной системы, был уже широко известен как автор трудов по патологии, клинике и лечению опухолей поджелудочной железы (до сих пор классическим является описание клинической симптоматики инсулиномы – «триада Whipple»). Не менее широко был известен А. Whipple как решительный противник трансдуоденального удаления периампулярных опухолей, считавший перспективными при данной патологии лишь радикальные резекции панкреатодуоденального комплекса.
В своем отчете 1935 года А. Whipple, W. Parsons и C. Mullins обобщили опыт трех панкреатодуоденальных резекций, в первых двух случаях (1934 год) сопровождавшихся летальными исходами. Все три операции имели общие черты. На первом этапе формировались различные варианты билиодигестивных анастомозов для разрешения желтухи: холедоходуоденостомия с холецистостомией или холецистогастростомия. На втором этапе проводилась собственно резекция панкреатодуоденального комплекса, но также в различном объеме и с различными вариантами реконструкции.
У первой пациентки была выполнена гемициркулярная резекция стенки двенадцатиперстной кишки с частью головки поджелудочной железы и дистальной частью холедоха; культя поджелудочной железы была подшита к дефекту в стенке двенадцатиперстной кишки. Летальный исход после первой операции наступил в течение первых тридцати часов вследствие несостоятельности сформированных кетгутом анастомозов и перитонита.
У второго пациента после выполнения парциальной дуоденэктомии и резекции головки поджелудочной железы последняя была ушита, а оставшиеся участки двенадцатиперстной кишки соединены между собой. Возникновение стойкого нарушения желудочной эвакуации потребовало выполнения третьей операции – гастро-энтеростомии. Летальный исход наступил спустя полгода при явлениях холангита с развитием холангиогенных абсцессов печени.
У третьего пациента были произведены практически полное удаление двенадцатиперстной кишки, формирование гастро-энтероанастомоза и ушивание культи поджелудочной железы. В раннем послеоперационном периоде пациент был подвергнут релапаротомии по поводу парапанкреатического абцесса, трансформировавшегося в наружный панкреатический свищ. С течением времени свищ закрылся, пациент был выписан и прожил более двух лет, скончавшись от метастатического поражения печени.
Мы видим, как далеки были эти первые операции, выполненные A. Whipple от вмешательства, которое сегодня принято называть «the Whipple’s procedure». Тем не менее, мы отдаем сегодня дань уважения мужеству хирурга, представившему на суд коллег свой весьма неутешительный отчет и при этом непреклонно продолжавшего поиски новых путей к покорению вершины. В 1938 году A. Whipple для предупреждения послеоперационного холангита использовал Ру-петлю тонкой кишки при формировании билиодигестивного анастомоза, а в 1940 году незапланированно выполнил свою первую одномоментную панкреатодуоденальную резекцию.
Нетрудно заметить одну общую черту всех первых панкреатодуоденальных резекций – операций A. Codivilla, W. Kausch, A. Whipple – обязательное сохранение дистальной части двенадцатиперстной кишки. Химера технической невозможности и непереносимости для организма пациента тотальной дуоденэктомии достаточно прочно обосновалась в умах хирургов начала двадцатого века. Лишь благодаря выполненной в 1937 году Alexander Brunschwig анатомической резекции поджелудочной железы на уровне перешейка с тотальной дуоденэктомией вопрос о возможности проведения полноценной панкреатодуоденальной резекции был закрыт.
Как уже обсуждалось выше решение вопроса о судьбе остающейся после резекции головки большей части поджелудочной железы было крайне сложным и при этом принципиально важным. Упорные попытки копирования техники ушивания культи с модели дистальной резекции железы на панкреатодуоденальную резекцию оказались неприемлемыми, как минимум, по причине почти неизбежного развития парапанкреатических абсцессов и наружных панкреатических свищей. С другой стороны, горький опыт первых неудач и аргументированные сомнения заставляли хирургов снова и снова отказываться от попыток формирования панкреатико-энтероанастомозов еще весьма длительное время. Так, A. Whipple, лишь спустя восемь лет после первой операции, в 1942 году, выполнил панкреатодуоденальную резекцию с двухрядным панкреатико-энтероанастомозом «конец в бок».
Свой окончательный вид с классическим формированием панкреатико-энтероанастомоза, гастро-энтероанастомоза и холедохо-энтероанастомоза на одной кишечной петле Whipple’s procedure получила после двенадцати лет эволюции. Всего за время своей хирургической карьеры A. Whipple было выполнено 37 панкреатодуоденальных резекций с послеоперационной летальностью в 33%. В 1946 году была опубликована статья A. Whipple «Observations on radical surgery for lesions of the pancreas», в которой он обобщил собственный опыт выполнения панкреатодуоденальных резекций и представил оптимальный с его точки зрения вариант выполнения данного вмешательства. Принципиальное значение при выполнении панкреатодуоденальной резекции, с точки зрения A. Whipple, имеют: 1) полное удаление двенадцатиперстной кишки и головки поджелудочной железы, 2) восстановление пассажа панкреатического сока в кишечную трубку формированием панкреатико-энтероанастомоза, 3) предпочтение формирования гепатико-энтероанастомоза формированию холецисто-энтероанастомоза с целью профилактики послеоперационного холангита.
В настоящее время известно более двухсот модификаций панкреатодуоденальной резекции. Тем не менее как в профессиональной литературе, так и в доступных для пациентов источниках в качестве названия вмешательства прочно укрепился эпоним «операция Whipple (Whipple’s procedure)». Справедливо ли это? Ведь первым хирургом, выполнившим панкреатодуоденальную резекцию, пусть и экспромтом, был A. Codivilla. А первым хирургом, запланировавшим и выполнившим по предварительному плану билиарную декомпрессию, а затем панкреатодуоденальную резекцию, является W. Kausch. К слову, в немецкоговорящих странах фамилия Kausch и сегодня служит непременным эпонимом для обозначения панкреатодуоденальной резекции… но в обязательном сочетании с фамилией Whipple (Kausch – Whipple – Operation). Почему же все-таки Whipple?
Именно Allen Oldfather Whipple, как руководитель созданной им междисциплинарной рабочей группы по изучению патологии, клиники и хирургии гепатопанкреатобилиарной зоны, является пионером в обосновании и клиническом внедрении системного подхода в диагностике и лечении периампулярных опухолей. Именно A. Whipple был первым, кто решительно отстаивал необходимость резекции панкреатодуоденального комплекса и порочность парциальных резекций головки поджелудочной железы, сегментарных резекций двенадцатиперстной кишки и локальных резекций большого дуоденального сосочка при злокачественных новообразованиях данной области. Наконец именно A. Whipple принадлежит приоритет в формулировке трех вышеприведенных классических постулатов панкреатодуоденальной резекции. Полтора десятилетия упорного и целенаправленного движения в одной из самых сложных областей хирургии, способного стать примером несгибаемой воли и профессионального мужества, и его результаты, не потерявшие своей актуальности и по сей день, дают нам полное основание называть панкреатодуоденальную резекцию «операцией Whipple». Тем не менее, имя A. Whipple стало достоянием уже уходящей эпохи, а история покорения вершины продолжалась.
В 1946 году J. Waugh и W. Cladett описали первую панкреатодуоденальную резекцию, выполненную по всем канонам онкохирургии, c одномоментным удалением антрального отдела желудка, общего желчного протока, желчного пузыря, двенадцатиперстной кишки и головки поджелудочной железы единым блоком. Очевидно, что при уже определенном основном векторе движения дальнейшие исследования имели своей целью улучшение непосредственных и отдаленных результатов панкреатодуоденальной резекции, поскольку в течение достаточно короткого времени стало очевидным, что как непосредственные, так и отдаленные результаты операции остаются, увы, мало впечатляющими. Резектабельность вследствие местного распространения опухоли не превышает десяти процентов, послеоперационная летальность остается на уровне и выше двадцати процентов, а пятилетняя выживаемость вследствие локального рецидива или диссеминации составляет не более пяти процентов. В этой связи с целью повышения хирургического радикализма в 1942 году впервые было предложено и выполнено оперативное вмешательство в объеме тотальной панкреатдуоденэктомии. 19 июня 1942 года Eugene Watson Rockey первым произвел полное удаление поджелудочной железы по поводу аденокарциномы тела и головки. Первый опыт оказался неудачным – пациент скончался в ближайшем послеоперационном периоде. 14 июля того же года James Taggart Pristley выполнил тотальную панкреатэктомию при мотивированном подозрении на наличие инсулиномы. В ткани удаленной поджелудочной железы действительно была обнаружена искомая опухоль размерами 8 × 5 × 5 мм. После операции пациентка прожила еще двадцать девять лет. Детальный анализ результатов тотальной панкреатдуоденэктомии позволил заключить, что количество локальных рецидивов опухоли после операции такого объема сопоставимо со стандартной панкреатодуоденальной резекцией, а число ранних послеоперационных осложнений и риск возникновения сахарного диабета после тотальной панкреатдуоденэктомии оказываются принципиально выше.
Следующим шагом в преодолении барьера нерезектабельности опухолей поджелудочной железы явилось освоение резекции магистральных сосудов при вовлечении их в опухолевый процесс. В 1951 году George Eugene Moore первым выполнил резекцию верхней брыжеечной вены при аденнокарциноме головки поджелудочной железы, а годом позже William Vincent McDermott после панкреатодуоденальной резекции с резекцией верхней брыжеечной вены en bloc впервые сформировал портокавальный анастомоз. Тринадцать лет спустя Bernard Sigel сообщил о своем опыте замещения дефекта воротной вены после резекции головки поджелудочной железы венозным аутотрансплантатом.
И, наконец, своего рода вершиной онкологического радикализма при опухолях пакреатодуоденальной зоны стала операция регионарной панкреатэктомии, предложенная Joseph Gerald Fortner в 1973 году. В оригинальном описании регионарная панкреатэктомия проводится в двух вариантах. При первом выполняется тотальная панкреатэктомия с резекцией панкреатического сегмента воротной вены с сосудистым анастомозом, расширенной лимфаденэктомией в воротах печени, в области чревного ствола и верхней брыжеечной артерии. При втором варианте оперативное вмешательство дополняется резекцией верхней брыжеечной артерии, печеночной артерии или чревного ствола, иссечением фасции Герота, лимфаденэктомией в воротах правой почки, по ходу нижней полой вены и аорты. В отчете J. Fortner, охватывавшем опыт шестидесяти одной регионарной панкреатэктомии, приводились весьма впечатляющие данные о продолжительности вмешательства от восьми до двадцати девяти (!) часов, средней интраоперационной кровопотере в шесть литров и средней длительности послеоперационной госпитализации в сорок один день. При этом к моменту выписки в живых оставались лишь двадцать девять процентов из числа всех оперированных пациентов. Приведенные J. Fortner результаты заставили серьезно задуматься даже самых решительных хирургов-радикалов, а сам вопрос о целесообразности выполнения регионарной панкреатэктомии остается открытым и по сей день.
Помимо вопросов онкологического радикализма в период становления резекционной хирургии периампулярных опухолей достаточно остро стояли проблемы гастроэнтерологических последствий операции. Как указывалось выше, в стандартном варианте панкреатодуоденальная резекция, имея своей составной частью дистальную резекцию желудка, в полной мере несет на себе все риски развития постгастрорезекционных синдромов. Действительно, пептические язвы гастро-энтероанастомозов и, реже, демпинг-синдром были, как казалось, неизбежными спутниками операции. С целью улучшения функциональных результатов вмешательства 11 февраля 1937 года Alexander Brunschwig произвел первую анатомическую пилоросохраняющую панкреатодуоденальную резекцию. В 1944 году Kenneth Watson подробно описал принципиально иной для того времени вариант реконструкции пищеварительной трубки, который, кстати, касался и объема резекции. В оригинальном исполнении автора данное вмешательство выполнялось в два этапа. Двенадцатиперстная кишка пересекалась на дюйм дистальнее привратника с последующим формированием дуодено-энтероанастомоза «конец в конец». Несмотря на теоретическую обоснованность операции, она не получала должного признания вплоть до 1978 года, когда была «реинкарнирована» усилиями L. William Traverso и William P. Longmire.
Этими событиями, очевидно, заканчивается эпоха первых шагов покорения вершины панкреатодуоденальной резекции, эпоха ее рождения и доказательства права на жизнь в хирургической клинике. Впоследствии будут новые периоды разочарований и взлетов, времена малоинвазивного паллиатива и онкологического сверхрадикализма, эпоха лапароскопических технологий и робототехники. Впрочем, этим событиям, также уже ставшим историей, еще только предстоит быть подвергнутым безжалостному анализу потомков. Но все же: «Лучшее, что нам дает история, — это возбуждаемый ею энтузиазм». Энтузиазм для покорения новых вершин.
Кубышкин В.А., Козлов И.А., Алиханов Р.Б. Панкреатодуоденальная резекция с сохранением желудка при раке периампулярной зоны и головки поджелудочной железы. ХИРУРГИЯ, 6, 2001, с. 55-58.
Пархисенко Ю.А., Жданов А.И., Пархисенко В.Ю., Калашник Р.С. Хирургические операции на печени, желчных путях и поджелудочной железе. Часть III. Хирургия поджелудочной железы. АННАЛЫ ХИРУРГИЧЕСКОЙ ГЕПАТОЛОГИИ, 2015, том 20, №2.
Патютко Ю.И., Котельников А.Г. «Хирургия рака органов билиопанкреатодуоденальной зоны. Руководство для врачей». М., 2007.
Alexakis N., Halloran C., Raraty M., Ghaneh P. Current standards of surgery for pancreatic cancer. Br J Surg 2004; 91: 1410–27.
Brunschwig A. Resection of head of pancreas and duodenum for carcinoma-pancreatoduodenectomy. Surg Gynecol Obstet (1937) 65:681–685.
Cameron J.L. William Stewart Halsted. Our surgical heritage. Ann Surg (1997) 225:445–458.
Cameron J.L., Riall T.S., Coleman J.A., Belcher K.A. One thousand consecutive pancreaticoduodenectomies. Ann Surg, 2006; 244: 10–15.
Chandrakanth A., Mashaal D., Ravipati L. History of pancreaticoduodenectomy: early misconceptions, initial milestones and the pioneers. HPB, 2011, 13, 377–384.
consecutive pancreaticoduodenectomies. Ann Surg 244:10–15.
Desjardins A. Technique de la Pancréatectomie. Rev chir (1907) 35:945–
Dragstedt L.R., Dragstedt C., McClintock J.T., Chase C.S. Extirpation of the duodenum. Am J Physiolo (1918) 46:584–590.
Griffin J.F., Poruk K., Wolfgang Ch. Pancreatic cancer surgery: past, present, and future. Chin J Cancer Res 2015;27(4):332-348.
Halsted W.S. Contributions to the surgery of the bile passages, especially of the common bile-duct. Boston Med Surg J (1899) 141:645–654.
Hirschel G. Die Resektion des Duodenums mit der Papille wegen Karzinoms. Munchen Med Wochenschr (1914) 61:1728–1729.
Howard J.M. Historical Aspects and the Future of Pancreatoduodenectomy. F. Hanyu et al. (eds.), Pancreatoduodenectomy. Springer-Verlag Tokyo, 1997.
Howard J.M., Heiss W. History of the pancreas. Kluwer Academic/Plenum Publishers; 2002.
Hunt V.C. Surgical Management of Carcinoma of the Ampulla of Vater and of the Periampullary Portion of the Duodenum. Ann Surg (1941) 114:570–602.
Johna S., Schein M., editors. The memoirs of Allen Oldfather Whipple. tfm Publishing Ltd; 2003.
Kausch W. Das Carcinom der Papilla duodeni und seine radikale Entfernung. Beitrage zur Klinische Chirurgie (1912) 78:439–486.
Kehr H. Die gut- und bösartigen Neubildungen der Gallenblase und der Gallengänge unter besonderer Berücksichtigung eigener Erfahrungen (Das Karzinom der Papilla Vateri). Ergebn d Chir u Orth (1914) 8:471–624.
O’Sullivan A. Whipple pancreaticoduodenectomy: a historical comment. Grand Rounds Vol 7 DOI: 10.1102/1470-5206.2007.L0001. 2007.
Owens F.M. The problem of peptic ulcer following pancreatectomy. (1948) Ann Surg 128:15–20.
Peters J.H., Carey L.C. Historical review of pancreaticoduodenectomy.Am J Surg. 1991 Feb;161(2):219-25.
Sauve L. Des pancréatectomies et spécialement de la pancréatectomie céphalique. Rev chir (1908) 37:113–152 and 335–85.
Schnelldorfer T., Adams D.B., Warshaw A.L., Lillemoe K.D., Sarr M.G. Forgotten pioneers of pancreatic surgery: beyond the favorite few. Ann Surg (2008) 247:191–202.
Schnelldorfer T., Sarr M.G. Alessandro Codivilla and the First Pancreatoduodenectomy. Arch Surg. 2009;144(12):1179-1184. doi:10.1001/archsurg.2009.219
Tenani O. Contributo alla chirurgia della papilla del Vater. Policlinico (1922) 29:291–300.
Toneto M.G., Itaqui Lopes M.H. Historical evolution of the surgical treatment of pancreatic cancer English version of the article “Evolução histórica do tratamento cirúrgico do cancer de pâncreas” (Sci Med. 2014;24(2):193-201).
Traverso L.W., Longmire Jr. W.P. Preservation of the pylorus in pancreaticoduodenectomy a follow-up evaluation. Ann Surg 1980; 192: 306–10.
Trimble I.R., Parsons J.W., Sherman C.P. A one-stage operation for the cure of carcinoma of the ampulla of Vater and of the head of the pancreas. Surg Gynecol Obstet (1941) 73:711–722.
Whipple A.O. A reminiscence: pancreaticduodenectomy. Rev Surg (1963) 20:221–225.
Whipple A.O. Observations on radical surgery for lesions of the pancreas. Surg Gynecol Obstet (1946) 82:623–631.
Whipple A.O. Pancreaticoduodenectomy for Islet carcinoma – a five year follow-up. Ann Surg (1945) 121: 847–52.
Whipple A.O., Parsons W.B., Mullins C.R. Treatment of carcinoma of the ampulla of Vater. Ann Surg (1935) 102: 763–79.
Статья добавлена 13 октября 2017 г.