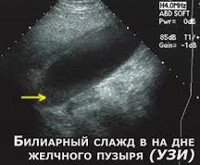
Билиарный сладж
Билиарный сладж — это патологическое состояние, при котором в желчевыводящей системе образуется взвесь из холестериновых или других кристаллов. Вначале протекает бессимптомно, в последующем проявляется болью в правом подреберье и диспепсией. Диагностируется при помощи УЗИ и динамической сцинтиграфии желчевыводящей системы, дуоденального зондирования, РХПГ и биохимического исследования крови. Терапия предполагает назначение урсодезоксихолевой кислоты, миотропных спазмолитиков, холеретиков, холекинетиков и растительных гепатопротекторов. При обструкции желчевыводящих путей выполняется холецистэктомия, бужирование желчных ходов.
МКБ-10
Общие сведения
Диагностика билиарного сладжа как самостоятельного патологического состояния стала возможной после широкого внедрения ультразвуковых методов исследования печени и желчевыводящих путей. Распространенность расстройства в популяции составляет 1,7-4%, у пациентов с заболеваниями пищеварительного тракта — 7-8%, у больных с гепатобилиарной патологией — 24,4-55%. В состав сладжа входят кристаллы холестерина, муцин, билирубинат кальция и другие пигменты. Наиболее часто болезнь выявляется у женщин старше 55 лет. Большинство гастроэнтерологов и гепатологов рассматривают наличие у пациента кристаллической билиарной взвеси как доклиническую (предкаменную) форму желчнокаменной болезни.
Причины
Билиарный сладж имеет полиэтиологическое происхождение, провоцируется теми же факторами, что и желчнокаменная болезнь. Ключевую роль в возникновении заболевания имеют изменение химического состава желчи и ее застой в желчевыводящих путях. В развитии патологии прослеживается наследственная предрасположенность, вероятность билиарного сладжеобразования у пациентов, родственники которых страдают холелитиазом, увеличивается в 2-4 раза. Специалисты в сфере гастроэнтерологии и гепатологии выделяют несколько групп предпосылок, при которых повышается риск появления сладжа в билиарной системе:
Расстройство может осложнять течение небилиарной патологии. До 8-16% случаев заболевания диагностируется у пациентов, страдающих серповидно-клеточной анемией. При повреждении спинного мозга выше 10 грудного позвонка образование сладжа обусловлено желчепузырной гипокинезией. Пусковым моментом билиарного сладжеобразования часто становятся хирургические вмешательства на органах ЖКТ: шунтирующие операции на желудке, гастрэктомия. В послеоперационном периоде сладж определяется у 42% больных.
Патогенез
Механизм формирования билиарного сладжа основан на возникшем дисбалансе между содержанием литогенных и противонуклеирующих факторов. При высокой концентрации холестерина начинается нуклеация, осаждение его кристаллов в желчи. В последующем преципитированные частицы агрегируются в микролиты, которые увеличиваются в размерах, превращаясь в желчные камни. Ускоренному осаждению холестерина способствуют нарушения желчеотделения функционального или органического генеза. В зависимости от причин сладжеобразования в состав билиарного содержимого могут входить пигменты, кальций и другие компоненты желчи.
Классификация
По происхождению кристаллической взвеси заболевание бывает первичным (эссенциальным) и вторичным, связанным с действием установленных этиологических факторов. При систематизации вариантов билиарного сладжа учитывают состав кристаллов (с преобладанием холестерин-муцинового комплекса, кальциевых солей или билирубинсодержащих пигментов), наличие холелитиаза и сократительную активность желчного пузыря. Для выбора терапевтической тактики важно знать УЗИ-форму болезни:
Симптомы билиарного сладжа
Зачастую болезнь длительное время протекает без явной симптоматики. Клиника неспецифична и обусловлена основной патологией, которая привела к скоплению холестериновых кристаллов в протоках билиарного тракта. Чаще всего пациентов беспокоят болевые ощущения справа в подреберье, связанные с приемом пищи и иррадиирующие в правую лопатку. Интенсивность болевого синдрома зависит от степени поражения желчевыделительной системы. Боль становится более сильной при миграции сладжа и может отдаленно напоминать типичную желчную колику. Также наблюдаются диспепсические симптомы: тошнота и рвота, горечь во рту, дискомфорт в животе после еды. Иногда отмечается изменение характера стула с преобладанием запоров. Общее состояние пациентов с симптоматикой билиарного сладжа не нарушено.
Осложнения
Длительное травмирование стенок желчевыводящих протоков кристаллами и микролитами приводит к воспалительной реакции — холангиту. При желчепузырном застое густой желчи возможно возникновение хронического холецистита. В случае присоединения вторичной инфекции развивается гнойный холангит, эмпиема желчного пузыря. Наиболее частым осложнением билиарного сладжа считается формирование конкрементов крупного размера. Длительное течение заболевания приводит к рубцовым изменениям желчных протоков, стенозирующему папиллиту, что требует хирургического вмешательства. При распространении патологического процесса за пределы билиарной системы возникает дуоденит, криптогенный панкреатит.
Диагностика
Постановка диагноза может быть затруднена, поскольку клиника билиарного сладжа часто сочетается с симптомами другой болезни. Обычно расстройство осложняет течение иной патологии желчных путей, что обуславливает полиморфность и неспецифичность проявлений. Диагностический поиск направлен на исключение других заболеваний с помощью комплексного обследования гепатобилиарной системы. Наибольшей информативностью обладают:
Лейкоцитоз и повышение СОЭ в общем анализе крови свидетельствует об осложнении заболевания. В копрограмме выявляются капли нейтрального жира, повышенное количество желчных кислот. Дополнительно может рассчитываться холестериновый индекс, свидетельствующий о повышении концентрации холестерина в пузырной желчи. Для исключения возможной онкологической патологии выполняется КТ или МРТ брюшной полости.
Чаще всего преципитацию холестерина в системе желчевыведения приходится дифференцировать с функциональными дискинезиями. При этом ключевым критерием болезни становятся УЗИ-признаки наличия в желчи кристаллической взвеси. В отличие от онкологических заболеваний при желчном сладже отсутствуют объёмные новообразования в гепатобилиарной зоне. Организацией обследования пациента занимается гастроэнтеролог или гепатолог.
Лечение билиарного сладжа
Пациентам с впервые выявленными признаками заболевания без клинической симптоматики рекомендовано динамическое наблюдение и устранение факторов, спровоцировавших сладжеобразование, — лечение основной патологии, отмена литогенных средств и коррекция диеты. При постоянном наличии УЗИ-признаков патологической взвеси в течение 3 месяцев назначается консервативная антилитогенная терапия. Схема лечения обычно включает следующие группы лекарственных средств:
Для более быстрой элиминации сладжа применяют энтеросорбенты, блокаторы липаз и регуляторы кишечной моторики, затрудняющие всасывание холестерина в кишечнике. Хирургические методы при выявлении билиарной взвеси используются редко, в основном при наличии терапевтически резистентного спазма или стеноза сфинктера Одди. В подобных случаях для ликвидации холестаза выполняется сфинктеропапиллотомия. При обтурации замазкообразной желчью узких мест желчевыводящих путей может проводиться открытая или лапароскопическая холецистэктомия, эндоскопическое бужирование желчных протоков.
Прогноз и профилактика
Исход билиарного сладжа определяется степенью функциональных и органических изменений в желчевыводящих протоках и желчном пузыре, общим состоянием пациента, наличием сопутствующей патологии. Прогноз благоприятный при известном этиологическом факторе, устранение которого приводит к полному регрессу симптоматики. В остальных случаях существует высокий риск трансформации заболевания в органическую билиарную патологию. Для профилактики сладжа необходимо снизить количество жирных и жареных блюд в рационе, соблюдать интервалы между приемами пищи (не более 3-4 часов), ограничить прием медикаментов, которые могут вызывать спазм сфинктера Одди. Важно проводить своевременную диагностику и лечение заболеваний, приводящих к билиарному застою.
О частоте выявления «желчного сладжа» с помощью УЗИ
УЗИ сканер WS80
Идеальный инструмент для пренатальных исследований. Уникальное качество изображения и весь спектр диагностических программ для экспертной оценки здоровья женщины.
Введение
С развитием различных методов визуализации, в частности, ультрасонографии, появились специфические нозологические формы, среди которых встречается и «желчный сладж» (ранее не диагностировавшийся с помощью рентгенологического исследования). «Желчный сладж» представялет собой смесь слизи, билирубината кальция и кристаллов холестерина. Он появляется, когда желчь становится густой и вязкой, замещая нормальную желчь [1, 2].
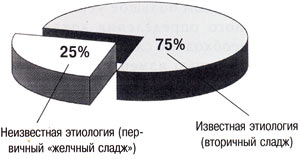
Рассматривая этиологию «желчного сладжа», его можно классифировать на вторичный и первичный. Вторичный сладж появляется, когда имеется хорошо известное этиопатогенетическое условие: после ударно-волновой литотрипсии по поводу желчных конкрементов, при желчно-каменной болезни, беременности [3, 4], циррозе печени, механической желтухе, водянке желчного пузыря, длительном парентеральном питании [5,6], сахарном диабете, серповидно-клеточной анемии [7], после приема цефтриаксона [8, 9]. Как первичный сладж расценивается в тех случаях, когда не может быть выявлено ни одно из указанных выше состояний.
Материалы и методы
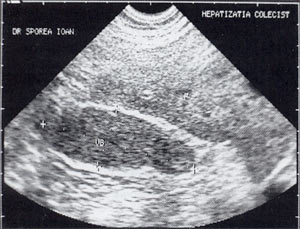
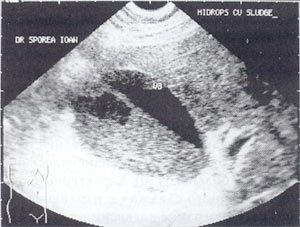
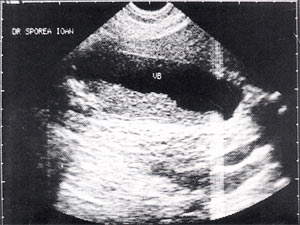
Рис. 1. Гепатизация желчного пузыря, полностью заполненного сладжем.
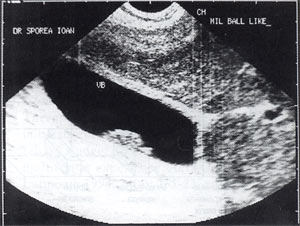
Кроме типичного вида, «желчный сладж» может иметь особый вид, похожий на круглое полипоидное объемное образование с острыми краями или неравномерным контуром («опухолеподобный желчный сладж» или «сладжевые шарики» [12, 13]). При изменении положения больного видны перекатывающиеся или разрушающиеся шарики сладжа, затем снова формирующие исходное объемное образование (рис. 2-8).
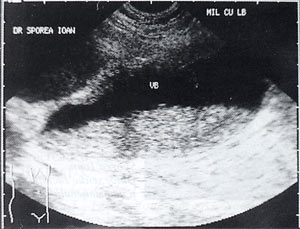
Рис. 2. Желчный пузырь, наполовину заполненный сладжем.
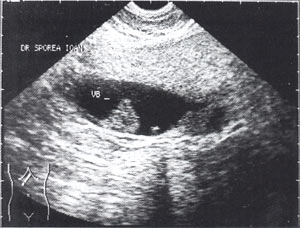
Рис. 3. Большой желчный пузырь со сладжем.
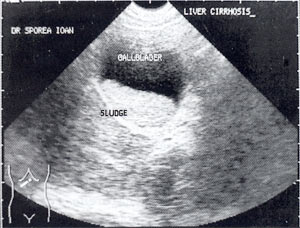
Рис. 4. «Желчный сладж» у больного с циррозом печени.
Рис. 5. Желчный пузырь, заполненный сладжем, у больного циррозом.
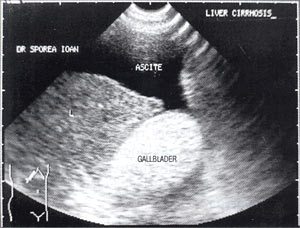
Рис. 6. Желчный пузырь и «желчный сладж».
Рис. 7. «Желчный сладж» в виде шара.
Рис. 8. Шароподобный «желчный сладж».
Используя определение «желчный сладж», с помощью ультразвукового сканера с конвексным и секторным датчиками 3,5 и 5 МГц мы проспективным образом обследовали 11 800 больных с целью выявления сладжа. Ультразвуковое исследование проводилось по меньшей мере после 10-часового периода голодания.
На основании клинических или параклинических данных, мы разделили сладжи на первичный и вторичный.
Результаты
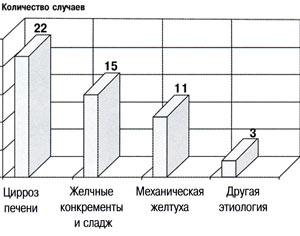
Рис. 9. Этиология «желчного сладжа».
Чаще обнаруживали вторичный сладж при циррозе печени (22 случая), затем при сопутствующих желчных конкрементах (15 человек) и механической желтухе (11 больных) (рис. 10).
Рис. 10. Случаи вторичного сладжа.
Обсуждение
Наличие «желчного сладжа» у 0,6% больных, прошедших ультразвуковое исследование, означает, что эта нозологическая форма является относительно редкой. Если по вторичному сладжу вопрос достаточно ясен, то клиническое значение первичного «желчного сладжа» понятно еще не полностью. В исследовании, включавшем 96 больных с желчным сладжем, ультразвуковое наблюдение проводилось в среднем в течение 38 мес, и W. Middleton [14] показал, что у 14 (14,5%) пациентов развились желчные конкременты, 6 (6,2%) больных со сладжем предъявляли жалобы на печеночные колики (при отсутствии холелитиаза).
Что касается «опухолевидного желчного сладжа», то его ультразвуковая диагностика может быть трудной, потому что требуется дифференциальная диагностика с раком и конкрементами желчного пузыря (в частности, билирубиновые конкременты иногда имеют тонкую акустическую тень).
Другим аспектом, который необходимо обсудить, является ложный вид сладжа при условии несоответствия мощности звука (слишком большое усиление). Для правильного определения локализации сладжа необходимо следить за его движением с помощью изменения положения тела больного. Но для достаточно опытного специалиста в области ультразвуковых исследований правильная диагностика сладжа почти никогда не представляет трудностей.
Выводы
С появлением новых методов визуализации обнаружение «желчного сладжа » стало реальностью, что имеет клиническое значение. Его частота не так высока (0,6% всех случаев, обследованных с помощью ультразвука), но отдельные пациенты с первичным «желчным сладжем» требуют динамического наблюдения для последующего решения вопроса о возможном лечении.
Литература
УЗИ сканер WS80
Идеальный инструмент для пренатальных исследований. Уникальное качество изображения и весь спектр диагностических программ для экспертной оценки здоровья женщины.
Желчный пузырь: песок, густая желчь, взвесь, рыхлый осадок в желчном пузыре (билиарный сладж)
Наша клиника занимается лечением заболеваний органов пищеварения, мы предложим Вам лечение у врача гастроэнтеролога или терапевта с дополнительной подготовкой по гастроэнтерологии. У нас опытные врачи, широкий выбор ультразвуковых и лабораторных исследований. Большая часть исследований входит в программы годового обслуживания – это удобно. Наша задача – найти и по возможности устранить актуальные причины образования сладжа, избежать образования камней и других хирургических осложнений, нормализовать пищеварение.
Билиарный сладж. Причины и симптомы
Билиарный сладж, его еще называют плотная желчь, желчный осадок, желчный песок, микролитиаз, определяют как вязкую взвесь в пузырной желчи с наличием кристаллов или даже мелких камней. Если ситуацию пустить на самотек, возможно постепенное склеивание кристаллов с образованием крупных камней. Поэтому билиарный сладж является первой (предкаменной) стадией желчнокаменной болезни и лечение, проводимое на этой стадии, позволяет предотвратить образование желчных камней.
Желчная колика. Билиарный сладж может сформировать своего рода мягкую пробку, способную закупорить желчевыводящие пути. А желчная колика – это мощное болезненное сокращение стенок желчных протоков, стремящихся вытолкнуть эту пробку, т.е. закупоривший их сладж. Спровоцировать желчную колику может жирная, жареная, острая пища, тряская езда, эмоциональный стресс, прием желчегонных препаратов (например, аллохол).
Симптомы желчной колики:
Диагностика и лечение билиарного сладжа в клинике «Эхинацея»
 |  |
УЗИ желчного пузыря. Левое изображение – осадок на дне желчного пузыря, там же замазкообразная желчь. Справа – взвесь в желчном пузыре.
Что такое билиарный сладж и как его вылечить?
Очень часто врачу-терапевту медицинского центра приходится сталкиваться с заключением специалиста УЗИ, проведшим исследование печени и желчного пузыря, где используется выражение: «Сладж –синдром». Что же это такое?
Причины заболевания и её разновидности
Специалисты называют следующие основные предпосылки возникновения сладж-синдрома. В первую очередь – это:
Выделяют 3 типа БС:
Если говорить о видах патологии, то здесь речь идёт о:
Факторами риска возникновения болезни опытные терапевты считают:
Каковы же причины патологии?
13.Ограничение употребления жидкости.
Симптомы болезни
Большой практический опыт работы в должности терапевта поликлиники позволяет утверждать, что клинические проявления билиарного сладжа в некоторых случаях у пациентов могут вообще отсутствовать, но могут вызывать и осложнения вплоть до оперативных вмешательств.
Чаще всего наблюдаются следующие признаки:
Лечение билиарного сладжа
Схема лечения выбирается лечащим врачом индивидуально для каждого больного в зависимости от личных качеств и стадии заболевания. Она, как правило, включает такие медикаментозные и немедикаментозные методы терапии, как:
Профилактика БС
Рекомендуемые специалистами меры по предупреждению развития билиарного синдрома включают:
Абдулмуслимова Лаюза Мухтарахмедовна, врач-терапевт, кардиолог.
Работает в медицинской клиники «Целитель» в Хасавюрте по адресу: ул. Абубакарова, д.9а.
График работы: ежедневно, с понедельника по субботу – с 9.00 до 17.00.
Современный взгляд на проблему билиарного сладжа
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Введение Можно считать окончательно признанным взгляд на желчно–каменную болезнь (ЖКБ), как на длительный и многостадийный процесс, при котором периоду камнеобразования предшествуют изменения метаболизма и физико–химических свойств желчи. Эти успехи послужили серьезным толчком для внедрения научных достижений в клиническую практику. Начали предприниматься многочисленные попытки, направленные на диагностику заболевания на предкаменной стадии, так как это открывало широкие перспективы по первичной профилактике холелитиаза. По степени нарушения солюбилизирующих свойств желчи предлагались различные классификации предкаменной стадии ЖКБ [D. Small, 1974; Х.Х. Мансуров, 1982 и др.].
Можно считать окончательно признанным взгляд на желчно–каменную болезнь (ЖКБ), как на длительный и многостадийный процесс, при котором периоду камнеобразования предшествуют изменения метаболизма и физико–химических свойств желчи. Эти успехи послужили серьезным толчком для внедрения научных достижений в клиническую практику. Начали предприниматься многочисленные попытки, направленные на диагностику заболевания на предкаменной стадии, так как это открывало широкие перспективы по первичной профилактике холелитиаза. По степени нарушения солюбилизирующих свойств желчи предлагались различные классификации предкаменной стадии ЖКБ [D. Small, 1974; Х.Х. Мансуров, 1982 и др.].
Однако эти классификации не нашли практического применения, так как для диагностики начальных стадий заболевания требовалось проведение дуоденального зондирования и биохимическое исследование полученной желчи, что значительно ограничивало использование метода в качестве скринингового. Поэтому и в настоящее время в подавляющем большинстве случаев ЖКБ выявляется на стадии сформировавшихся желчных камней. Внедрение малоинвазивных хирургических технологий привело к тому, что холецистэктомия стала основным методом лечения ЖКБ и даже создало иллюзию появления «золотого стандарта» лечения холецистолитиаза. Однако вряд ли логично считать «золотым стандартом» метод, направленный на удаление органа. В билиарном литогенезе единственным и обязательным фактором камнеобразования является секреция литогенной желчи. Остальные факторы носят вспомогательный характер. Поэтому «обвинять» желчный пузырь за то, что в нем «заводятся» камни и в качестве наказания его удалять, никоим образом не решает проблемы ЖКБ. Сохраняющиеся хроническая билиарная недостаточность и билиарные дисфункции в сочетании с другими заболеваниями органов пищеварения, ассоциированными с ЖКБ вследствие длительного камненосительства, обеспечивают после операции развитие так называемого постхолецистэктомического синдрома (ПХЭС). По разным оценкам, частота ПХЭС достигает 40%, а согласно нашим последним исследованиям – 51,3% [1].
Холецистолитиаз – наиболее частая причина холецистэктомий, а потому и наиболее дорогая операция. Так, по данным Е. Shaffer, в США ежегодно выполняется более 700 тыс. холецистэктомий и общая сумма затрат на лечение больных ЖКБ составляет около 6,5 млрд. долларов [2]. В связи с этим наиболее перспективным направлением является диагностика и лечение заболевания на предкаменной стадии.
Для решения этой проблемы необходимо ответить на два главных вопроса. Во–первых, какую стадию изменений физико–химических свойств желчи и даже ее микроструктуры следует взять за основу в качестве предкаменной стадии и рекомендовать ее диагностику в клиническую практику. Во–вторых, какой метод диагностики рекомендовать, с помощью которого можно было бы даже в условиях поликлиники диагностировать предкаменную стадию заболевания. За более чем 30–летнюю историю изучения предкаменных состояний предлагалось выделять несколько стадий – от генетических, биохимических и метаболических дефектов, приводящих к перенасыщению желчи холестерином до стадии формирования и роста кристаллов холестерина. В соответствии с этим рекомендовались и всевозможные методы диагностики – от ядерной магнитно–резонансной спектроскопии, лазерного квазиупругого рассеивания, гельраспределительной хроматографии до сканирующей электронной и поляризационной микроскопии. Естественно, эти методы могли использоваться лишь для научных целей, но не для применения в клинической практике.
Ответ на первый вопрос можно найти, проанализировав основные этапы холестеринового литогенеза, который включает:
•• перенасыщение желчи холестерином;
•• нуклеация и преципитация кристаллов холестерина;
•• агрегация кристаллов и формирование микролитов.
С теоретической и практической точки зрения наиболее приемлемой является диагностика предкаменной стадии ЖКБ на III этапе – агрегации кристаллов моногидрата холестерина с последующим формированием микролитов. С теоретической точки зрения эта предкаменная стадия является наиболее продвинутой, и, по результатам наших исследований, биохимические свойства на этой стадии мало отличаются от стадии сформировавшегося холецистолитиаза. С практической точки зрения на этой стадии, как правило, заканчивается формирование основных и вспомогательных факторов билиарного литогенеза, и процесс принимает однонаправленный характер, реже подвергается обратному развитию.
Диагностика ЖКБ на стадии сформировавшихся микролитов облегчает ответ и на второй вопрос. Изменение микроструктуры желчи в виде сформировавшихся микролитов делают их макроскопически видимыми, что легко выявляется с помощью трансабдоминальной ультрасонографии и трактуется в виде различных вариантов билиарного сладжа.
Таким образом, в настоящее время появилась реальная возможность выявлять ЖКБ на ее предкаменной стадии в любом клиническом учреждении, оснащенным аппаратом ультразвуковой диагностики. Эти достижения послужили толчком для разработки новой клинической классификации ЖКБ с включением в нее предкаменной стадии заболевания. Такая классификация была разработана в Центральном НИИ гастроэнтерологии, обсуждена на III съезде Научного общества гастроэнтерологов России (НОГР) и рекомендована для применения в клинической практике [3].
Клиническое значение
билиарного сладжа
Клиническое значение билиарного сладжа практикующими врачами, как правило, оценивается недостаточно. Накопленные в настоящее время обширные эпидемиологические исследования свидетельствуют о широком распространении билиарного сладжа. Анализ многочисленных литературных источников показывает, что частота выявления билиарного сладжа в различных популяциях колеблется в широких пределах и составляет:
• в общей популяции среди лиц, не страдающих ЖКБ – 1,7–4%;
• среди лиц, предъявляющих жалобы со стороны органов пищеварения – 7–8%;
• среди лиц, предъявляющих жалобы, характерные для диспепсии билиарного типа – 24,4–55%.
Наиболее часто билиарный сладж выявляется у лиц с билиарной патологией. По нашим данным, среди 1500 больных с различной патологией билиарного тракта, обследованных с помощью УЗИ, билиарный сладж выявлен у 613 (41%) (рис. 1).
Высокая распространенность билиарного сладжа позволила накопить обширный клинический материал, свидетельствующий об особенностях его клинического течения, прогнозе, осложнениях, что обосновывает необходимость проведения качественной диагностики и эффективной терапии.
Основное клиническое значение билиарного сладжа заключается в том, что он является источником камнеобразования. Однако это отнюдь не означает, что у всех больных с билиарным сладжем обязательно образуются камни. Несмотря на то, что билиарный сладж является исходным материалом для формирования желчных камней, они, по разным оценкам, образуются только у 5–20% пациентов за 1–3–летний период. Это связано с тем, что при исчезновении причин, способствующих образованию сладжа, последний исчезает спонтанно.
Билиарный сладж, содержащий микролиты, может свободно проходить по всей протоковой системе, постоянно раздражая богатую болевыми рецепторами слизистую оболочку желчных путей (особенно сфинктерного аппарата), и обусловливать возникновение болевого синдрома. По последним данным, причиной «необъяснимых» болей в правом подреберье у 83% больных может быть билиарный сладж [4]. Причиной болей при билиарном сладже являются и дисфункции сфинктерного аппарата желчных путей, которые в данной ситуации носят вторичный характер. Так, например, дисфункция сфинктера Одди при билиарном сладже выявляется в 50–93% случаев.
Кроме того, длительная персистенция билиарного сладжа и постоянный пассаж его в двенадцатиперстную кишку может осложняться развитием стриктур терминального отдела общего желчного протока и/или стенозирующего папиллита.
Билиарный сладж (БС) – частая причина билиарного панкреатита. Исследованиями установлено, что частота выявления билиарного сладжа у больных с идиопатическим панкреатитом достаточно высока и, по данным разных авторов, достигает 33–90% [4–6]. Основные причины развития панкреатита при билиарном сладже обусловлены дисфункцией сфинктера Одди, создающей условия для билиарных рефлюксов в протоковую систему поджелудочной железы, стеноз сфинктера Одди и/или панкреатического протока.
Более редкие осложнения билиарного сладжа – развитие острого холецистита, холангита. В отдельных случаях при наличии замазкообразной желчи возможно отключение желчного пузыря вследствие закупорки пузырного протока.
По последним данным японских исследователей, билиарный сладж является маркером раннего рака желчного пузыря. В связи с этим рекомендуется эндоскопическая катетеризация желчного пузыря с цитологическим исследованием билиарного осадка на наличие атипичных клеток.
Клиника
В последние годы благодаря широкому применению УЗИ и обширным скрининговым исследованиям, изменилось представление о клинической картине ЖКБ и накоплены определенные сведения о клиническом течении БС. По нашим данным, при БС боли встречаются более чем у половины пациентов, нередко отмечаются симптомы билиарной диспепсии и только в 21% случаев не удается выявить каких–либо жалоб [7,8]. Более яркая клиническая симптоматика при БС по сравнению с холецистолитиазом вполне объяснима. Во–первых, в отличие от желчных конкрементов, БС может свободно проходить по всей протоковой системе, раздражая болевые рецепторы слизистой оболочки желчных путей, особенно дистальных сфинктеров. Во–вторых, сократительная функция желчного пузыря (СФЖП) при БС, как показали исследования, страдает меньше, чем при холецистолитиазе, что способствует постоянной элиминации БС и возникновению болей. Так, коэффициент опорожнения желчного пузыря после желчегонного завтрака при различных формах БС составляет в среднем 31–36% [7].
Причиной абдоминальной боли при билиарной патологии могут быть как функциональные, так и органические заболевания желчного пузыря и желчных путей. Возникновение абдоминальной боли при билиарной патологии обусловлено спазмом гладкой мускулатуры, особенно сфинктерного аппарата билиарного тракта, перерастяжением стенки желчного пузыря и желчных протоков в результате развития билиарной гипертензии, механического раздражения стенки желчного пузыря и протоковой системы билиарным сладжем или конкрементом. Все эти причины отдельно или в сочетании встречаются и при БС. В зависимости от причины, вызвавшей боли, различается и ее характер. Боли могут возникать спонтанно или усиливаться постепенно, продолжаться в течение нескольких минут или часов, сохраняться длительно или рецидивировать с различной периодичностью, быть локализованными или распространенными.
Кроме того, тесная анатомо–функциональная взаимосвязь билиарной системы с органами гастропанкреатодуоденальной зоны и их вовлечение в патологический процесс при БС обусловливает смешанный характер боли и сочетание ее с другой симптоматикой желудочно–кишечного тракта (тошнотой, рвотой, изжогой, чувством переполнения в желудке, поносами, запорами и т.д.).
Следует учитывать, что длительная персистенция БС способствует формированию различных осложнений и обусловливает дополнительный полиморфизм клинической картины.
Таким образом, специфической картины при билиарном сладже не существует. При самостоятельном его течении наиболее частыми симптомами является боль, однако у части больных она может отсутствовать. Сочетание БС с билиарными дисфункциями существенно может менять клиническую симптоматику, а осложнения, развивающиеся при длительной персистенции БС, в большинстве случаев проявляются клиникой этих осложнений.
Диагностика
Основным методом диагностики БС является трансабдоминальная ультрасонография (ТУС), которая позволяет судить об эхооднородности желчи (рис. 2). Исследование проводят в положении больного на спине, левом боку и после перемены положения, что дает возможность более четко судить о наличии макроскопически видимых изменениях в пузырной желчи.
Согласно клинической классификации, разработанной Центральным НИИ гастроэнтерологии и рекомендованной III съездом НОГР, предкаменная стадия ЖКБ подразделяется на стадию, при которой ультразвуковое исследование выявляет только неоднородную желчь и стадию сформировавшегося билиарного сладжа. С практической точки зрения наиболее целесообразной является диагностика заболевания на стадии билиарного сладжа.
Мы выделяем 3 основных варианта билиарного сладжа:
1. Эхонеоднородная желчь со сгустками: эхонеоднородная желчь, с наличием единичных или множественных участков повышенной эхогенности, имеющих четкие или размытые контуры, смещаемых, без акустической тени и, как правило, расположенных по задней стенке желчного пузыря (рис. 3).
2. Взвесь гиперэхогенных частиц (ВГЧ): точечные, единичные или множественные, смещаемые гиперэхогенные образования, не дающие акустической тени, выявляемые при изменении положения тела пациента (рис. 4).
3. Замазкообразная желчь: эхонеоднородная желчь с наличием участков, приближающихся по эхогенности к паренхиме печени, смещаемых (рис. 5) или фиксированных к стенке желчного пузыря (рис. 6), с четким контуром, не дающих акустическую тень, или в редких случаях с эффектом ослабления за сгустком.
В клинической практике чаще всего встречается вариант билиарного сладжа в виде ВГЧ (около 70%), тогда как частота обнаружения двух других вариантов составляет около 10–12%.
Основным методом диагностики БС является ТУС. Чувствительность трансабдоминальной сонографии в диагностике БС составляет 55–65%, а специфичность – более 90%.
ТУС позволяет изучить состояние стенки желчного пузыря и его сократительную функцию, так как БС часто сопровождается снижением сократительной функции желчного пузыря. При БС в виде ВГЧ стенка желчного пузыря обычно не изменена, при других вариантах могут быть выявлены ультразву-ковые признаки воспаления. Нередко БС сочетается с сетчатой формой холестероза желчного пузыря.
ТУС дает возможность осуществлять динамическое наблюдение за больными с БС, так как у части пациентов БС может спонтанно исчезать. Кроме того, УЗИ является объективным методом контроля за эффективностью терапии.
Для диагностики БС применяют прямое микроскопическое исследование пузырной желчи, хотя этот метод на практике используется реже, чем сонография.
При биохимическом исследовании сыворотки крови примерно у половины больных выявляют повышенные уровни общего холестерина. При биохимическом исследовании пузырной желчи, полученной при дуоденальном зондировании, коэффициент холаты/холестерин при наличии БС снижен, а индекс насыщения желчи холестерином, напротив, повышен. Время нуклеации желчи у пациентов с БС меньше, чем у здоровых лиц, но больше, чем при холецистолитиазе.
В патогенезе формирования БС наряду с другими факторами, важную роль играют дисфункции сфинктерного аппарата билиарного тракта. Поэтому при обследовании больного с БС необходимо иметь представление о функциональном состоянии сфинктерного аппарата желчных путей и, в частности, сфинктера Одди.
При метеоризме, выраженной подкожно–жировой клетчатке передней брюшной стенки исследование с помощью трансабдоминальной ультрасонографии может быть затруднено. В этих ситуациях ТУС необходимо дополнить эндоскопической ультрасонографией (ЭУС), информативность которой в диагностике БС существенно выше (чувствительность 92–96%, специфичность – 86–100%). ЭУС показана и в тех случаях, когда имеются трудности в проведении дифференциального диагноза, например, между фиксированным к стенке желчного пузыря сгустком замазкообразной желчи и пристеночными образованиями, в первую очередь опухолевого генеза (рис. 7).
С помощью УЗИ изучают состояние стенки желчного пузыря (наличие холестероза или воспаления), что в ряде случаев может объяснить причину формирования БС. Важно исследование СФЖП. С этой целью изучают базальный объем желчного пузыря и после желчегонного завтрака. В качестве стандартизованного желчегонного завтрака целесообразно использовать 200 мл 1–% сливок. При сохраненной СФЖП коэффициент опорожнения составляет не менее 50%.
Для диагностики БС используются и другие методы. По данным компьютерной томографии у пациентов с БС прозрачность пузырной желчи ниже, чем при нормальной желчи. Для диагностики БС применяют прямое микроскопическое исследование пузырной желчи, хотя этот метод реже применяется на практике, чем сонография.
Несмотря на то, что УЗИ позволяет достаточно точно судить о функциональном состоянии желчного пузыря, диагностика дисфункций сфинктера Одди с помощью УЗИ затруднена. Одним из наиболее информативных методов оценки функционального состояния желчевыводящих путей и биохимического состава желчи является этапное хроматическое дуоденальное зондирование (ЭХДЗ). Применение ЭХДЗ с изучением стимулированного дебита желчи и количества основных ее компонентов дает возможность в рамках одного исследования диагностировать нарушения процессов желчеобразования, желчеотделения, моторики билиарного тракта и выявлять степень билиарной недостаточности при БС. Исследования показывают, что часто причиной гипокинезии желчного пузыря и, как следствие, причиной формирования БС является гипертонус сфинктера Одди.
Таким образом, в настоящее время имеются все возможности для диагностики БС и дано клиническое обоснование необходимости его элиминации. Эти факты послужили серьезным стимулом для разработки методов терапии при БС.
Лечение
Тактика ведения при билиарном сладже и терапевтические подходы не разработаны. Высказывается мнение, что пациенты с БС, не имеющие каких–либо клинических проявлений, не требуют медикаментозного лечения и врачебного наблюдения. По нашему мнению, подобный взгляд не может быть поддержан. В этом убеждают и данные, свидетельствующие о том, что у пациентов даже с длительным (до 6 лет) бессимптомным течением БС в последующем в 13% случаев возникают различные клинические проявления [9].
Учитывая тот факт, что течение билиарного сладжа отличается разноообразием (БС может спонтанно исчезать, длительно персистировать или прогрессировать), на наш взгляд, показанием к проведению курсов консервативной терапии при БС, даже не сопровождающегося клинической симптоматикой, является стойкое его выявление по данным УЗИ на протяжении 3 месяцев.
В зависимости от особенностей клинического течения билиарного сладжа определяется и тактика ведения больных [10]:
I — не требующие лечения, так как устранение этиологического фактора приводит к регрессу БС.
II — нуждающиеся в терапевтическом лечении, ибо без соответствующего лечения БС трансформируется в желчные камни с вовлечением в патологический процесс других органов и систем.
III — нуждающиеся в хирургическом лечении, без которого возможны осложнения, требующие неотложного хирургического вмешательства, с высоким риском гнойных осложнений и летальности.
Однако выбор тактики ведения и лечения при БС должен исходить не только из особенностей клинического течения, но и диагностированных с помощью УЗИ вариантов билиарного сладжа. При БС в виде взвеси гиперэхогенных частиц (микролитах) вряд ли может понадобиться хирургическое вмешательство. Исключение могут составлять лишь случаи, когда вследствие длительной персистенции БС формируются стриктура терминального отдела общего желчного протока или стенозирующий папиллит, затрудняющие отток желчи. В то время как при наличии замазкообразной желчи ситуации, требующие хирургического лечения, встречаются чаще. Сгустки замазкообразной желчи могут вызывать закупорку желчных протоков в наиболее узких местах. Таковыми являются пузырный проток и дистальные отделы общего желчного протока. Мы наблюдали «отключение» желчного пузыря, развившееся в течение одной недели пребывания больного в стационаре и потребовавшее удаления желчного пузыря. Причина – спонтанное формирование сгустка замазкообразной желчи, закупорившего пузырный проток.
Для снижения литогенных свойств желчи традиционно применяются препараты желчных кислот и, в частности, урсодеоксихолевой кислоты (УДХК). Одним из свойств УДХК является способность уменьшать насыщенность желчи холестерином за счет угнетения абсорбции в кишечнике, подавления синтеза в печени, что сопровождается снижением секреции его в желчь. В связи с этим клинический эффект урсотерапии при БС в первую очередь обусловлен снижением литогенности желчи и, как следствие, увеличением времени нуклеации, что в конечном итоге предупреждает образование микролитов, способствует растворению холестериновых камней. Препараты УДХК назначают в дозе 10–15 мг/кг однократно всю суточную дозу на ночь. Курс лечения зависит от формы билиарного сладжа. Для элиминации билиарного сладжа в виде взвеси гиперэхогенных частиц обычно достаточно месячного курса лечения. При других формах БС курс лечения более длительный, но, как правило, не превышающий трех месяцев. Эффективность урсотерапии в сроки лечения до 3 месяцев в зависимости от вида БС составляет 75–85%. Это обусловлено тем, что УДХК, снижая литогенные свойства желчи, слабо влияет на синхронную работу сфинктерного аппарата желчных путей. Однако, как известно, одной из причин формирования БС является сниженная СФЖП, которая в большинстве случаев выявляется при БС.
Собственные исследования, проведенные с помощью ЭХДЗ, показали, что сниженная сократительная функция желчного пузыря в 73,7% случаев сочеталась с гипертонусом сфинктера Одди, а в 68,4% имелся диссинергизм сфинктеров Люткенса и Одди, в 78,9% – диссинергизм сфинктеров Мирицци и Одди [11,12]. Эти данные позволяют предположить, что снижение СФЖП при БС носит вторичный характер и обусловлено гипертонусом сфинктера Одди.
Проведенные ранее собственные исследования других авторов показали, что мебеверин (Дюспаталин®) оказывает селективный спазмолитический эффект на сфинктер Одди [13, 14]. Эти данные послужили обоснованием для включения мебеверина в схему лечения при БС, течение которого сопровождается сниженной СФЖП и гипертонусом сфинктера Одди.
Исследование проведено с участием 40 больных, у которых при УЗИ был выявлен БС в виде взвеси гиперэхогенных частиц (микролитов 1–2 мм). Пациенты первой группы (n=20) получали УДХК в суточной дозе 10 мг/кг массы тела в сочетании с мебеверином (Дюспаталином®) по 200 мг 2 раза в сутки на протяжении двух месяцев. Пациенты второй группы – только УДХК в той же дозе и в те же сроки, что и первая группа. Как показали исследования, подобное сочетание быстрее по сравнению с монотерапией УДХК купировало боли и диспепсические расстройства, а элиминация БС в эти сроки наступила у 19 из 20, в то время как в первой группе у 16 из 20 больных.
Таким образом, в результате проведенных исследований установлено, что наиболее оптимальной схемой в лечении билиарного сладжа в виде взвеси гиперэхогенных частиц является сочетание УДХК и мебеверина. Примененная схема лечения позволяет устранить явления дисхолии и нарушения моторики билиарного тракта, уменьшает сроки лечения и повышает частоту элиминации БС у 95% больных.
Существует мнение, что у больных с наличием литогенной желчи для профилактики холестеринового камнеобразования целесообразно выполнять эндоскопическую папиллосфинктеротомию (ЭПСТ), так как через 5–6 лет у таких больных в 36% случаев образуются конкременты в желчном пузыре [15]. С этим мнением трудно согласиться по двум причинам. Во–первых, коррекция дисхолии с помощью современных лекарственных препаратов на начальной стадии ЖКБ не представляет особых трудностей. Во–вторых, опасность развития осложнений во время проведения ЭПСТ и ее последствия могут быть более серьезными, чем риск развития холелитиаза у части пациентов.
В ряде случаев после успешной терапии БС может возникнуть вновь. В этой ситуации повторные курсы терапии позволяют быстро купировать рецидив.