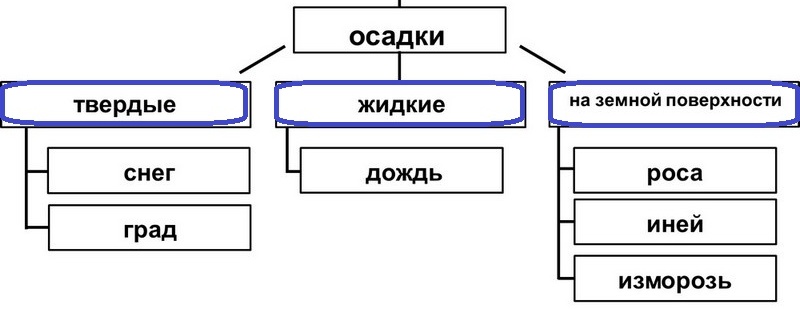
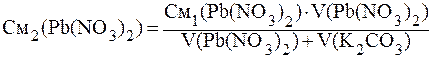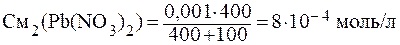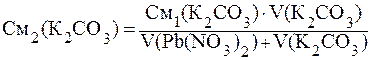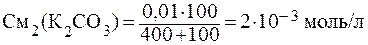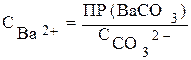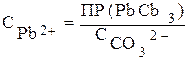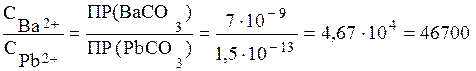УСЛОВИЕ ВЫПАДЕНИЯ ОСАДКА.



Произведение растворимости является одной из основных характеристик осадка. Пользуясь этой характеристикой, можно изменять растворимость осадка, рассчитывать оптимальные условия осаждения, предвидеть, какими реакциями осаждения лучше пользоваться для определения тех или иных ионов.
Из уравнения (3.1.) вытекают условия образования в растворе осадка:
Осадок малорастворимого электролита образуется только в том случае, когда произведение концентраций его ионов (П) в растворе превышает величину произведения растворимости этого соединения, т.е. когда раствор становится пересыщенным относительно данного малорастворимого соединения. Из ненасыщенного раствора осадок не выделяется, происходит растворение твёрдой фазы.
ПРИМЕР 3.6 Определить, образуется ли осадок PbCО3 при смешении 400 мл 0,001 М Pb(NO)2 и 100 мл 0,01 М К2СО3.
Решение: Найдём молярные концентрации веществ в момент смешения по формуле:
Концентрации ионов, образующих осадок, равны:
[Pb 2+ ]= См2(Pb(NO)2), т.к. при диссоциации из 1 моль соли образуется 1 моль ионов свинца.
Итак, карбонаты бария и свинца будут выпадать одновременно из раствора, если СВа 2+ >СРb 2+ в 46700 раз. Если отношение СВа 2+ / СPb 2+ >46700, то первым из раствора будет выпадать ВаСО3 до тех пор, пока отношение СВа 2+ / СPb 2+ не будет равным 46700. И только после этого начнется одновременное выпадение осадков. Если же отношение концентрации ионов бария и свинца меньше 46700, то первым начнет осаждаться карбонат свинца. Осаждение карбоната свинца будет протекать до тех пор, пока отношение СВа 2+ / СPb 2+ не достигнет значения, при котором ВаСО3 и РbСО3 будут осаждаться одновременно.
Осадок
Резюме
Химический подход
Продукт растворимости
Наличие стабильного осадка является результатом термодинамического равновесия между жидкой фазой ( раствором ) и твердой фазой (солью).
Осаждение обозначается как химическое уравнение :
и потенциал этой постоянной p K s :
Механизмы осадков
Использует
Материальный подход
В металлургии и материаловедении в целом нас интересуют два явления:
В обоих случаях формирование этой гетерогенной фазы происходит в два этапа:
Затвердевание
Прорастание
В случае затвердевания прорастание обычно происходит при охлаждении.
Термодинамически создание кристалла высвобождает энергию, но также требует ее из-за создания границы раздела твердое тело-жидкость ( поверхностное натяжение ); Чтобы прорастание происходило, оно должно быть термодинамически благоприятным, то есть энергия, выделяемая при расположении атомов, компенсирует поверхностное натяжение.
Твердофазное осаждение
Внутри сплава происходит выделение твердой фазы. Как правило, это основной металл M, содержащий незначительное количество сплава A. Когда концентрация легирующего элемента A низкая, имеется гомогенная фаза, состоящая из твердого раствора A в M (см. Статью Одноразовая неисправность ).
Если температура повышается и C s ( T ) становится больше, чем концентрация A в фазе M, тогда происходит растворение осадков, все еще находящихся в твердой фазе.
На самом деле это явление более сложное, потому что обычно существует несколько легирующих элементов, которые влияют на фазовую стабильность.
Прорастание
Осаждение твердой фазы также происходит при медленном охлаждении ( закалка может предотвратить осаждение).
Как и в случае затвердевания, поверхностное натяжение вызывает прорастание при температуре ниже температуры растворения осадка.
Рост относится к увеличению или увеличению размера кристаллов.
Коалесценция
Подход в биохимии / иммунохимии
Осадки вступают в игру:
Что такое выпадение осадка
В атмосфере всегда имеется некоторое количество влаги в виде водяного пара, испарившегося с поверхности океанов, озер, рек, почвы и т. д. Испарение зависит от температуры воздуха, ветра (даже слабый ветер увеличивает испарение раза в 3, т. к. все время уносит насыщенный водяными парами воздух и приносит новые порции сухого), характера рельефа, растительного покрова, цвета почвы.
Различают испаряемость – количество воды, которое могло бы испариться при данных условиях в единицу времени, и испарение – действительно испарившееся количество воды. В пустыне испаряемость велика, а испарение незначительно.
Насыщение воздуха. При каждой конкретной температуре воздух может принимать водяные пары до известного предела (до насыщения). Чем выше температура, тем большее количество воды может содержать воздух. Если охлаждать ненасыщенный воздух, он постепенно будет приближаться к точке насыщения. Температура, при которой данный ненасыщенный воздух переходит к насыщению, называется точкой росы. Если насыщенный воздух охлаждать дальше, то в нем начнется сгущение избыточных водяных паров. Влага начнет конденсироваться, образуются облака, затем выпадают осадки.
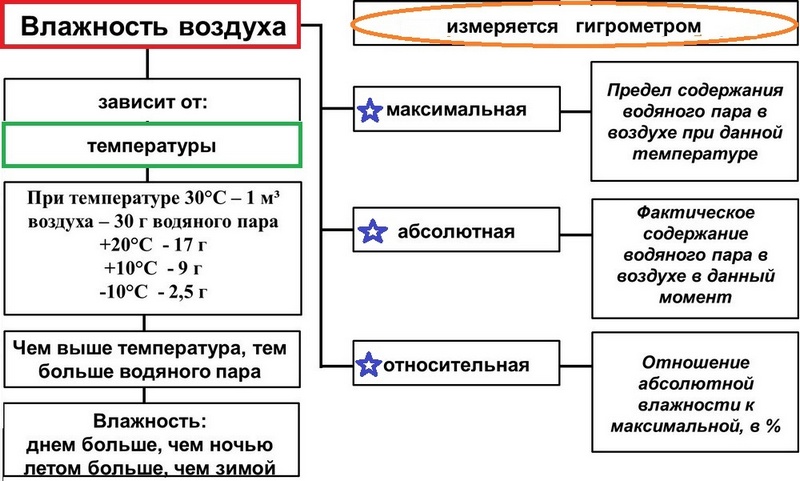
Следовательно, для характеристики погоды необходимо знать относительную влажность воздуха – процентное соотношение количества водяных паров, содержащихся в воздухе, к тому количеству, которое он может содержать при насыщении.
Абсолютная влажность – количество водяного пара в граммах, находящегося в данный момент в 1 м3 воздуха.
Атмосферные осадки и их образование.
Атмосферные осадки – вода в жидком или твердом состоянии, выпадающая с облаков. Облаками называются скопления взвешенных в атмосфере продуктов конденсации водяного пара – капелек воды или кристалликов льда. В зависимости от сочетания температуры и степени увлажнения образуются капельки или кристаллики разной формы и величины. Мелкие капельки плавают в воздухе, более крупные начинают падать в виде мороси (измороси) или мелкого дождя. При низких температурах образуются снежинки.
Схема образования осадков такова: воздух охлаждается (чаще при подъеме вверх), приближается к насыщению, водяные пары конденсируются, образуются осадки.
Измерение количества осадков происходит с помощью дождемера – металлического ведра цилиндрической формы высотой 40 см и площадью сечения 500 см2. Все измерения количества осадков суммируются за каждый месяц, и выводят месячное, а затем годовое количество осадков.
Факторы, влияющие на количество осадков
Количество осадков на территории зависит от:
Выпадение осадков неравномерно. Оно подчиняется закону зональности, т. е. изменяется от экватора к полюсам.
В тропических и умеренных широтах количество осадков значительно изменяется при движении от побережий в глубь материков, что зависит от многих факторов (циркуляции атмосферы, наличия океанических течений, рельефа и т. п.).
Выпадение осадков на большей территории земного шара происходит неравномерно в течение года. Возле экватора в течение года количество осадков изменятся незначительно, в субэкваторальных широтах выделяют сухой сезон (до 8 месяцев), связанный с действием тропических воздушных масс, и дождевой (до 4 месяцев) сезон, связанный с приходом экваториальных воздушных масс. При движении от экватора к тропикам продолжительность сухого сезона возрастает, а дождевого – уменьшается. В субтропических широтах преобладают зимние осадки (их приносят умеренные воздушные массы). В умеренных широтах осадки выпадают в течение всего года, но во внутренних частях материков большее количество осадков выпадает в теплое время года. В полярных широтах также преобладают летние осадки.
Таблица «Вода в атмосфере»
Конспект урока «Влажность. Осадки». Следующая тема: «Климат»
Что такое выпадение осадка
Глава 4. Произведение растворимости
§ 19. Условия осаждения и растворения
При проведении в растворе таких реакций, которые могут привести к выделению осадка, существует определенное требование к значению аналитических концентраций реагентов − условие выпадения осадка.
Образование осадка малорастворимого сильного электролита МxАy произойдет только тогда, когда после смешивания растворов реагентов в конечном объеме смеси будет соблюдаться соотношение
где в круглых скобках стоят выбранные (по условию проведения опыта) молярные концентрации катионов и анионов в конечном растворе (после смешивания растворов реагентов).
Если условие выпадения осадка не выполняется, т.е. (сM y+ ) x · (сА x− ) y >>
Рассмотрим насыщенный раствор труднорастворимого сильного электролита, где содержится наряду с жидкой фазой и кристаллический осадок. Если удастся осуществить некоторые операции, в результате которых произведение концентраций ионов в растворе над осадком станет меньше произведения растворимости: (сM y+ ) x · (сА x− ) y −12 ), осадок будет выпадать.
Наоборот, выпавший осадок Mg(OH)2 начнет растворяться, если один из ионов, присутствующих в растворе над осадком, мы будем выводить из сферы реакции и связывать тем или иным способом (одновременно в раствор из осадка будет поступать второй ион, а ПР останется неизменным до тех пор, пока существует твердая фаза).
Такое растворение обусловлено смещением фазового равновесия по принципу Ле Шателье.
Если требуется растворить осадок, следует связывать ионы из насыщенного раствора путем перевода их
а) в слабую кислоту или слабое основание,
б) в прочный комплекс
в) в другой труднорастворимый осадок.
(осадок гидроксида магния растворяется, в результате получается слабое основание − гидрат аммиака)
Знание описанных выше закономерностей позволяет целенаправленно вести осаждение и растворение труднорастворимых сильных электролитов и успешно применять такие процессы в практических целях.
Что такое выпадение осадка
В гравиметрическом анализе к осадку предъявляется ряд требований.
1 Осадок должен быть практически нерастворим. Для уменьшения растворимости обычно применяют избыток осадителя (см. разд. 5.1.1). Осадки часто представляют собой соли слабых кислот, поэтому полнота их осаждения зависит от концентрации ионов водорода в растворе (см. разд. 5.1.3).
2 Гравиметрическая форма после высушивания или прокаливания должна соответствовать определенной формуле. Это требование связано с чистотой осадка, так как при его образовании из раствора могут быть захвачены посторонние вещества. Кроме того, некоторые осадки имеют переменный состав, например, фосфаты двухвалентных металлов: МеНРО4 и (Ме)3(РО4)2, что не позволяет использовать их в количественном анализе.
3 Осадок должен получаться в форме, удобной для отделения его от раствора фильтрованием. Это требование связано, главным образом, с размерами зерна осадка.
Образование осадков и их свойства
Создание оптимальных условий осаждения при количественных определениях имеет большое значение, так как потери вещества здесь недопустимы.
В процессе формирования осадка очень большое значение имеет пересыщение раствора. Его характеризуют так называемым относительным пересыщением:
где Q – концентрация осаждаемого вещества, S – его растворимость. Из приведенной формулы следует, что чем выше будет растворимость образующегося осадка и чем ниже концентрация осаждаемого вещества и осадителя, тем меньше будет относительное пересыщение, меньше число первичных кристаллов, и тем крупнее они будут.
Таким образом, можно сформулировать правила осаждения кристаллических осадков:
1 Вести осаждение из достаточно разбавленного раствора разбавленным раствором осадителя.
2 Прибавлять осадитель медленно, особенно в начале осаждения.
3 Непрерывно перемешивать раствор, чтобы избежать местных пересыщений при добавлении осадителя.
4 Вести осаждение из горячего раствора (иногда нагревают и раствор осадителя).
5 Прибавлять при осаждении вещества, повышающие растворимость осадка.
При образовании кристаллических осадков нередко достаточно полное выделение соответствующего вещества из раствора происходит не сразу, а через более или менее длительный промежуток времени. Поэтому в таких случаях после добавления осадителя реакционную смесь оставляют на несколько часов для созревания осадка. При этом происходит ряд процессов, приводящих к укрупнению кристаллов осадка и получению их в чистой, практически свободной от примесей форме.
Причиной укрупнения кристаллов является растворение мелких кристаллов и рост за их счет более крупных кристаллов. Это явление объясняется поверхностным натяжением, стремящимся возможно сильнее уменьшить поверхность соприкосновения раствора с осадком. В результате мелкие кристаллы растворяются, и происходит рост крупных кристаллов. Вследствие меньшей растворимости крупных кристаллов раствор, насыщенный относительно них, является ненасыщенным относительно мелких кристаллов, которые растворяются. При этом раствор становится пересыщенным относительно крупных кристаллов, и растворенное вещество отлагается на их поверхности. Течение указанных процессов связано с диффузией вещества в растворе от мелких кристаллов к крупным, которая протекает при комнатной температуре достаточно медленно. Повышение температуры ускоряет диффузию и увеличивает растворимость, поэтому ускоряет созревание осадка.
Важным процессом, происходящим при созревании осадка, является совершенствование формы кристаллов, и, как следствие, повышение чистоты осадка. Вследствие динамического равновесия между раствором и осадком одни ионы (обычно образующие дефекты на поверхности кристаллической решетки) переходят в раствор с поверхности твердой фазы, а другие осаждаются на ее поверхности. В результате такой перекристаллизации образуются кристаллы более правильной формы.
Другим фактором устойчивости коллоидных систем является сольватация (гидратация) коллоидных частиц, т.е. адсорбция ими молекул растворителя. В результате этого коллоидные частицы окружаются сольватными оболочками, препятствующими их соединению в более крупные агрегаты. Разрушение сольватных оболочек может быть достигнуто за счет добавления электролитов достаточно высокой концентрации. Ионы электролитов, сольватируясь, отнимают молекулы растворителя от коллоидных частиц, а также нейтрализуют заряды этих частиц, что способствует их коагуляции.
Коагуляции способствует повышение температуры раствора. Оно уменьшает адсорбцию ионов и способствует разрушению сольватных оболочек частиц.
Таким образом, правила осаждения аморфных осадков следующие:
· Проводить осаждение из концентрированного раствора концентрированным раствором осадителя.
· Проводить осаждение из горячего раствора.
· Проводить осаждение в присутствии подходящего электролита-коагулянта.
Аморфные осадки после осаждения сразу подвергают дальнейшим операциям: перенесению на фильтр и промыванию для предотвращения образования скрытокристаллической структуры при выдерживании под реакционным раствором.