Содержание
Решения и сольватация
Когда одно вещество растворенный в другой, решение сформирован. [2] Это противоположно ситуации, когда соединения нерастворимый как песок в воде. В растворе все ингредиенты равномерно распределены на молекулярном уровне и не остается остатков. Смесь растворителя и растворенного вещества состоит из одного фаза со всеми молекулами растворенного вещества, встречающимися как сольваты (растворитель-растворенный комплексы), в отличие от отдельных непрерывных фаз, как в суспензиях, эмульсиях и других типах смесей, не являющихся растворами. Способность одного соединения растворяться в другом известна как растворимость; если это происходит во всех пропорциях, это называется смешивающийся.
Помимо перемешивания, вещества в растворе взаимодействуют друг с другом на молекулярном уровне. Когда что-то растворяется, молекулы растворителя располагаются вокруг молекулы растворенного вещества. Теплопередача участвует и энтропия увеличивается, делая решение более термодинамически стабильнее, чем растворенное вещество и растворитель по отдельности. Такое расположение опосредуется соответствующими химическими свойствами растворителя и растворенного вещества, такими как водородная связь, дипольный момент и поляризуемость. [3] Сольватация не вызывает химической реакции или изменений химической конфигурации растворенного вещества. Однако сольватация напоминает координационный комплекс реакция образования, часто со значительной энергетикой (теплота сольватации и энтропия сольватации) и, таким образом, далека от нейтрального процесса.
Классификация растворителей
Растворители можно условно разделить на две категории: полярный и неполярный. Особый случай Меркурий, решения которой известны как амальгамы; также другие металлические решения существуют жидкие при комнатной температуре. Как правило, диэлектрическая постоянная Количество растворителя позволяет приблизительно определить полярность растворителя. На сильную полярность воды указывает ее высокая диэлектрическая проницаемость 88 (при 0 ° C). [4] Растворители с диэлектрической проницаемостью менее 15 обычно считаются неполярными. [5] Диэлектрическая проницаемость измеряет тенденцию растворителя частично компенсировать напряженность электрического поля заряженная частица погрузился в него. Это сокращение затем сравнивается с напряженность поля заряженной частицы в вакууме. [5] Эвристически диэлектрическую проницаемость растворителя можно рассматривать как его способность снижать эффективность растворенного вещества. внутренний заряд. Как правило, диэлектрическая проницаемость растворителя является приемлемым показателем способности растворителя растворять обычные ионные соединения, например соли.
Другие шкалы полярности
В Грюнвальд – Винштейн мY шкала измеряет полярность с точки зрения влияния растворителя на накопление положительного заряда растворенного вещества во время химической реакции.
Kosowerс Z шкала измеряет полярность с точки зрения влияния растворителя на УФ-максимумы поглощения соли, обычно пиридиний йодид или пиридиний цвиттерион. [6]
Номер донора и шкала акцептора донора измеряет полярность с точки зрения того, как растворитель взаимодействует с определенными веществами, например, сильным Кислота Льюиса или сильная база Льюиса. [7]
В Параметр Хильдебранда квадратный корень из плотность когезионной энергии. Его можно использовать с неполярными соединениями, но он не подходит для сложных химических процессов.
Полярность, дипольный момент, поляризуемость и водородная связь растворителя определяет, какой тип соединения он способен растворяться и с какими другими растворителями или жидкими соединениями он смешивающийся. Обычно полярные растворители лучше всего растворяют полярные соединения, а неполярные растворители лучше всего растворяют неполярные соединения: «подобное растворяется в подобном». Сильно полярные соединения, такие как сахара (например, сахароза) или ионные соединения, такие как неорганический соли (например. столовая соль) растворяются только в очень полярных растворителях, таких как вода, в то время как сильно неполярные соединения, такие как масла или же воск растворяются только в очень неполярных органических растворителях, таких как гексан. Точно так же вода и гексан (или же уксус и растительное масло) не смешивающийся друг с другом и быстро разделятся на два слоя даже после хорошего встряхивания.
Полярность может быть разделена на разные вклады. Например, Параметры Камлета-Тафта диполярность / поляризуемость (π *), водородно-связывающая кислотность (α) и основность водородных связей (β). Их можно рассчитать по сдвигу длин волн 3–6 различных сольватохромных красителей в растворителе, обычно включая Краситель Рейхардта, нитроанилин и диэтилнитроанилин. Другой вариант, параметры Хансена, разделяют плотность энергии когезии на вклады дисперсии, полярности и водородных связей.
Полярный протон и полярный апротический
Многокомпонентный
Многокомпонентные растворители появились после Второй мировой войны в СССР и продолжают использоваться и производиться в постсоветских странах.
Растворители
| Имя | Сочинение |
|---|---|
| Растворитель 645 | толуол 50%, бутилацетат 18%, этилацетат 12%, бутанол 10%, этанол 10%. |
| Растворитель 646 | толуол 50%, этиловый спирт 15%, бутанол 10%, бутил- или амилацетат 10%, этилцеллозольв 8%, ацетон 7% [9] |
| Растворитель 647 | бутилацетат или амилацетат 29,8%, ацетат этила 21,2%, бутанол 7,7%, толуол или пиробензол 41.3% [10] |
| Растворитель 648 | бутил ацетат 50%, этанол 10%, бутанол 20%, толуол 20% [11] |
| Растворитель 649 | этилцеллозольв 30%, бутанол 20%, ксилол 50% |
| Растворитель 650 | этилцеллозольв 20%, бутанол 30%, ксилол 50% [12] |
| Растворитель 651 | белый дух 90%, бутанол 10% |
| Растворитель КР-36 | бутилацетат 20%, бутанол 80% |
| Растворитель П-4 | толуол 62%, ацетон 26%, бутилацетат 12%. |
| Растворитель П-10 | ксилол 85%, ацетон 15%. |
| Растворитель П-12 | толуол 60%, бутилацетат 30%, ксилол 10%. |
| Растворитель П-14 | циклогексанон 50%, толуол 50%. |
| Растворитель П-24 | растворитель 50%, ксилол 35%, ацетон 15%. |
| Растворитель П-40 | толуол 50%, этилцеллозольв 30%, ацетон 20%. |
| Растворитель П-219 | толуол 34%, циклогексанон 33%, ацетон 33%. |
| Растворитель Р-3160 | бутанол 60%, этанол 40%. |
| Растворитель RCC | ксилол 90%, бутилацетат 10%. |
| Растворитель РМЛ | этанол 64%, этилцеллозольв 16%, толуол 10%, бутанол 10%. |
| Растворитель ПМЛ-315 | толуол 25%, ксилол 25%, бутилацетат 18%, этилцеллозольв 17%, бутанол 15%. |
| Растворитель ПК-1 | толуол 60%, бутилацетат 30%, ксилол 10%. |
| Растворитель ПК-2 | уайт-спирит 70%, ксилол 30%. |
| Растворитель RFG | этанол 75%, бутанол 25%. |
| Растворитель РЭ-1 | ксилол 50%, ацетон 20%, бутанол 15%, этанол 15%. |
| Растворитель РЕ-2 | Растворитель 70%, этанол 20%, ацетон 10%. |
| Растворитель РЭ-3 | растворитель 50%, этанол 20%, ацетон 20%, этилцеллозольв 10%. |
| Растворитель РЭ-4 | растворитель 50%, ацетон 30%, этанол 20%. |
| Растворитель ФК-1 (?) | абсолютный спирт (99,8%) 95%, этилацетат 5% |
Разбавители
| Имя | Сочинение |
|---|---|
| Разбавитель РКБ-1 | бутанол 50%, ксилол 50% |
| Разбавитель РКБ-2 | бутанол 95%, ксилол 5% |
| Разбавитель РКБ-3 | ксилол 90%, бутанол 10% |
| Разбавитель М | этанол 65%, бутилацетат 30%, этилацетат 5%. |
| Разбавитель П-7 | циклогексанон 50%, этанол 50%. |
| Разбавитель Р-197 | ксилол 60%, бутилацетат 20%, этилцеллозольв 20%. |
| Разбавитель WFD | толуол 50%, бутилацетат (или амилацетат) 18%, бутанол 10%, этанол 10%, этилацетат 9%, ацетон 3%. |
Физические свойства
Таблица свойств распространенных растворителей
Растворители сгруппированы в неполярный, полярный апротический, и полярный протический растворители, причем каждая группа упорядочена по возрастанию полярности. В характеристики растворители, превышающие водные, выделены жирным шрифтом.
| Растворитель | Химическая формула | Точка кипения [13] (° C) | Диэлектрическая постоянная [14] | Плотность (г / мл) | Дипольный момент (D) |
|---|---|---|---|---|---|
| 36.1 | 1.84 | 0.626 | 0.00 | ||
| Циклопентан | 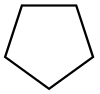 C5ЧАС10 | 49.2 | 1.97 | 0.751 | 0.00 |
| Гексан | 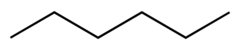 | 69 | 1.88 | 0.655 | 0.00 |
| Циклогексан |  C6ЧАС12 | 80.7 | 2.02 | 0.779 | 0.00 |
| Бензол | 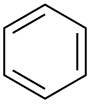 C6ЧАС6 | 80.1 | 2.3 | 0.879 | 0.00 |
| Тетрахлорметан | CCl4 | 76.7 | 2.3 | 1.5867 | 0.00 |
| Толуол | C6ЧАС5-CH3 | 111 | 2.38 | 0.867 | 0.36 |
| 1,4-диоксан |  C4ЧАС8О2 | 101.1 | 2.3 | 1.033 | 0.45 |
| Диэтиловый эфир |  Полярный апротический растворители | 100–103 | 35.87 | 1.1371 | 3.56 |
| Пропиленкарбонат |  Полярный протический растворители | 1.42 | |||
| Муравьиная кислота | 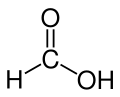 Н-С (= O) ОН | 100.8 | 58 | 1.21 | 1.41 |
| п-Бутанол |  | 64.7 | 33 | 0.791 | 1.70 |
| Уксусная кислота |  CH3-С (= О) ОН | 118 | 6.2 | 1.049 | 1.74 |
| Вода |  H-O-H | 100 | 80 | 1.000 | 1.85 |
В ACS Green Chemistry Institute поддерживает инструмент для выбора растворителей на основе Анализ главных компонентов свойств растворителя. [15]
Значения параметра растворимости Хансена
| Растворитель | Химическая формула | δD Дисперсия | δP Полярный | δH Водородная связь | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Растворитель | Точка кипения (° C) [13] |
|---|---|
| этилендихлорид | 83.48 |
| пиридин | 115.25 |
| метилизобутилкетон | 116.5 |
| метиленхлорид | 39.75 |
| изооктан | 99.24 |
| сероуглерод | 46.3 |
| четыреххлористый углерод | 76.75 |
| о-ксилол | 144.42 |
Температура кипения является важным свойством, поскольку от нее зависит скорость испарения. Небольшие количества растворителей с низкой температурой кипения, например диэтиловый эфир, дихлорметан, или ацетон испарится за секунды при комнатной температуре, в то время как растворители с высокой точкой кипения, такие как вода или диметилсульфоксид нужны более высокие температуры, воздушный поток или нанесение вакуум для быстрого испарения.
Плотность
Большинство органических растворителей имеют более низкую плотность чем вода, что означает, что они легче, чем вода, и образуют слой поверх нее. Важными исключениями являются большинство галогенированный растворители, такие как дихлорметан или же хлороформ опустится на дно емкости, оставив воду в качестве верхнего слоя. Это очень важно помнить, когда разделение соединения между растворителями и водой в разделительная воронка во время химического синтеза.
Часто, удельный вес цитируется вместо плотности. Удельный вес определяется как отношение плотности растворителя к плотности воды при той же температуре. Таким образом, удельный вес является безразмерным значением. Он легко сообщает, будет ли нерастворимый в воде растворитель плавать (SG 1,0) при смешивании с водой.
| Растворитель | Удельный вес [18] |
|---|---|
| Пентан | 0.626 |
| Петролейный эфир | 0.656 |
| Гексан | 0.659 |
| Гептан | 0.684 |
| Диэтиламин | 0.707 |
| Диэтиловый эфир | 0.713 |
| Триэтиламин | 0.728 |
| Трет-бутилметиловый эфир | 0.741 |
| Циклогексан | 0.779 |
| Трет-бутиловый спирт | 0.781 |
| Изопропанол | 0.785 |
| Ацетонитрил | 0.786 |
| Этиловый спирт | 0.789 |
| Ацетон | 0.790 |
| Метанол | 0.791 |
| Метилизобутилкетон | 0.798 |
| Изобутиловый спирт | 0.802 |
| 1-пропанол | 0.803 |
| Метилэтилкетон | 0.805 |
| 2-бутанол | 0.808 |
| Изоамиловый спирт | 0.809 |
| 1-бутанол | 0.810 |
| Диэтилкетон | 0.814 |
| 1-октанол | 0.826 |
| п-ксилол | 0.861 |
| м-ксилол | 0.864 |
| Толуол | 0.867 |
| Диметоксиэтан | 0.868 |
| Бензол | 0.879 |
| Бутил ацетат | 0.882 |
| 1-хлорбутан | 0.886 |
| Тетрагидрофуран | 0.889 |
| Ацетат этила | 0.895 |
| о-ксилол | 0.897 |
| Триамид гексаметилфосфора | 0.898 |
| 2-этоксиэтиловый эфир | 0.909 |
| N, N-диметилацетамид | 0.937 |
| Диметиловый эфир диэтиленгликоля | 0.943 |
| N, N-диметилформамид | 0.944 |
| 2-метоксиэтанол | 0.965 |
| Пиридин | 0.982 |
| Пропановая кислота | 0.993 |
| Вода | 1.000 |
| 2-метоксиэтилацетат | 1.009 |
| Бензонитрил | 1.01 |
| 1-метил-2-пирролидинон | 1.028 |
| Гексаметилфосфорамид | 1.03 |
| 1,4-диоксан | 1.033 |
| Уксусная кислота | 1.049 |
| Уксусный ангидрид | 1.08 |
| Диметилсульфоксид | 1.092 |
| Хлорбензол | 1.1066 |
| Оксид дейтерия | 1.107 |
| Этиленгликоль | 1.115 |
| Диэтиленгликоль гликоль | 1.118 |
| Пропиленкарбонат | 1.21 |
| Муравьиная кислота | 1.22 |
| 1,2-дихлорэтан | 1.245 |
| Глицерин | 1.261 |
| Сероуглерод | 1.263 |
| 1,2-дихлорбензол | 1.306 |
| Метиленхлорид | 1.325 |
| Нитрометан | 1.382 |
| 2,2,2-Трифторэтанол | 1.393 |
| Хлороформ | 1.498 |
| 1,1,2-трихлортрифторэтан | 1.575 |
| Тетрахлорметан | 1.594 |
| Тетрахлорэтилен | 1.623 |
Безопасность
Огонь
Большинство органических растворителей легко или легко воспламеняются в зависимости от их летучести. Исключение составляют некоторые хлорированные растворители, например дихлорметан и хлороформ. Смеси паров растворителей и воздуха могут взорваться. Пары растворителя тяжелее воздуха; они опускаются на дно и могут преодолевать большие расстояния почти в неразбавленном виде. Пары растворителя также можно найти в предположительно пустых бочках и банках, что создает вспышка огня опасность; следовательно, пустые емкости с летучими растворителями следует хранить открытыми и перевернутыми.
Обе диэтиловый эфир и сероуглерод имеют исключительно низкий температуры самовоспламенения которые значительно увеличивают риск возгорания, связанный с этими растворителями. Температура самовоспламенения сероуглерода ниже 100 ° C (212 ° F), поэтому такие предметы, как пар трубы лампочки, конфорки, и недавно погашенный горелки Бунзена способны воспламенить его пары.
Кроме того, некоторые растворители, такие как метанол, могут гореть очень горячим пламенем, которое может быть почти невидимым при некоторых условиях освещения. [19] [20] Это может задержать или предотвратить своевременное распознавание опасного пожара до тех пор, пока пламя не перейдет на другие материалы.
Взрывоопасное образование перекиси
Гетероатом (кислород) стабилизирует образование свободный радикал который образован абстракцией водород атом другим свободным радикалом. [ требуется разъяснение ] Образованный таким образом углерод-центрированный свободный радикал способен реагировать с молекулой кислорода с образованием пероксидного соединения. Процесс образования перекиси значительно ускоряется даже при слабом освещении, но может протекать медленно даже в темноте.
Чтобы избежать взрывоопасного образования пероксида, эфиры следует хранить в герметичном контейнере, вдали от света, потому что и свет, и воздух могут способствовать образованию пероксида. [21]
Пероксиды можно удалить промыванием кислым сульфатом железа (II), фильтрованием через глинозем, или же дистилляция из натрий/бензофенон. Оксид алюминия не разрушает пероксиды, а просто улавливает их, и от него необходимо утилизировать надлежащим образом. Преимущество использования натрия / бензофенона заключается в том, что влага и кислород также удаляются. [ нужна цитата ]
Влияние на здоровье
Общие опасности для здоровья, связанные с воздействием растворителей, включают токсичность для нервной системы, повреждение репродуктивной системы, повреждение печени и почек, нарушение дыхания, рак и дерматит. [22]
Острое воздействие
Хроническое воздействие
Некоторые растворители, включая хлороформ и бензол общий ингредиент в бензин известны как канцерогенный, в то время как многие другие рассматриваются Всемирная организация здоровья вероятно, канцерогены. Растворители могут повредить внутренние органы, например печень, то почки, то нервная система, или мозг. Кумулятивные эффекты длительного или многократного воздействия растворителей называются хроническая энцефалопатия, вызванная растворителями (CSE).
Хроническое воздействие органических растворителей в рабочей среде может вызвать ряд неблагоприятных психоневрологических эффектов. Например, профессиональное воздействие органических растворителей было связано с увеличением числа художников, страдающих от алкоголизм. [26] Этанол имеет синергетический эффект при приеме в сочетании со многими растворителями; например, сочетание толуол/бензол а этанол вызывает большее тошнота/рвота чем любое вещество в отдельности.
Известно или предполагается, что многие растворители обладают катарактогенными свойствами, что значительно увеличивает риск развития катаракта в хрусталике глаза. [27] Воздействие растворителей также было связано с нейротоксическим повреждением, вызывающим потеря слуха [28] [29] и цветовое зрение убытки. [30]
Загрязнение окружающей среды
РАСТВОРИТЕЛИ И РАЗБАВИТЕЛИ
Форумы полнятся вопросами о том, из чего состоит тот или иной фирменный состав разбавителя для акриловых или полиуретановых красок, как его заменить, на чём сэкономить, чем смывать и разбавлять краску и т.п.
Всё это происходит на фоне полнейшего тумана со стороны производителей (или продавцов) красок, не желающих раскрывать профессиональные секреты (а некоторые просто не знают ответов на некоторые вопросы покупателей J )
Попробуем изложить то, что известно на эту тему мне с общетеоритечиских позиций и примерами из практики.
Сначала длинное теоретическое предисловие, которое стоит прочитать:
Молекула может быть диполем (например, вода или большинство спиртов).
А может и не быть (например, бензол).
Растворители, молекула которых является диполем, называются полярными.
Растворители, молекула которых диполем не является, называются неполярными.
В теории тот состав, который растворяется каким-то полярным растворителем, может быть растворен другим полярным растворителем той же или более высокой полярности.
Точно так же, эмали можно растворять маслами, производными бензина, бензола и т.п.
Практические примеры:
Стандартный фирменный растворитель для акрила представляет собой 60-65% раствор изопропилового спирта в дистиллированной воде с содержанием примерно 7% пропиленгликоля.
Важно, чтобы вода была деминерализована, поскольку иначе соли могут повысить или понизить ту самую полярность с плохо предсказуемыми результатами.
Еще нужно отметить, что коммерческие растворители для использования в помещении чаще всего используют неядовитые (слабо ядовитые) вещества.
Фирменный растворитель для эмалей устроен схожим образом, но без воды. В нем основой выступает уайт-спирит, а в качестве ретардера используется минеральное масло (меняется от года к году).
Эмали, в принципе, можно растворять и чистым уайт-спиритом, и сохнет она тогда быстрее, но это не рекомендуется.
Масло в большинстве красок используется как красочная основа, и если его недостаточно, то получившаяся смесь ведет себя неоднородно, как очень жидкая суспензия.
Стойкими к абсолютизированному изопропанолу являются только 2-компонентные краски с отвердителем после полной полимеризации.
Теперь несколько слов про лаки и металлики, а также растворители с переменной полярностью.
Ацетон слабо растворяет пластик, так что разведенные им краски въедаются в поверхностный слой, а если покрытие смыть, то поверхность будет матовой. Так что при добавлении растворителя для лаков и металликов к акрилам можно работать без грунта, что удобно для базового покрытия.
Точно так же полистирол растворяется этилацетатом или дихлорэтаном.
Все эти вещества характерны еще и тем, что расщепляют жиры и некоторые углеводороды, и умеют растворять как эмали, так и водорастворимые акрилы.
Жидкость для очистки аэрографа чаще всего представляет собой тот же бутилацетат или дихлорэтан с добавками. Она не просто растворяет пластик, как ацетон, она его проплавляет в глубину. При этом фактура поверхности обычно нарушается, но получившееся покрытие смыть становится совершенно невозможно. В жидкости для очистки аэрографов можно растворять любые краски, но использовать получившуюся смесь следует очень осторожно, тонким напылением, ни в коем случае не на кисти.
Напоследок несколько слов о тех растворителях, которые продаются в хозяйственных магазинах.
Продукция отечественного химпрома не отличается ни чистотой ни экологичностью, так что лучше не экономить.
Растворители 646 и 647 предназначены прежде всего для растворения нитроэмалей, которые (за исключением баллончиков) в моделизме используются нечасто. В основном они состоят из толуола (от 40%), бутилацетата и этилацетата. В 646-й рецептуре больше толуола (порядка половины), и есть также этиловый спирт и ацетон, он лучше испаряется и оставляет меньше следов.
Обратите внимание: в советских растворителях отсутствует ингибитор/ретардер.




