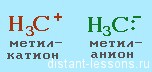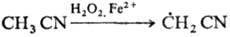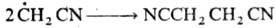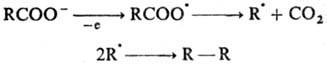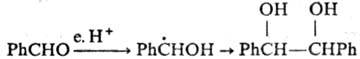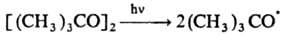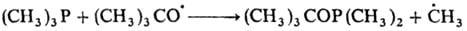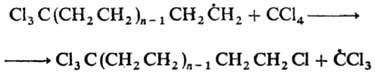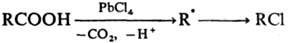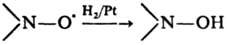Химия, Биология, подготовка к ГИА и ЕГЭ
Ионный и радикальный механизмы
химических реакций органической химии
Ионный механизм химической реакции
Судя по названию, ионный механизм реакции — это механизм, приводящий к образованию ионов. Соответственно, образуются органические катионы и анионы — карбокатионы или карбоанионы.
Такие ионы образуются при разрыве полярных ковалентных связей в органическом веществе.
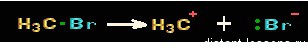
Гетеролитический разрыв связей:
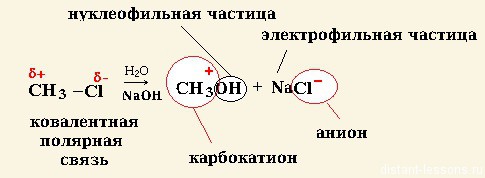
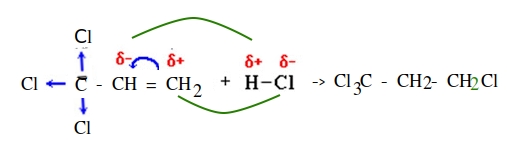
Пример ионного механизма химической органической реакции:
Нуклеофильные частицы:
Электрофильные частицы:
Электрофильные и нуклеофильные реакции
Нуклеофильные реакции — органическое вещество реагирует с нуклеофильным реагентом.
S N — substitution nucleophile
Ad N — addition nucleophile
нуклеофильное замещение протекает в тяжелых условиях ( t,p),
но если в бензольном кольце будут электроноакцепторные
заместители, то реакции пойдут намного легче,
электронодонорные — наоборот — затрудняют реакцию
Электрофильные реакции — органическое вещество реагирует с электрофильным реагентом
S E Ar — substitution electrophilic reaction
Ad E — addition electrophilic reaction
( образуется промежуточная частица NO 2 + )
В органической химии чаще всего атакующей электрофильной частицей является протон H +
бромирование кратной связи
гидратация двойной связи
присоединение аминов или NH3
Присоединение по правилу Марковникова — типичный пример ионного типа механизма химической реакции:
водород присоединяется к наиболее гидрогенизированному атому углерода при двойной связи.
В основном, это реакции присоединения к кратным связям или обменные реакции.
Присоединение против правила Марковникова:
Ионные реакции проводят:
Радикальный механизм химической реакции
— механизм, приводящий к образованию радикалов.
Соответственно, образуются органические частицы — радикалы — имеющие неспаренный электрон.
Такие частицы образуются при разрыве неполярных \ слабо полярных ковалентных связей в органическом веществе.
Гомолитический разрыв связей:
Образовавшиеся радикалы могут взаимодействовать друг с другом.
Классическая реакция, идущая по радикальному механизму — хлорирование метана (обязательно на свету):
Радикальные реакции проводят:
Механизмы реакций в органической химии
Ионный (правило В.В. Марковникова) и радикальный механизмы реакций в органической химии.
Механизмы разрыва химических связей в органических реакциях
| Гомолитический разрыв связи – это такой разрыв химической связи, когда каждый атом получает при разрыве связи по одному электрону из общей электронной пары. |
Образующиеся при этом частицы — это свободные радикалы.
| Свободные радикалы – это частицы, каждая из которых содержит один неспаренный электрон. A:B → A∙ + ∙B Гомолитический разрыв связи характерен для слабо полярных или неполярных связей. Условия протекания радикальных реакций: То есть реакция протекает как цепь последовательных превращений с участием свободных радикалов. Свободные радикалы R∙ – это атомы или группы связанных между собой атомов, которые содержат один или несколько неспаренных электронов. Свободные радикалы – очень активные частицы, которые стремятся образовать связь с каким-либо другим атомом. Этапы радикально-цепного процесса: Стадия 1. Инициирование цепи. Под действием кванта света или при нагревании молекула галогена распадается на радикалы: Cl:Cl → Cl⋅ + ⋅Cl Стадия 2. Развитие цепи. Радикалы взаимодействуют с молекулами с образованием новых молекул и радикалов. Радикал галогена взаимодействует с молекулой алкана и отрывает от него водород. При этом образуется промежуточная частица – алкильный радикал, который в свою очередь взаимодействует с молекулой хлора: CH4 + ⋅Cl → CH3⋅ + HCl Стадия 3. Обрыв цепи. При протекании цепного процесса рано или поздно радикалы сталкиваются с радикалами. При этом образуются молекулы, т.е. радикальный процесс обрывается. Могут столкнуться разные радикалы, в том числе два метильных радикала:
При гетеролитическом разрыве связи образуются ионы – положительно заряженный катион и отрицательно заряженный анион. A:B → A: – + B +
Гетеролитический (ионный) механизм характерен для полярных и легко поляризуемых связей. Условия протекания ионных реакций: Присоединение галогеноводородов (гидрогалогенирование). Например, этилен взаимодействует с бромоводородом: Реакция протекают по механизму электрофильного присоединения в несколько стадий. II стадия. Карбокатион взаимодействует с анионом Br – : При присоединении галогеноводородов и других полярных молекул к симметричным алкенам образуется одно вещество. При присоединении полярных молекул к несимметричным алкенам образуется смесь изомеров. При этом выполняется правило Марковникова.
В некоторых случаях присоединение к двойным связям происходит против правила Марковникова. Исключения из правила Марковникова: 1) Если в молекуле присутствует заместитель, который оттягивает на себя электронную плотность двойной связи. 2) Если в реакционной системе присутствуют свободные радикалы или источники свободных радикалов, то реакция присоединения полярных молекул вида НХ к двойной связи протекает по радикальному механизму против правила Марковникова. РАДИКАЛЬНЫЕ РЕАКЦИИРАДИКАЛЬНЫЕ РЕАКЦИИ, осуществляются с участием радикального центра своб. радикалов.
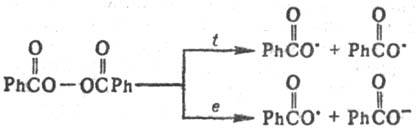
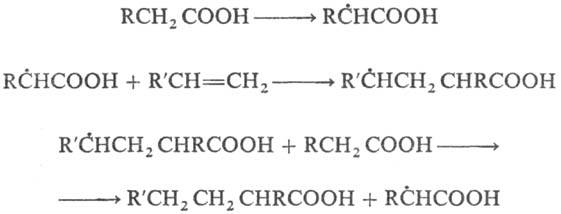
Эта р-ция м. б. индуцирована нагреванием, облучением, действием восстановителей или др. путями. Радикалы обладают разл. реакц. способностью, зависящей от их природы, типа р-ций, полярного и стерич. факторов, эффекта р-рителя. Реакции между свободными радикалами. Осуществляются при взаимод. двух одинаковых или разл. радикалов с образованием новой хим. связи (рекомбинация). Р-ция обычно диффузионно контролируемая; Е от 0 до 5 кДж/моль. Происходит, напр., при дегидродимеризации орг. соедине-ний под действием пероксидов или др. окислителей, напр.:
При близком расположении двух своб. радикалов в «клетке» р-рителя (напр., генерируемых при термораспаде пероксидов или диазосоединений) р-ция осуществляется с высокой селективностью (см. Клетки эффект). Влияние этого эффекта уменьшается с увеличением т-ры и понижением вязкости р-рителя. При взаимод. двух радикалов возможно также диспропор-ционирование- перенос атома Н (реже-атома галогена) от одного радикала к другому, напр.:
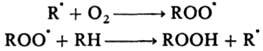
Диспропорционирование, как правило, более медленный процесс, чем рекомбинация. Обе р-ции экзотермичны и нередко идут одновременно. Реакции свободных радикалов с молекулами. Характерны для таких практически важных процессов, как хлорирование, бромирование, сульфохлорированис, автоокисление, полимеризация и др., протекающих по цепному механизму (см. Цепные реакции). Их константы скорости на неск. порядков ниже, чем для рекомбинации; Е = 20-60 кДж/моль. Так, р-ция автоокисления осуществляется в результате многократно повторяющихся р-ций по схеме:
Механизм р-ции замещения радикалами алкильных, тиильных, ацилоксильных, алкоксильных и нек-рых др. групп включает разрыв связи в исходной молекуле и образование новой связи с участием радикала, напр.:
По аналогии с нуклеоф. р-циями замещения такой механизм наз. механизмом S R 2. Стереохимия р-ции зависит от характера субстрата. Обычно образующийся радикал с неспаренным электроном у хирального атома С имеет плоскую или близкую к плоской конфигурацию, что приводит к рацемизации. В циклич. системах инверсия радикального центра затруднена, особенно в случае малых циклов, напр.:
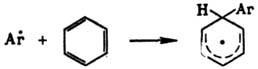
Р-ции радикального замещения в ароматич. ядре обычно не являются цепными и осуществляются через стадию образования циклогексадиенильных радикалов:
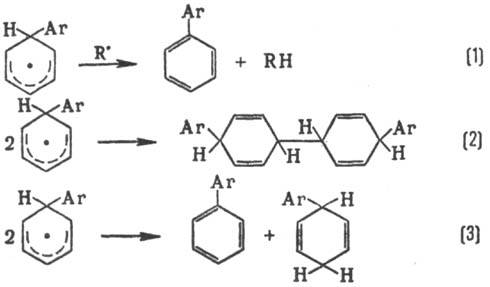
Превращение в конечный продукт происходит в результате отрыва атома Н (р-ция 1); побочные процессы-рекомбинация (2) и диспропорционирование (3):
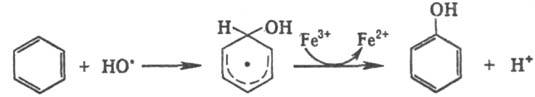
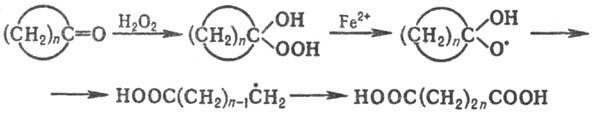
Электронедонорные и электроноакцепторные заместители активируют ароматич. ядро. В р-циях образуются о, м, и n-изомеры с преобладанием о-изомера. Гидроксильные радикалы, к-рые генерируются реактивом Фентона (Н 2 О 2 +Fe 2+ ), способны атаковать неактивир. ароматич. ядро. При этом образуется радикал, к-рый диме-ризуется или в присут. Fe 3+ превращ. в фенол:
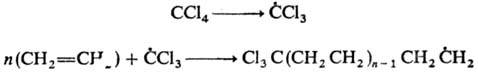
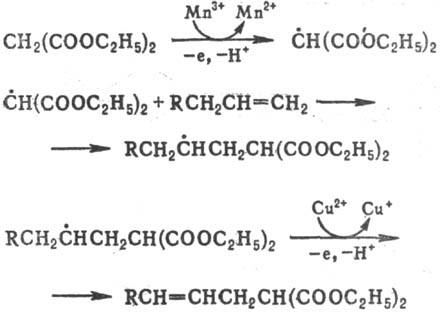
Среди р-ций радикального замещения в ароматич. ядро практич. значение имеет алкилирование протонир. гетеро-ароматич. соединений с атомом N в кольце. В пиридинах и хинолинах замещение происходит у атомов С в положениях 2 и 4. Свободнорадикальное присоединение по связи С=С-цепной процесс с короткими кинетич. цепями. Инициируется пероксидами, ионами переходных металлов и УФ облучением. Р-ция нестереоселективна для алкенов, высокостерео-селективна (транс-присоединение) для циклоалкенов; Е обычно не превышает 40 кДж/моль. К 1-алкенам радикал обычно присоединяется по а-атому С, напр.:
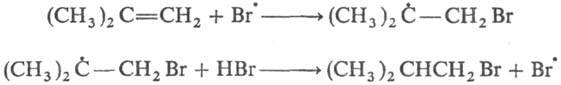
Свободнорадикальное присоединение НВr к несимметричным олефинам идет против правила Марковникова. Это объясняется тем, что в случае атаки такого олефина р-ция осуществляется по пути образования более стабильного радикала (увеличение числа алкильных заместителей при радикальном центре увеличивает стабильность радикала), поболее доступному атому С и па месту наиб. электронной плотности в молекуле, напр.:
Свободнорадикальное присоединение по связи С=С широко используется в органическом синтезе, в т.ч. в промышленности.
По аналогичному механизму осуществляется радикальная полимеризация непредельных соединений.
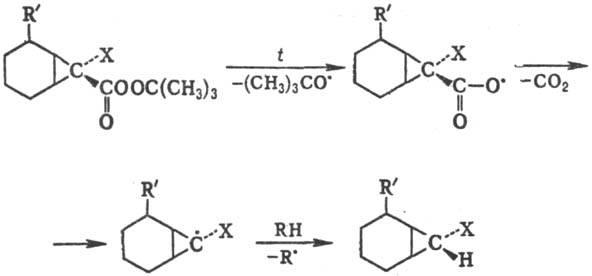
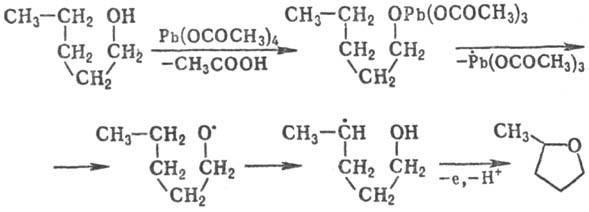
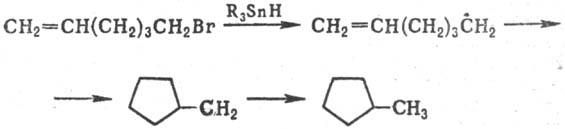
Фрагментацию циклоалкоксильных радикалов, генерируемых из циклоалканолов или циклоалканонов, используют в синтезе алифатич. бифункцион. соединений по схеме:
Фрагментация промежуточно образующихся алкильных радикалов происходит при получении этилена путем пиролиза нефтяных углеводородов.
Иногда наблюдается наряду с 1,5- также и 1,6-миграция атомов Н, значительно реже-1,3- и 1,4-миграции. Известны примеры р-ций С-центрированных радикалов с 1,4-миграцией арилов или группы CN, с 1,2-миграцией атомов С1, Вr или арильных, ацетоксилъных, ацильных и винильных группировок, напр.:
Известно также внутримол. присоединение углерод- или кислород центрированных радикалов к кратным связям или к ароматич. ядру. Таким путем легко образуются 5- и 6-членные циклы, напр.:
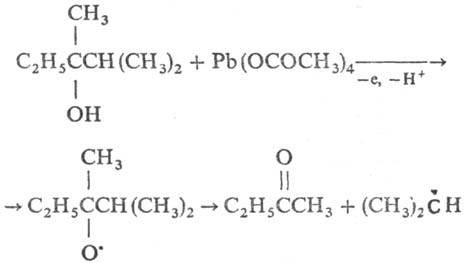
Окисление и восстановление свободных радикалов. Наиб. известно одноэлектронное окисление С-центрированных радикалов солями Сu(II), Co(III), Mn(III), Fe(III), Pb(IV), Се (IV). Р-ция осуществляется с высокими скоростями с переносом лиганда (С1, Вг, CN и др.), напр.:
При окислении ацетатом или сульфатом Сu(II) р-ция сопровождается депротонированием, что приводит к образованию двойной связи; р-ция используется в синтезе непредельных соед. с функц. группами, напр.:
Восстановление-типичная р-ция феноксильных и нйтро-ксильных радикалов, напр.:
Относительно легко восстанавливаются по механизму переноса электрона С-центрированные радикалы с электро-ноакцепторными заместителями при радикальном центре, напр.: РАДИКАЛЬНЫЕ РЕАКЦИИосуществляются с участием радикального центра своб. радикалов.
Эта р-ция м. б. индуцирована нагреванием, облучением, действием восстановителей или др. путями. Радикалы обладают разл. реакц. способностью, зависящей от их природы, типа р-ций, полярного и стерич. факторов, эффекта р-рителя. Реакции между свободными радикалами. Осуществляются при взаимод. двух одинаковых или разл. радикалов с образованием новой хим. связи (рекомбинация). Р-ция обычно диффузионно контролируемая; Еот 0 до 5 кДж/моль. Происходит, напр., при дегидродимеризации орг. соедине-ний под действием пероксидов или др. окислителей, напр.:
При близком расположении двух своб. радикалов в «клетке» р-рителя (напр., генерируемых при термораспаде пероксидов или диазосоединений) р-ция осуществляется с высокой селективностью (см. Клетки эффект).Влияние этого эффекта уменьшается с увеличением т-ры и понижением вязкости р-рителя. При взаимод. двух радикалов возможно также диспропор-ционирование- перенос атома Н (реже-атома галогена) от одного радикала к другому, напр.:
Диспропорционирование, как правило, более медленный процесс, чем рекомбинация. Обе р-ции экзотермичны и нередко идут одновременно. Реакции свободных радикалов с молекулами. Характерны для таких практически важных процессов, как хлорирование, бромирование, сульфохлорированис, автоокисление, полимеризация и др., протекающих по цепному механизму (см. Цепные реакции). Их константы скорости на неск. порядков ниже, чем для рекомбинации; Е= 20-60 кДж/моль. Так, р-ция автоокисления осуществляется в результате многократно повторяющихся р-ций по схеме:
Механизм р-ции замещения радикалами алкильных, тиильных, ацилоксильных, алкоксильных и нек-рых др. групп включает разрыв связи в исходной молекуле и образование новой связи с участием радикала, напр.:
По аналогии с нуклеоф. р-циями замещения такой механизм наз. механизмом R 2. Стереохимия р-ции зависит от характера субстрата. Обычно образующийся радикал с неспаренным электроном у хирального атома С имеет плоскую или близкую к плоской конфигурацию, что приводит к рацемизации. В циклич. системах инверсия радикального центра затруднена, особенно в случае малых циклов, напр.:
Р-ции радикального замещения в ароматич. ядре обычно не являются цепными и осуществляются через стадию образования циклогексадиенильных радикалов:
Превращение в конечный продукт происходит в результате отрыва атома Н (р-ция 1); побочные процессы-рекомбинация (2) и диспропорционирование (3):
Электронедонорные и электроноакцепторные заместители активируют ароматич. ядро. В р-циях образуются о, м, и n-изомеры с преобладанием о-изомера. Гидроксильные радикалы, к-рые генерируются реактивом Фентона (Н 2 О 2 +Fe 2+ ), способны атаковать неактивир. ароматич. ядро. При этом образуется радикал, к-рый диме-ризуется или в присут. Fe 3+ превращ. в фенол:
Среди р-ций радикального замещения в ароматич. ядро практич. значение имеет алкилирование протонир. гетеро-ароматич. соединений с атомом N в кольце. В пиридинах и хинолинах замещение происходит у атомов С в положениях 2 и 4. К 1-алкенам радикал обычно присоединяется по а-атому С, напр.:
Свободнорадикальное присоединение НВr к несимметричным олефинам идет против правила Марковникова. Это объясняется тем, что в случае атаки такого олефина р-ция осуществляется по пути образования более стабильного радикала (увеличение числа алкильных заместителей при радикальном центре увеличивает стабильность радикала), поболее доступному атому С и па месту наиб. электронной плотности в молекуле, напр.:
Свободнорадикальное присоединение по связи С=С широко используется в органическом синтезе, в т. ч. в промышленности.
По аналогичному механизму осуществляется радикальная полимеризация непредельных соединений.
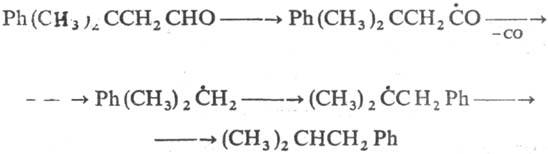
Т. к. в р-циях этого типа гемолизу подвергается связь, обычно расположенная в b-положении по отношению к неспаренному электрону, то такой процесс иногда наз. b-рас-щеплением или b-распадом. Ацильные радикалы, генерируемые из альдегидов, легко фрагментируют при т-ре выше 100°С на алкильные радикалы и СО. Фрагментацию циклоалкоксильных радикалов, генерируемых из циклоалканолов или циклоалканонов, используют в синтезе алифатич. бифункцион. соединений по схеме:
Фрагментация промежуточно образующихся алкильных радикалов происходит при получении этилена путем пиролиза нефтяных углеводородов.
Иногда наблюдается наряду с 1,5- также и 1,6-миграция атомов Н, значительно реже-1,3- и 1,4-миграции. Известны примеры р-ций С-центрированных радикалов с 1,4-миграцией арилов или группы CN, с 1,2-миграцией атомов С1, Вr или арильных, ацетоксилъных, ацильных и винильных группировок, напр.:
Известно также внутримол. присоединение углерод- или кислород центрированных радикалов к кратным связям или к ароматич. ядру. Таким путем легко образуются 5- и 6-членные циклы, напр.:
Окисление и восстановление свободных радикалов. Наиб. известно одноэлектронное окисление С-центрированных радикалов солями Сu(II), Co(III), Mn(III), Fe(III), Pb(IV), Се (IV). Р-ция осуществляется с высокими скоростями с переносом лиганда (С1, Вг, CN и др.), напр.:
При окислении ацетатом или сульфатом Сu(II) р-ция сопровождается депротонированием, что приводит к образованию двойной связи; р-ция используется в синтезе непредельных соед. с функц. группами, напр.:
Восстановление-типичная р-ция феноксильных и нйтро-ксильных радикалов, напр.:
Относительно легко восстанавливаются по механизму переноса электрона С-центрированные радикалы с электро-ноакцепторными заместителями при радикальном центре, напр.:
См. также Радикалы свободные. Лит.: НонхибелД., Уолтон Дж., Химия свободных радикалов, пер. с англ., М., 1977; Розанцев Э. Г., Шолле В. Д., Органическая химия свободных радикалов, М., 1979; Девис Д., Перрет М., Свободные радикалы в органическом синтезе, пер. с англ., М., 1980; Нонхибел Д., Теддер Дж., Уолтон Дж., Радикалы, пер. с англ., М., 1982; Free radicals, ed. by J.K. Kochi, v. 1-4, N.Y., 1973-80; Selectivity and synthetic applications of radical reactions. Tetrahedrpn symposia-in-print, «Tetrahedron», 1985, v. 41, № 19; Giese В., Radical in organic synthesis. Formation of carbon bonds, Oxf., 1986; Curran D.P., «Synthesis», 1988, № 6, p. 417-39; там же, 1988, № 7, p. 489-513. ПолезноеСмотреть что такое «РАДИКАЛЬНЫЕ РЕАКЦИИ» в других словарях:РАДИКАЛЬНЫЕ РЕАКЦИИ — РАДИКАЛЬНЫЕ РЕАКЦИИ, химические реакции с участием свободных радикалов (см. РАДИКАЛЫ СВОБОДНЫЕ), обладающих высокой реакционной способностью. Характеризуются малыми энергиями активации. Наиболее изучены рекомбинация (см. РЕКОМБИНАЦИЯ в физике) и… … Энциклопедический словарь радикальные реакции — radikalinė reakcija statusas T sritis chemija apibrėžtis Reakcija, kurios metu susidarančios tarpinės dalelės yra laisvieji radikalai. atitikmenys: angl. free radical reactions; radical reactions rus. радикальные реакции; свободно радикальные… … Chemijos terminų aiškinamasis žodynas свободно-радикальные реакции — radikalinė reakcija statusas T sritis chemija apibrėžtis Reakcija, kurios metu susidarančios tarpinės dalelės yra laisvieji radikalai. atitikmenys: angl. free radical reactions; radical reactions rus. радикальные реакции; свободно радикальные… … Chemijos terminų aiškinamasis žodynas РЕАКЦИИ ХИМИЧЕСКИЕ — (от лат. re приставка, означающая обратное действие, и actio действие), превращения одних в в (исходных соед.) в другие (продукты р ции) при неизменяемости ядер атомов (в отличие от ядерных реакций). Исходные соединения в Р. х. иногда наз.… … Химическая энциклопедия Реакции замещения — (англ. substitution reaction) химические реакции, в которых одни функциональные группы, входящие в состав химического соединения, меняются на другие группы. Реакции замещения обозначают английской буквой «S». Общий вид реакций… … Википедия Реакции нуклеофильного замещения — (англ. nucleophilic substitution reaction) реакции замещения, в которых атаку осуществляет нуклеофил реагент, несущий неподеленную электронную пару.[1] Уходящая группа в реакциях нуклеофильного замещения называется нуклеофуг. Все … Википедия Реакции электрофильного замещения — (англ. substitution electrophilic reaction) реакции замещения, в которых атаку осуществляет электрофил частица, заряженная положительно или имеющая дефицит электронов. При образовании новой связи уходящая частица электрофуг … Википедия Реакции нуклеофильного присоединения — (англ. addition nucleophilic reaction) реакции присоединения, в которых атаку на начальной стадии осуществляет нуклеофил частица, заряженная отрицательно или имеющая свободную электронную пару. На конечной стадии образующийся… … Википедия Реакции присоединения — (англ. addition reaction) в органической химии так называются химические реакции, в которых одни химические соединения присоединяются к кратным (двойным или тройным) связям другого химического соединения. Присоединение может… … Википедия Реакции электрофильного присоединения — (англ. addition electrophilic reaction) реакции присоединения, в которых атаку на начальной стадии осуществляет электрофил частица, заряженная положительно или имеющая дефицит электронов. На конечной стадии образующийся… … Википедия |