МР-спектроскопия
Магнитно-резонансная спектроскопия (МРС) — метод позволяющий определить биохимические изменения тканей при различных заболеваниях по концентрации определённых метаболитов. МР-спектры отражают относительное содержание биологически активных веществ в определённом участке ткани, что характеризует процессы метаболизма. Нарушения метаболизма возникают, как правило, до клинических проявлений заболевания, поэтому на основе данных МР-спектроскопии можно диагностировать заболевания на более ранних этапах развития.
МРС впервые использовали при исследовании эритроцитов в 1973 году Мун и Ричардс, а в 1974 году при помощи МРС Хаулт исследовал бедренную мышцу мыши.
Основные ядра для in vivo-МР-спектроскопии – это протоны (H), 31-фосфор ( 31 P) и 13-углерод ( 13 С). Из всех магнитных ядер протоны дают наибольший сигнал МР. Атомы водорода входят в состав всех биологических и медицинских препаратов, интермедиатов и продуктов. Поэтому протоны – удачный зонд для мониторинга метаболизма. Однако, протонная спектроскопия связана с большими техническими трудностями. Сигналы воды и липидов чаще всего не очень интересны с медицинской точки зрения. Концентрация протонов воды в тканях составляет 35 M, в то время как концентрация интересующих нас метаболитов находится в диапазоне ниже 10 мМ, т.е. она минимум в 3000 раз ниже. Поэтому маленькие сигналы метаболитов маскируются гигантскими по сравнению с ними сигналами воды и липидов. Только такие технически сложные методы, как селективное возбуждение, селективное насыщение, подавление за счет релаксации и многоквантовая спектроскопия, позволяют подавлять эти сигналы до уровня сигналов метаболитов и обнаружить сигналы таких метаболитов, как лактат (Lac), холин (Ch), креатин (Cr), N-ацетил-аспартат (NAA), фосфохолин (РСНО), д-инозитол и др. 1 Н in vivo спектроскопия применяется прежде всего для изучения демилиенизирующих процессов белого вещества мозга и дифференциации
Патологические сдвиги
Глиома
По мере повышения уровня NAA и креатина снижаются, а холин, липиды и лактат увеличиваются. В условиях глиомы холин будет повышаться за пределами усиления контраста в соответствии с клеточной инфильтрацией.
Не-глиальные опухоли
Незначительные изменения пика NAA.
Лейкодистрофии
Прогрессирующая мультифокальная лейкоэнцефалопатия повышение Мио-инозитол. Болезнь Канавана повышение NAA.
Митохондриальные заболевания
Синдром Лея: повышение пика холина, снижение NAA и реже повышение пика лактата.
Инфекция
Пик NAA отсутствует при всех патологических процессах, разрушающих ткань головного мозга. При абсцессе пик лактата, аланина, ацетата повышен. Пик холина низкий или отсутствует при токсоплазмозе, а при лимфоме повышен, данный показатель используют для отличия одного патологического процесса от другого.
Ишемия и инфаркт
Пик лактата будет повышаться, как только клетки головного мозга переходят на анаэробный метаболизм. Пик липидов и всех остальных пиков будет снижаться.
Фосфорная спектроскопия
Углеродная спектроскопия
В отличие от Т Н и 31 Р, магнитный изотоп углерода 13 С не является самым распространенным изотопом этого ядра. Его абсолютная чувствительность примерно в 5000 раз ниже, чем для H, однако, современные методы МРС позволяют наблюдать и его сигнал с достаточной чувствительностью. 13 С присутствует во всех биологических препаратах, и соответствующие сигналы имеют широкий интервал химических сдвигов, т.е. частоты химически неэквивалентных ядер настолько отличаются друг от друга, что вероятность их наложения невелика. Одним из преимуществ МРС 13 С-спектроскопии является возможность проведения исследований с мечеными веществами. Давая животному или пациенту вещества, обогащенные 13 С, мы можем следить за большими и четко различимыми сигналами этих меченых веществ и пытаться выяснить, как они метаболируют в организме. Поскольку каждому положению атома углерода в молекуле отвечает вполне характерный сигнал, эксперимент с метками можно использовать не просто для доказательства того, какие молекулы взаимодействуют с меткой, но и для достоверного указания точной внутримолекулярной позиции такого взаимодействия. Такая информация предельно полезна при изучении биохимических путей превращения одних молекул в другие в организме. 13 С МР-спектроскопия может также обнаруживать сигналы от сахаров, липидов и гликогена в печени и в мышцах. Можно получить информацию об углеродном балансе энергетического метаболизма, которая дополняет информацию, приносимую об этом метаболизме с помощью МР 31 Р-спектроскопии. Многообещающей областью применения U C МР-спектроскопии является анализ таких физиологических жидкостей, как кровь и моча. Эта процедура может осуществляться вполне рутинным образом с помощью аналитических МР- спектрометров с очень сильными магнитными полями.
СПЕКТРОСКОПИЯ
СПЕКТРОСКОПИЯ — раздел физики, изучающий качественный и количественный состав спектров электромагнитного излучения. Методами С. исследуют уровни энергии атомов, молекул и образованных ими макросистем, а также возможные переходы между уровнями энергии (см. Молекула), что дает необходимую информацию о строении и свойствах вещества (его качественном и количественном составе, структуре и т. д.). Одной из областей применения С. является спектральный анализ (см.), широко используемый в медицине.
Существенно расширились возможности спектроскопической техники в связи с созданием лазеров (см. Лазер). Разработаны методы С. резонансного комбинационного рассеяния и оптической доплеровской С. В частности, с помощью метода оптической.доплеровской С. возможно непрерывное наблюдение за перемещением молекул, макромолекул, цитоплазматических структур в живых клетках, а также изучение действия лекарственных и других веществ на клетку и т. д.
С. проводится с помощью разнообразных спектральных приборов. Их классифицируют по различным признакам: способу диспергирования (разложения) света, методу регистрации спектра, рабочей области (диапазону) спектра и др.
По способу диспергирования электромагнитного излучения на монохроматические составляющие и их последующей регистрации различают призменные спектральные приборы (основаны на зависимости показателя преломления материала призмы от длины волны) и дифракционные спектральные приборы, использующие зависимость угла дифракции света от длины волны (см. Оптика).
По методу регистрации спектральные приборы делят на спектроскопы (регистрация спектра осуществляется визуально), спектрографы (регистрация спектров ведется на фотоэмульсии), спектрометры (регистрируют абсолютные интенсивности спектров) и спектрофотометры (регистрируют спектры поглощения в процентах пропускания или единицах оптической плотности), кванто-метры, или полихроматоры,— приборы с фотоэлектрической регистрацией, используемые для проведения быстрого эмиссионного анализа соединений.
В зависимости от диапазона измерений спектральные приборы делят на спектрометры и спектрографы для коротковолновой области УФ (диапазон 10 — 200 нм); спектрографы, спектрометры и спектрофотометры для У Ф и видимой части спектра (200—760 нм); спеьгтрометры и спектрофотометры для ближней инфракрасной (2—50 мкм) и дальней инфракрасной области спектра (50—1000 мкм).
Широко используется ряд своеобразных гибридных спектроскопических методов, таких, в частности, как фотоакустическая С., при к-рой образец облучают светом (в ультрафиолетовой, видимой или ближней инфракрасной областях), модулированным звуковой частотой. В процессе безызлучательного перехода системы в основное состояние возникают колебания давления в газовой среде, окружающей образец, улавливаемые микрофоном как акустические сигналы.
С.— универсальный метод качественного и количественного анализа состава вещества, изучения его строения, свойств и других параметров. Методы атомной С. позволяют определять элементы, входящие в состав вещества, в частности содержание тех или иных ионов в сыворотке, моче и других биол. жидкостях (эмиссионный и атомно-абсорбционный спектральный анализ). Молекулярная С. используется с целью идентификации веществ, количественного анализа (определения содержания в пробе ферментов, витаминов, гормонов, белков, нуклеиновых к-т, углеводов. липидов, ионов и пр.), изучения кинетики хим. и биохим. реакций.
С помощью методов ядерного магнитного резонанса и инфракрасной С. проводится определение строения органических молекул, их пространственной структуры, механизмов и кинетики биохим. реакций. Методом электронного парамагнитного резонанса выявляют промежуточные свободно-радикальные продукты, изучают механизм повреждения биол. тканей (см. Радикалы свободные) и т. д. С помощью гамма-резонансной С. изучают структурные превращения железосодержащих белков, в частности при заболевании крови человека. Метод фотоакустической С. используют для изучения сильно рассеивающих свет образцов, в т. ч. интактного биол. материала (клеточных органелл, клеток, тканей и органов).
Библиография: Грибов Л. А. Введение в молекулярную спектроскопию, М., 1976; Зайдель А. Н., Островская Г. В. и Островский Ю. И. Техника и практика спектроскопии, М., 1976; Ландсберг Г. С. Оптика. М., 1976; Славин У. Атомно-абсорбционная спектроскопия, пер. с англ., Л., 1975, библиогр.; Фрайфелдер Д. Физическая биохимия, пер. с англ., с. 383, М., 1980.
Что такое спектроскопия в медицине
Психическое здоровье детей определяет будущее нации и является приоритетной задачей социальной политики. В последние годы среди подростков произошло выраженное ухудшение состояния здоровья. По официальным данным Минздрава РФ, число здоровых подростков едва достигает 10 %. Каждый четвертый подросток имеет пограничные нервно-психические отклонения. Проблема терапии психосоматических расстройств детей является наиболее острой, так как именно в этом возрасте, в связи с ранним онтогенезом и довольно частым дизонтогенезом различного происхождения, соматизация возникает чаще, чем в зрелом возрасте [1].
Глобальный подход к реализации идеи интегрированного обучения может служить объяснением наблюдающейся в последние годы тенденции усиления неоднородности состава учащихся общеобразовательной школы по уровню психического развития. Как показывают исследования, среди неуспевающих учащихся есть школьники с педагогической запущенностью, задержкой психического развития, неярко выраженными сенсорными, интеллектуальными, речевыми нарушениями, причинами которых являются остаточные поражения центральной нервной системы, минимальными мозговыми дисфункциями. Считается, что дети с задержкой психического развития (ЗПР) составляют примерно 50 % неуспевающих учащихся [2]. Диагностика ЗПР на ранних стадиях крайне сложна. В настоящее время она осуществляется преимущественно в медико-педагогическом плане. Однако, нарушения метаболизма и связанные с этим биохимические изменения в исследуемой системе наступают на молекулярном уровне задолго до клинических проявлений заболевания, что находит свое отражение в ИК – спектре биологических жидкостей [3, 4].
Цель работы. Установить влияние патологического состояния «задержка психосоматического развития» на ИК-спектр сыворотки плазмы крови подростков.
Материалы и методы исследования
ИК-спектрометрию сыворотки крови проводили у 30 подростков с ЗПР в возрасте от 12 до 15 лет (средний возраст 14,0±0,6 лет), из них 17 мальчиков, 13 девочек (группа № 1). Пациенты отбирались до лечения с четко выраженными клиническими симптомами. Диагноз «Задержка психического развития» обследованных подростков был установлен при прохождении ими медико-педагогической психологической комиссии. Для данных больных проведена терапия препаратом «Кортексин», курс лечения составлял 10 внутримышечных инъекций через 2 дня по 10 мг. Для оценки эффективности лечения, наряду с общепринятыми клиническим обследованием, изучали изменения спектральных характеристик сыворотки крови. В контрольную группу (группа № 2) вошли 30 подростков с нормативным психическим развитием аналогичного возраста (13,8±0,8 лет) из них 14 мальчиков, 16 девочек. Критериями исключения детей из обследования стало наличие острой инфекционной патологии и обострение сопутствующих хронических заболеваний.
Забор крови проводился утром натощак из кубитальной вены и совмещался с общим клиническим и биохимическим анализом крови. После отделения сыворотки плазмы крови (объемом 0,1 мл) ее равномерно распределяли пипеткой по подложке из полиэстерола и медленно высушивали в ламинарном потоке воздуха при температуре 250С. Полученную пленку переносили на кристалл приставки НПВО ИК- спектрометра с Фурье преобразованием Nicolet IS10 и проводили снятие спектра. Расчеты осуществляли в программной среде OMNIC.
Результаты исследования и их обсуждение
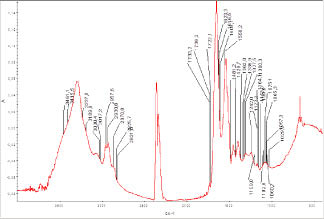
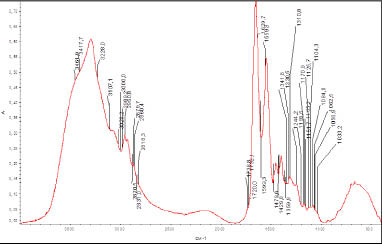
В ИК-спектрах (рис. 1, 2) сыворотки плазмы крови подростков с патологией и без нее установлено, что у детей первой группы, относительно здоровых выявлен ряд отличий. В диапазоне длины волны 3462см-1, относящейся к симметричным валентным колебаниям групп –OH, –NH, значительно снижена высота пика, что говорит о меньшем содержании веществ с данными функциональными группами. Обнаружено уменьшение высоты пика 3417 см-1, характеризующего симметричные валентные колебания транс –NH группы, а так же ее смещение на 3412см-1. Валентные симметричны колебания связанных транс –NH групп смещены от своего нормального положения (3228 см-1) к 3227 см-1, при этом происходит уменьшение высоты пика. Поглощение в области 3207 см-1, смещенное к 3190 см-1 и менее интенсивное, может быть приписано симметричным валентным колебаниям связанных групп –OH, –NH. Деформационные колебания –NH3+, определяемые у здоровых детей при длине волны 1311см-1, значительно ослаблены и смещены к 1300 см-1 (табл.1) для детей с патологией.
В области 3600-3450 см-1 обнаружены пики, которые можно отнести к валентным колебаниям –OH групп, что говорит о наличии воды в составе гидратных оболочек биологически активных веществ крови. Область деформационных колебаний воды сыворотки плазмы (1645 см-1) исследуемой группы достоверно ниже у исследуемой группы, по сравнению с контрольной [5].
Рис. 1. ИК-спектрограмма сыворотки плазмы крови подростков с задержкой психического развития
Рис. 2. ИК-спектрограмма сыворотки плазмы крови здоровых подростков
При помощи программной среды Omnic нами была проведена оценка различий в ИК-спектрах сыворотки плазмы крови исследуемых групп исходя из высоты пиков и площади полос поглощения основных характеристических групп. Результаты представлены в табл. 1, 2.
Высоты пиков поглощения основных характеристических групп сыворотки плазмы крови
Магнитно-резонансная спектроскопия

Суть исследовательской методики
Современные исследовательские клиники проводят магнитно-резонансную спектроскопию с применением специализированного оборудования. Такой метод исследования определяет биохимические изменения, которые вызываются различными патологическими состояниями, в разных участках человеческого организма.
Протонная магнитно-резонансная спектроскопия основывается на изменениях резонансной частоты протонов, из которых состоят всевозможные химические соединения. Такой процесс в медицине принято называть химическим сдвигом, что определяет различия частот пиков спектра.
Единицей измерения химического сдвига принято считать миллионную долю (ррт). На сегодняшний день протонная магнитно-резонансная спектроскопия подразделяется на ту, что проводится по одновоксельной методике, и мультивоксельную, которая может одномоментно определять спектры из нескольких участков головного мозга.
В современной медицине применяется еще одна разновидность спектроскопии – мультиядерная, учитывающая магнитно-резонансные сигналы фосфорных, углеродных и некоторых иных ядер.
При одновоксельной магнитно-резонансной спектроскопии анализу подлежит лишь один воксел или участок мозга человека. При анализе состава частот спектра выбранного воксела специалисты получают определенное метаболитное распределение химического сдвига в миллионных долях. При этом по соотношению в спектре метаболитных пиков, уменьшению или увеличению их высот можно неинвазивным путем оценить протекающие в тканях биохимические процессы.
Мультивоксельная спектроскопия предоставляет спектральные значения сразу нескольких необходимых при исследовании вокселов, которые можно сравнить для получения целостности картины исследуемого участка.
Данные мультивоксельной магнитно-резонансной спектроскопии позволяют строить карту среза по параметрам, где цветовыми маркерами обозначены концентрации необходимых метаболитов, а распределенность метаболитов в срезе визуализирована и предоставляет взвешенное по параметру химического сдвига изображение.

Наиболее частым спектром применения методики выступает анализ мышечной ткани, поскольку она не подлежит ни одному другому неинвазивному методу диагностики и может быть обследована только путем применения биопсии.
Области применения диагностики
Рассматриваемая диагностика позволяет расшифровывать процессы метаболизма тканей различных органов при помощи получаемых магнитно-резонансных спектров. Обменные процессы организма, в большинстве случаев, нарушаются гораздо раньше, чем пациент начинает ощущать какие-то симптомы того или иного заболевания.
Вот почему важно своевременно применять магнитно-резонансную спектроскопию, которая поможет выявить отклонения на ранних стадиях болезни и принять соответствующие меры по предотвращению ее прогрессирования. К тому же, данная методика для отдельных анатомических областей организма человека является единственной неинвазивной диагностической процедурой, которая известна на сегодняшний день.
Для диагностики энергетического показателя метаболического процесса сердечной мышцы без введения радиоактивных средств магнитно-резонансная спектроскопия является единственно возможным методом обследования.
При сочетании методики с результатами магнитно-резонансной томографии врач получает общую клиническую картину кардиологических параметров – размеров сердца, структуры миокарда и нарушений кровообращения в нем, функциональных расстройств. Также вышеназванная диагностика помогает контролировать ход лечения ишемической болезни сердца, различной гипертрофии, сердечной недостаточности.
При неврологических патологиях магнитно-резонансная спектроскопия позволяет уточнить диагноз, различая, например, рассеянный склероз и нейрооптикомиелит. При расстройствах психики важным является та особенность данной диагностики, которая помогает рассмотреть различные биохимические процессы в мозговых клетках.
Данная методика широко применима для оценки всевозможных новообразований в головном мозге. Несмотря на отсутствие гистологических данных о возникшем новообразовании, исследователи говорят об определенных соотношениях рассматриваемых в ходе диагностики показателей и возникновении пика лактата. Таким образом, большинство случаев магнитно-резонансной спектроскопии опухолевых тканей способно предоставить дифференциацию возникших новообразований по принципу злокачественности.
В клинических условиях при послеоперационных диагностиках данная методика свидетельствует об успешности проведенного хирургического вмешательства либо о продолжении роста рассматриваемой опухоли, ее рецидиве, лучевом некрозе.

Показательными являются в данном разрезе диагностированные случаи абсцессов, опирающиеся на диффузионно-взвешенные изображения.
Так, при отсутствующих пиках основных метаболитов при абсцессе отмечается возникновение пиков липид-лактатного комплекса и специфичных абсцессу пиков – например, продуктов анаэробного бактериального гликолиза и результатов протеолиза.
В медицинских источниках часто исследуется эффективность МР-спектроскопии при метаболических нарушениях и дегенеративных поражениях белого вещества мозга у детей, эпилепсии, черепно-мозговых травмах, ишемиях головного мозга и прочих заболеваниях.
Показания и противопоказания для МРС
Рассматриваемая диагностика аналогично магнитно-резонансной томографии основана на ядерно-магнитном резонансе, но ее результатом не выступают снимки.
Методика помогает рассматривать правильность распределения в тканях продуктов метаболических процессов, основываясь на их молекулярных особенностях.
Среди основных состояний и заболеваний, при которых пациентам показано прохождение магнитно-резонансной спектроскопии, выделяют эпилепсию, ишемическую болезнь, болезни Альцгеймера и Паркинсона, всевозможные воспалительные процессы, травмирование тканей, возникновение новообразований в головном мозге.
Поскольку метаболизм здоровых и пораженных тканей значительно отличается, проведение данного вида исследования помогает диагностировать и начать лечить проблему на самой ранней стадии, что чаще приводит к успешному результату.
Среди главных противопоказаний к процедуре специалисты называют искусственный водитель ритма. В случае наличия протезирования внутреннего уха либо искусственного сердечного клапана важно своевременно информировать об этом врача и предоставить ему подробное описание или аннотацию имеющегося протеза.
Также, поскольку исследование проводится в закрытом пространстве – продолговатой кабине, при наличии боязни таких пространств необходимо сообщить об этом специалисту, чтобы он мог прописать пациенту седативные (успокоительные) препараты.
Методика исследования, описанная выше, является многообещающей, поскольку при ее сочетании с другими обследованиями точность поставленного диагноза обычно достигает 90%. Иногда случаются неточности в связи с особенностью опухолевой ткани, которая может не сильно отличаться от нормальной по содержанию холина и степени зрелости.
В остальных случаях данное исследование очень информативно показывает специалистам, что происходит с обследуемым участком.
Больше свежей и актуальной информации о здоровье на нашем канале в Telegram. Подписывайтесь: https://t.me/foodandhealthru
Спектроскопия КР: новые возможности старого метода
Спектроскопия КР: новые возможности старого метода
Автор
Редактор
Статья на конкурс «био/мол/текст»: Спектроскопия комбинационного рассеяния света (КР) появилась более 80 лет назад и с тех пор широко используется в физике, химии и многих прикладных областях. Метод привлекателен тем, что на исследуемый образец воздействует только свет и ничего более, но при этом можно получать эксклюзивную информацию о свойствах объекта, которую нельзя получить другими методами. Однако минус КР для исследования живой клетки состоит в том, что получается сигнал со слишком низкой интенсивностью. Тем не менее за последние десятилетия появилось несколько усовершенствований, которые позволили значительно усиливать сигнал, что открыло широкие возможности для применения КР в исследованиях живых клеток и тканей. В обзоре будет рассказано о принципах данных подходов и об их применении для решения современных биофизических и биомедицинских задач.
Обратите внимание!
Эта работа опубликована в номинации «лучшая обзорная статья» конкурса «био/мол/текст»-2015.
Спонсором номинации «Лучшая статья о механизмах старения и долголетия» является фонд «Наука за продление жизни». Спонсором приза зрительских симпатий выступила фирма Helicon.
Спонсоры конкурса: Лаборатория биотехнологических исследований 3D Bioprinting Solutions и Студия научной графики, анимации и моделирования Visual Science.
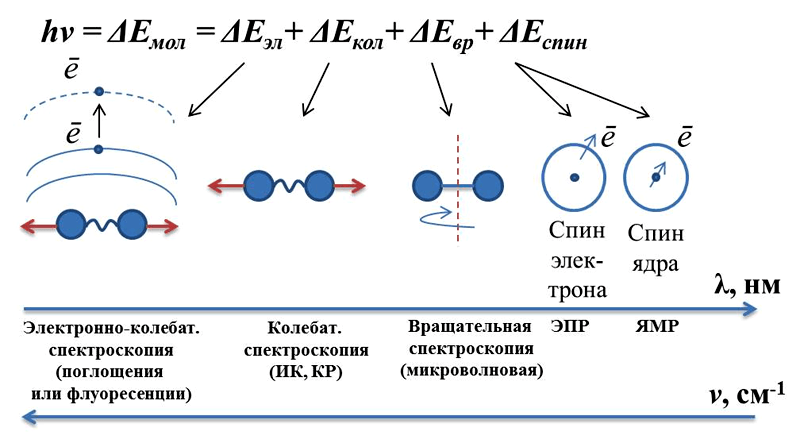
Если спросить, чем занимаются биофизики, то в большинстве случаев ответ будет — спектрами. А если попробовать уточнить, какими именно спектрами, то варианты ответа будут самыми разнообразными: и спектрами поглощения, и спектрами флуоресценции, инфракрасными, и ультрафиолетовыми, и спектрами электронного парамагнитного резонанса (ЭПР), и ядерного магнитного резонанса (ЯМР) [1], и спектрами комбинационного рассеяния (КР), и т.д. и т.п. Но в любом случае спектроскопия позволяет исследовать переходы между энергетическими уровнями молекул: электронными, колебательными или вращательными в зависимости от выбранного метода (рис. 1).
При этом выбор метода зависит от конкретной исследовательской задачи. Исторически в нашей группе биофизики клетки (кафедра биофизики биологического ф-та МГУ) изучают конформационные состояния различных биомолекул, используя для этого метод комбинационного рассеяния света (КР, Raman spectroscopy, RS). Итак, что это за метод, и какую информацию можно из него извлечь?
Рисунок 1. Изменение энергии молекулы (ΔЕ) при взаимодействии с квантом света (hν). Каждый спектроскопический метод работает в своем энергетическом диапазоне. Энергии переходов: Еэл — электронных, Екол — колебательных, Евр — вращательных, Еспин — изменения спина. На основе лекций Ф.Ф. Литвина.
Эффект комбинационного рассеяния света
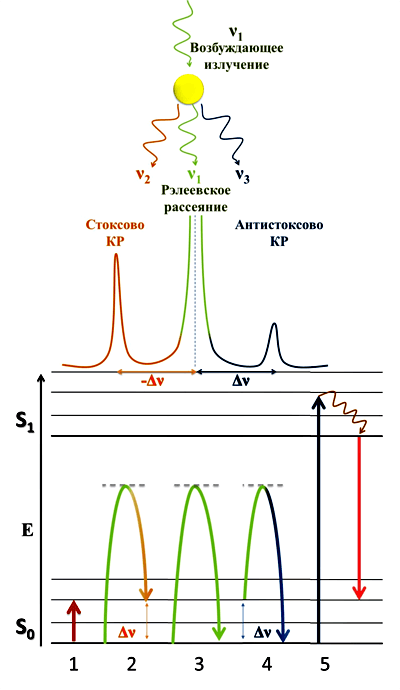
Явление КР основано на эффекте неупругого (рáмановского, или комбинационного*) рассеяния оптического излучения на молекулах вещества. При обычном (упругом, или рэлеевском) рассеянии свет после взаимодействия с веществом обладает той же энергией, что и возбуждающий луч, следовательно, и частота (и длина волны) излучения не меняется. А при неупругом рассеянии в результате взаимодействия света с молекулами вещества частота излучения меняется. В основном свет рассеивается на молекулах вещества без изменения частоты, но небольшая часть фотонов все же меняет свою частоту, что выражается в появлении дополнительных линий (линий КР) на спектре рассеяния. Схематично явление КР изображено на рис. 2.
* — Да-да, рамановское и комбинационное рассеяние — это одно и то же. Впервые появление новых линий в спектре рассеянного света на кристаллах кварца наблюдали в 1928 году советские учёные Г. С. Ландсберг и Л. И. Мандельштам, которые назвали увиденное явление комбинационным рассеянием света (КР). На неделю позже советских физиков комбинационное рассеяние наблюдали индийские учёные Ч. В. Раман и К. С. Кришнан на жидкостях, используя солнечные лучи в качестве источника света. Впоследствии за открытие эффекта неупругого рассеяния света только Раман был удостоен Нобелевской премии в 1930 году, а данный оптический эффект стал носить его имя (эффект Рамана, англ. Raman effect). Однако в русскоязычной литературе придерживаются названия, данного Ландсбергом и Мандельштамом, т.е. КР. Название «комбинационное» рассеяние означает, что спектр рассеяния представляет собой комбинацию частот возбуждающего света и собственных колебаний молекулы [2]. — Авт.
Рисунок 2. Рассеяние света на молекуле (жёлтый круг), устройство спектров КР* и схема переходов между колебательными подуровнями и электронными уровнями молекулы. S0 и S1 — основной и первый возбужденный электронные уровни со структурой колебательных подуровней. Серой пунктирной линией обозначен виртуальный подуровень (в случае, если энергии кванта не хватает для перехода на существующий подуровень). 1 — Поглощение инфракрасного (ИК)-кванта приводит к переходу молекулы на новый колебательный подуровень**. 2 — Стоксово КР наблюдается в случае, если молекула находится в невозбужденном состоянии и при взаимодействии со светом переходит на более высокий колебательный подуровень. Энергия рассеянного света при этом меньше энергии возбуждающего света (зеленый → оранжевый). 3 — Рэлевское рассеяние, не приводящее к изменению энергии (и соответственно, длины волны) возбуждающего света. 4 — Антистоксово КР наблюдается в случае, если молекула находится в возбужденном состоянии и при взаимодействии со светом переходит на нижний колебательный подуровень. В этом случае энергия рассеянного света будет больше энергии возбуждающего света (зеленый → синий). Происходит гораздо реже стоксового из-за разности в заселённости уровней. 5 — Флуоресценция: квант света вызывает электронно-колебательный переход, после чего наблюдается релаксация (бордовая фигурная стрелка) и испускание света с меньшей энергией (синий → красный). Рисунок из [3].
* — Спектры КР представляют как зависимость интенсивности сигнала от частотного сдвига, Δν [см −1 ], а не длины волны. В этом случае спектры не зависят от выбора лазера и их можно сравнивать.
** — Стоит заметить, что колебательные состояния, исследуемые в КР спектроскопии, являются такими же, что и в ИК спектроскопии. Однако колебания, которые сильно проявляются в ИК спектре обычно слабо проявляются в КР спектре и наоборот. Таким образом, КР и ИК спектроскопия — это взаимно дополняющие методы, хотя ИК спектроскопия — это по сути спектроскопия поглощения, а КР — рассеяния света.
Видео о том, как увидеть КР своими глазами
Какую информацию несёт спектр КР?
Под «взаимодействием» света с молекулой подразумевается энергетический обмен между фотонами и колебательными подуровнями энергии («колебаниями») молекулы. Это означает, что спектр КР несёт в себе информацию о колебаниях атомов в молекулах исследуемого вещества. Строго говоря, разность частот возбуждающего и рассеянного света (Δν) характеризует нормальные частоты колебаний молекулы в целом. Большинство пиков на спектре КР обусловлено колебаниями сразу нескольких химических связей в молекуле. Но некоторые пики описывают колебания совершенно определённых групп атомов. Например, положение максимумов пиков на спектре КР, характеризующих колебания одинарной С—С, двойной С=С и тройной C≡C связей, будет отличаться. Также на спектре хорошо различаются пики С=О, ароматических колец, тиолов и многих других групп атомов [2, 3]. С помощью таких ключевых колебаний можно определить, с чем мы имеем дело: с липидами, белками, ДНК, порфиринами или другими молекулами (рис. 3). И для каждой молекулы будет свой неповторимый спектр КР. Таким образом, спектр КР — это точный индивидуальный «отпечаток пальцев» молекулы. Поэтому метод чрезвычайно популярен среди химиков-аналитиков и физиков, а также применяется в археологии, экологии, геологии и даже в криминалистике. А вот биолога, как мы все понимаем, интересует не столько состав того, с чем он работает, сколько механизм самой работы.
Рисунок 3. Выявление различных веществ по ключевым пикам на спектре КР сложной смеси. Рисунок из [4] с изменениями.
КР в биологии
Первые биологические эксперименты с использованием метода КР провели еще в 1935-м году на аминокислотах [5]. Но, как известно, работы на изолированных молекулах не столь интересны, как на целых клетках. Давайте порассуждаем: если мы регистрируем спектр КР целой клетки, то какие колебания мы увидим?
Во-первых, сразу все, что есть в клетке. А клетка — это сложнейший по составу «раствор». Во-вторых, колебания только тех молекул, которых много, потому что сигнал КР обладает низкой интенсивностью (и это один из существенных недостатков метода). Именно поэтому, из-за сложности интерпретации спектров и недостаточно мощного оборудования, метод не получил широкого распространения среди биологов. И только в 1990-м году после совмещения КР-спектрометра с конфокальным микроскопом появилась возможность регистрировать КР целых клеток или отдельных участков клетки [6]. И в последние годы метод наконец-то приобрёл популярность, притом заслуженную, так как спектроскопия КР обладает существенными преимуществами перед другими методами и, главное, позволяет получать эксклюзивную информацию.
Основное преимущество спектроскопии КР — неинвазивность! В чём она проявляется? Во-первых, с помощью КР можно изучать биохимический состав клеток, не разрушая их. Подобную информацию можно получить только «разрушающими» технологиями, такими как масс-спектрометрия и хроматография. Во-вторых, не нужно использовать метки или зонды, как для флуоресцентной микроскопии. Это означает, что мы исследуем систему (в данном случае клетку) в естественных условиях. А это крайне важно, учитывая, что многие из существующих меток (как флуоресцентных, так и изотопных) являются токсичными. К тому же исчезает проблема выцветания меток и появляется возможность исследовать небольшие молекулы, к которым трудно пришить метку. В-третьих, можно отметить, что КР позволяет работать с водными растворами, в т.ч. с физиологическими буферами, в отличие от ИК спектроскопии, так как вода сильно поглощает в ИК-области.
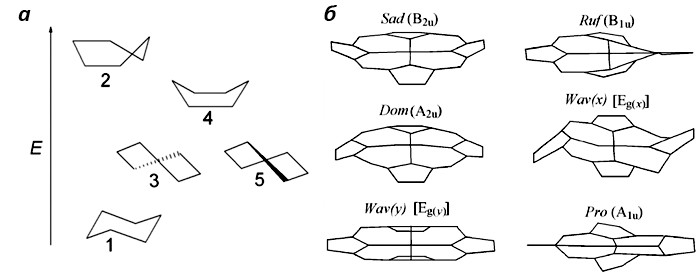
Что касается эксклюзивной информации, то это, в первую очередь, информация о конформации (рис. 4) исследуемых молекул и микроокружении функциональных групп. А от этих параметров может зависеть и активность молекул в клетке, и взаимодействие с другими молекулами, т.е. то, что влияет на работу целой клетки. Исследовать конформацию молекул — это сложная экспериментальная задача. Для её решения можно использовать ИК-спектроскопию, но, опять же, только на высушенных образцах. Можно использовать более сложные и дорогие технологии, такие как рентгеноструктурный анализ и ЯМР. Эти методы позволяют получать целостную картину расположения атомов в молекуле, но очевидно, их пока нельзя использовать для изучения молекул в живой клетке. А спектроскопию КР можно — в зависимости от того, в какой конформации находится молекула, атомы будут колебаться по-разному, что отразится на спектрах [7].
Рисунок 4. Конформации органических молекул. а — различные конформации циклогексана: 1 — «кресло»; 2 — «полукресло»; 3, 5 — «твист»; 4 — «ванна». б — различные конформации гема. Рисунки из «Википедии» и [8].
In vitro
В настоящее время существует множество работ по исследованию клеток методом КР. Основные направления исследований — это изучение распределения веществ в целой клетке [2]; сравнение нормальных и патологических клеток [9]; изучение динамики некоторых клеточных процессов [3]. Например, КР использовали для выявления патологических или раковых клеток, изучения процессов апоптоза и дифференцировки, изучения распределения лекарств в клетке и т.д. [7, 11–13].
In situ
КР-спектроскопию применяют и для исследования целых органов и тканей, не изымая их из организма. Это возможно благодаря тому, что не нужно специальной подготовки образца, введения специфических меток и т.д. Так, в 2007-м году появился маленький эндоскоп на основе КР-спектрометра для исследования пищевода крыс [14]. А в нашей лаборатории даже удалось зарегистрировать КР от целого сердца [15].
Такая разная спектроскопия КР
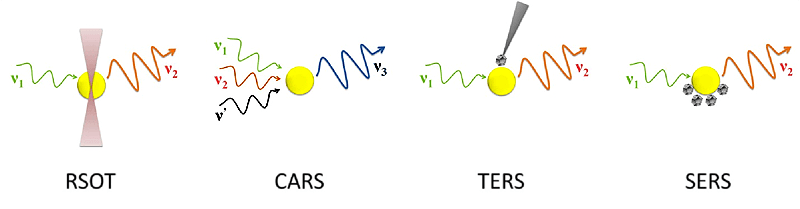
Итак, спектроскопия КР позволяет неинвазивно получать уникальную информацию о конформации и микроокружении молекул внутри живых клеток. Однако, как и любой метод, КР имеет свои ограничения. И, в первую очередь, это низкая интенсивность сигнала. Именно эту проблему решают различными модификациями метода КР [9] (рис. 5).
Рисунок 5. Методы, позволяющие усилить сигнал КР. Обозначения: ν1 — частота возбуждения, ν2 — стоксово КР, ν3 — антистоксово КР, ν’ — переменная частота. Желтый круг — исследуемая молекула, серый многогранник — наночастица. Обсуждение в тексте.
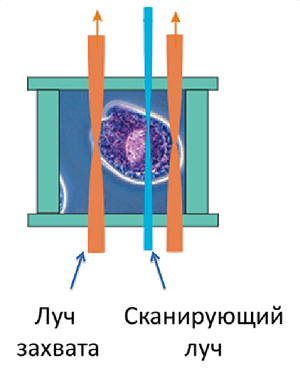
Рисунок 6. Схема установки для изучения одиночных клеток методом RSOT с двумя лучами захвата. Рисунок из [16].
Первый и самый простой способ усилить сигнал КР — использовать резонансную частоту возбуждения. Т.е. когда частота возбуждения попадает в область поглощения вещества, то наблюдается резонансное комбинационное рассеяние (РКР, англ. resonance Raman spectroscopy, RR), интенсивность которого на несколько порядков превышает обычное КР [3].
Второй любопытный способ — это спектроскопия КР с оптическим пинцетом (RSOT — Raman Spectroscopy Optical Tweezers), которая позволяет увеличивать интенсивность КР за счет увеличения времени накопления сигнала от одиночных молекул или клеток в растворе, при этом не осаждая и не фиксируя их [16]. Оптический пинцет — это прибор, который позволяет манипулировать микроскопическими объектами с помощью лазерного света: частички попадают в фокус лазерного луча как в ловушку [17]. Для исследования клеток чаще всего используют два лазерных луча-ловушки, чтобы избежать флуктуаций и вращения объекта (рис. 6). Также с помощью двух лучей можно растягивать клетку. Например, для эритроцита было показано, что растяжение клетки приводит к деоксигенации гемоглобина [18].
Как было показано выше (рис. 2), стоксовые линии КР (ν0−Δν) гораздо интенсивнее антистоксовых (ν0+Δν). При этом антистоксовые линии представляют больший интерес, потому что в этой области отсутствует люминесценция образца (из-за Стоксова сдвига). Как же получить интенсивный спектр антистоксового КР? Оказывается, способ есть, и называется он КАРС — когерентное антистоксовое рассеяние света (Сoherent anti-stokes Raman scattering, CARS).
В КАРС-спектроскопии используется не один источник света, а три: первый источник называется волной накачки (pump) — ν1, второй представляет собой излучение со стоксовой частотой ν2, а третий — это пробный луч, частота которого плавно изменяется ν’. Эти лучи взаимодействуют друг с другом, а также с колебаниями молекул исследуемого вещества. Если разность частот ν1−ν2 входит в резонанс с собственными колебательными частотами молекулы, то возникает интенсивное когерентное (т.е. согласованное по фазе колебаний) антистоксово излучение (с частотой ν3 = ν1 − ν2 + ν’) [19, 20].
Помимо большей интенсивности и отсутствия люминесценции, на спектрах КАРС легче различать близкорасположенные пики, благодаря когерентности рассеянного света, что особенно важно при изучении структурно схожих биомолекул [19]. Большинство современных приложений данного метода связано с изучением липидов. Так, методом КАРС визуализировали движение везикул внутри клеток; процесс дифференцировки жировой ткани; изучали метаболизм липидов, в т.ч. влияние небезызвестной омеги-3; по липидному составу попытались различить здоровую и раковую нервную ткань и т.д. [20].
SERS и TERS
И, наконец, самый мощный способом добиться усиления сигнала КР — поместить молекулу вблизи наночастиц благородных металлов. Для этого есть два способа: поместить наночастицу (НЧ) на поверхность иглы атомно-силового микроскопа [21] и зондировать исследуемые молекулы, регистрируя с них сигнал КР. В этом случае метод будет называться TERS (tip-enhanced Raman spectroscopy). Во втором случае исследуемые молекулы помещают на поверхность НЧ металла и регистрируют КР обычным способом. Этот метод называется гигантское комбинационное рассеяние (ГКР) или SERS (surface enhanced Raman spectroscopy) [9]. На мой взгляд, ГКР — самая удачная разновидность КР, позволяющая получать наибольшее усиление сигнала и обладающая множеством практических применений, поэтому о ней и пойдет речь.
Метод ГКР основан на эффекте плазмонного резонанса, о котором уже писали в статье на биомолекуле [22]. Плазмонный резонанс — это резонанс частоты падающего света и частоты коллективных колебаний свободных поверхностных электронов металла (квант таких колебаний называется плазмон). Плазмонный резонанс приводит к многократному усилению электрического поля вблизи НЧ металла — таким образом, НЧ металла выступают в качестве «наноантенн». И теоретически это усиление может достигать 14 порядков, т.е. 100 триллионов раз! [23].
Спектроскопия ГКР: от молекул к клеткам
Впервые явление усиления сигнала КР наблюдал Флейшманн с коллегами, которые опубликовали свое открытие в 1974 году. Они получили сигнал ГКР молекул пиридина, адсорбированного на шероховатом серебряном электроде [24]. Довольно долгое время существовала концепция усиления сигнала КР от молекул, адсорбированных на поверхности электродов и наноструктур. Но для биологии, очевидно, это не самый удачный подход.
В начале 90-х годов с развитием КР-микроскопии метод ГКР применили к живым клеткам. Для изучения живых клеток с помощью спектроскопии ГКР существовало несколько подходов, но все они предполагали введение в клетку НЧ. Одной из первых работ по введению НЧ в клетку путём эндоцитоза была работа нашего соотечественника И.Р. Набиева с соавт. по изучению взаимодействия антибиотика доксорубицина с ДНК на культуре клеток [25]. Позже появляются работы по помещению клеток на особые наноструктурированные поверхности [26, 27]. Однако все они были сопряжены с одной трудностью — расстояние между исследуемой молекулой и наноструктурой должно быть очень маленьким — до 10 нм. Поэтому в этих работах либо изучалось распределение в клетке некоторых веществ, которые сами по себе имели очень интенсивный сигнал КР, либо изучались строение и динамика плазматических мембран, которые как раз и адсорбировались на наноповерхностях. Это значительно ограничивало исследователей, и интерес к использованию ГКР-подложек временно угас.
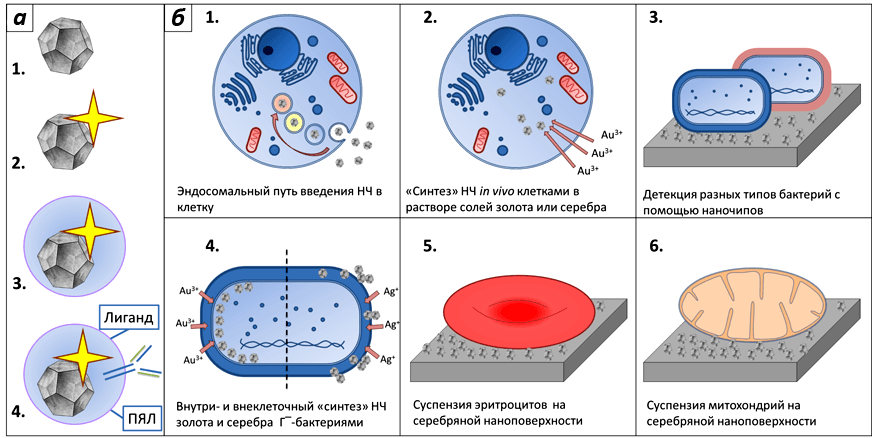
Тем не менее работы по внутриклеточному ГКР продолжались и на эукариотических клетках, и на бактериях. Основные стратегии эксперимента ГКР на живых клетках показаны на рисунке 7 в хронологическом порядке.
* — Спектр ГКР данной молекулы-репортера известен, а также известно, как он меняется в зависимости от ближайшего окружения молекулы.
Новые концепты
Следует заметить, что большинство стратегий ГКР-измерений на живых клетках представляют собой либо изучение распределения внутри клеток определенной чужеродной молекулы (например, какого-то лекарства), к которой пришиты НЧ. Но то же самое можно сделать и другими более распространенными методами — например, флуоресцентной микроскопией. К тому же внедрённая в клетку металлическая НЧ вряд ли менее токсична, чем флуорофор. Другой подход применения ГКР на живых клетках — регистрация спектров от собственных молекул клетки, например, от всех липидов и всех белков (пептидных связей), находящихся в плазматической мембране или в эндосоме, что тоже сужает круг возможных практических применений метода.
Основная сложность при работе методом ГКР — это необходимость комплексного междисциплинарного подхода. Помимо того, что нужно хорошо разбираться в объекте исследования, для каждого объекта нужны свои уникальные параметры регистрации спектров и самое главное — специальные наноструктуры. Поэтому, чтобы поставить хороший эксперимент, нужно знать и химию, и биологию. И вполне естественно, что любая успешная попытка зарегистрировать какой-то сигнал от биомолекулы — уже большое достижение.
Однако для исследования фундаментальных биологических процессов этого мало. Новый концепт исследований клеток методом ГКР был предложен в 2009-ом году сотрудниками нашей лаборатории Н.А. Браже с соавт. Они показали, что есть сигнал от молекул (собственных молекул клетки), которые находятся непосредственно под мембраной клеток, смешанных с коллоидным раствором наночастиц серебра [36].
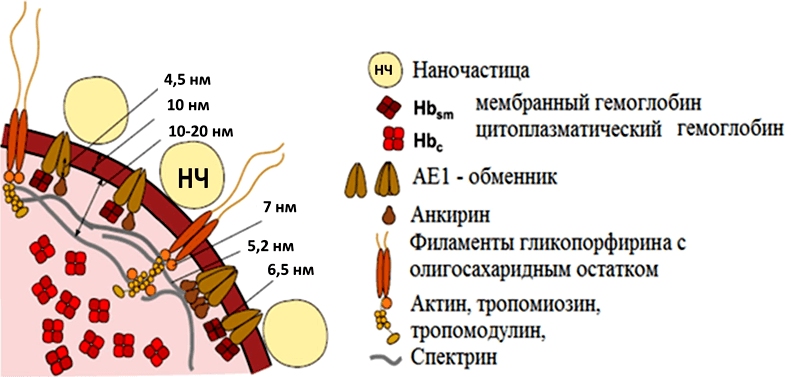
И произошло это из любопытства, когда вместо того, чтобы смешать с НЧ серебра раствор гемоглобина, исследователи использовали суспензию эритроцитов — и получили при этом сигнал ГКР гемоглобина. Поначалу это казалось странным, ведь толщина мембраны эритроцита около 10 нм — это как раз то предельное расстояние, на котором может возникать усиление сигнала. Однако такое открытие было связано как с выбором частоты излучения (вспомним резонансное КР), так и с удачной морфологией агрегатов наночастиц серебра на поверхности эритроцитов, ведь от этого зависит расстояние, на котором происходит усиление сигнала КР, и в данном случае оно было заведомо больше 10 нм. А сам сигнал соответствовал не всему гемоглобину в клетке, а только тем молекулам гемоглобина, которые были вблизи мембраны — примембранному гемоглобину (рис. 8).
Рисунок 8. Срез эритроцита в области контакта с НЧ. В эритроците есть два типа гемоглобина: цитоплазматический и примембранный (который составляет не более 0,5% от всего гемоглобина в клетке). Спектр КР эритроцитов — это спектр всего гемоглобина в клетке, точнее, того, которого больше (т.е. цитоплазматического). А спектр ГКР — это спектр того гемоглобина, который ближе к поверхности НЧ, т.е. примембранного гемоглобина. Этого гемоглобина так мало, что увидеть его конформацию другими методами in vivo невозможно. Рисунок из [36].
Но одной удачи далеко не достаточно. Несовершенством коллоидных растворов являлось уже то, что они все в некоторой степени токсичны для клеток и, кроме того, могут приводить к осмотическому шоку. И прошло более тех лет после первого наблюдения ГКР на эритроцитах, прежде чем совместно с группой материаловедов под руководством член-корр. РАН д.х.н. Гудилина Е.А. был разработан новый тип нетоксичных наноструктурированных поверхностей, позволяющих исследовать примембранный гемоглобин в интактных эритроцитах [37]. «Большинство работ, использующих метод ГКР в биологии, имеют описательный характер», — говорит к.б.н. Н.А. Браже. — «Но в идеале ГКР спектроскопия должна быть использована не только с маркерными целями, но и для проведения фундаментальных исследований функциональных изменений в структуре и свойствах молекул в клетках и тканях».
Избрав свою стезю фундаментального применения метода ГКР, учёные совершили следующее открытие в 2015-м году. Было обнаружено, что спектр ГКР целых функционирующих митохондрий — это спектр исключительно гема цитохрома с — мобильного переносчика электронов в митохондриях [38]. Его конформация постоянно изменяется во время работы (рис. 4б), и от этого зависит скорость электронного транспорта в митохондриях и, следовательно, эффективность обеспечения клеток энергией. Кроме того, определённое изменение конформации цитохрома с вызывает его выход из митохондрий, что запускает процесс апоптоза — запрограммированной клеточной гибели. Поэтому изучение такого фундаментального процесса как конформационные изменения цитохрома с представляет практический интерес. И это открытие означает, что можно изучать конформационные изменения такого важного белка в естественной «среде обитания», не выделяя его и не модифицируя, а просто помещая суспензию митохондрий на серебряную подложку и регистрируя спектр ГКР.
И в этом основная прелесть и новшество — теперь методом ГКР можно изучать молекулы, которые находятся непосредственно под мембраной живых клеток и мембранных органелл. При этом именно изучать их: исследовать изменения, которые с ними происходят в норме и при патологии.
Подводя итоги
Спектроскопия КР — это яркий пример метода, который обретает вторую жизнь с появлением новых технических возможностей. Благодаря различным модификациям КР, которые позволяют значительно усиливать сигнал, появилась возможность исследовать конформацию различных биомолекул в живых клетках и органах, что недоступно другим методам. А это значит, что с помощью КР мы каждый раз получаем принципиально новые знания о живой системе. Не в этом ли смысл науки?